作者简介:贾学静(1988-),男,四川广元人,在读硕士。E-mail:jiaxjsicau@gmail.com
以金心吊兰叶片边缘的绿色区域与中心黄白色区域为材料,研究了干旱胁迫对其活性氧及其清除系统的影响,结果表明,1)随着胁迫时间的延长,叶片各区域的过氧化氢(H2O2)、超氧阴离子(
The effects of drought stress on reactive oxygen species and their scavenging systems of leaf blade and the center parts of Chlorophytum capense var. medio-pictum were studied. 1) The content of H2O2,
在众多环境因子中, 干旱是影响植物生理生态最主要的非生物胁迫因子之一[1]。研究干旱对植物的影响主要有自然干旱[2]和模拟干旱[3]2种形式。自然干旱需在田间或者大棚中进行, 这其中有许多不可控因素, 如:风, 温度等。模拟干旱可以在人工气候箱中进行试验, 更加接近理想的实验条件, 聚乙二醇6000(Polyethylene Glycol-6000, PEG-6000)是一种渗透调节剂, 可以阻塞植物的输导组织, 是理想的干旱模拟剂, 因此许多学者利用PEG-6000模拟干旱, 对植物的抗旱性作了大量的研究[3, 4, 5]。
植物在正常情况下, 体内活性氧的产生与清除处于动态平衡状态。干旱胁迫后, 体内会产生大量的活性氧, 相应产生清除活性氧的抗氧化物质和抗氧化酶[5]。对活性氧的清除主要由两大抗氧化系统, 一是酶类清除系统, 包括超氧化物歧化酶(SOD), 过氧化物酶(POD)等, 二是非酶类抗氧化剂系统, 包括维生素C、β -胡萝卜素等[6]。当植物在胁迫条件下体内产生的活性氧超出了自身的清除能力后, 这些过量的活性氧可能会有3种形式在细胞内起作用, 1)作为信号激活细胞的防御机制; 2)作为信号激活细胞的程序性死亡; 3)直接氧化和破坏细胞, 严重会引起植物的死亡[7]。
金心吊兰(Chlorophytum capense var. medio-pictum), 又名斑心宽叶吊兰, 为宽叶吊兰的园艺栽培变种, 叶片中心为黄白色, 边缘为绿色, 形成绿-黄白-绿的嵌合纵条纹[8]。吊兰属植物耐阴性强, 是室内极佳的观赏植物, 能吸收甲醛、二甲苯等有毒气体, 是一种良好的室内空气净化花卉。吊兰体内的甾体皂苷具有一定的抗癌活性[9]。吊兰被广泛用于园林绿化中, 园林栽培植物常常会面临各种环境的胁迫而影响其美化效应, 目前, 干旱胁迫对其影响未见报道。
金心吊兰的叶片绿色部分和黄白色部分之间有一定宽度的淡绿色渐变带, 此渐变带背面呈黄绿色[8]。本研究以金心吊兰及其野生型全绿吊兰为试验材料, 选用金心吊兰叶片边缘的绿色部分和中心的黄白色部分, 以及野生型全绿吊兰相对应的边缘和中心部分, 研究在干旱胁迫下, 金心吊兰同一叶片不同颜色区域中活性氧的积累及清除情况, 并以此来评价金心吊兰的抗旱性, 这可为金心吊兰的栽培应用提供一定的理论依据。
实验材料选自四川农业大学校园绿化带内栽培的金心吊兰及其野生型全绿吊兰, 分别于2012年5月10日采集后, 去掉泥土和腐烂的老叶, 栽培于灭菌后的石英砂上, 置于人工气候箱中(20℃, 12 h光照/12 h黑暗, 相对湿度60%), 定时浇灌完全Hoagland培养液。生长至6月25日, 选取长势一致的苗株各12株, 分别给予10%, 20%, 30%浓度的PEG-6000处理, 以不加PEG-6000为对照。处理0, 2, 4, 6 d后, 采集其从顶端往下第4片成熟叶中段测定生理指标, 各处理取样3次重复, 指标测定时各样品重复测定3次。
叶绿素原位荧光检测, 分别采集金心吊兰及其野生型全绿吊兰叶片的边缘和中心部分做冰冻切片, 然后将切片放于Olympus DP71荧光显微镜下, 观察并照相(FITC, EX465-495, DM505, BA515-555)。叶绿素和类胡萝卜素的含量测定参考袁明等[10]的方法。丙二醛(MDA)含量的测定采用硫代巴比妥酸法[11]。过氧化氢(H2O2)含量与超氧阴离子(
用隶属函数法[15]对金心吊兰及其野生型全绿吊兰的边缘与中心部分的抗旱性进行综合评价。用下式计算每个样品各项指标的具体隶属函数值:Xu=(X-Xmin)/(Xmax-Xmin), 式中, X 为参试样品某一抗旱指标的测定值, Xmax, Xmin分别为所有试样中该指标的最大值和最小值, 若某一指标与抗旱性呈负相关, 可通过反隶属函数计算其隶属函数值, 公式为:Xu=1-(X-Xmin)/(Xmax-Xmin), 最后把每个试样各项指标隶属函数值累加, 取其平均值, 根据各样品平均隶属函数值大小确定其抗旱性强弱。平均值越大, 抗旱性越强, 反之, 抗旱性越弱。
所得数据均用Excel 2007和SPSS 19进行处理分析, 并使用t-检验对样本间差异性进行显著性检测, 图中数据为平均值± 标准误差。
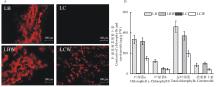
叶片经冰冻切片后, 将切片置于Olympus DP71荧光显微镜下检测叶片横截面的叶绿素原位荧光, 如图1所示, 金心吊蓝绿色部分与野生型全绿吊兰边缘部分的叶绿体数量, 分别多于金心吊兰黄白色部分和野生型全绿吊兰中心部分。在金心吊兰的黄白色部分(图1A)未检测到叶绿素的荧光, 说明叶绿素含量极低, 无典型的叶绿体。野生型全绿吊兰的边缘部分的叶绿体数量明显多于中心部分(图1 A)。
从叶绿素含量的定量分析(图1B)显示, 全绿吊兰的边缘部分叶绿素含量为其中心部分的1.9倍, 其中叶绿素a为中心部分的2.1倍, 叶绿素b的分布无明显的位置效应。对金心吊兰而言, 其边缘部分总叶绿素、叶绿素a和叶绿素b含量分别为中心的91.5, 98.3和77.1倍, 扣除吊兰叶绿素分布的位置效应, 金心吊兰中心部分的叶绿素积累明显受到抑制。金心吊兰边缘部分的叶绿素含量略高于野生型。
在植物体内的H2O2主要产生于线粒体、叶绿体和过氧化物酶体中, 线粒体中约1%5%氧被用于产生H2O2[7], 随着PEG-6000胁迫浓度的增加, 金心吊兰和野生型全绿吊兰的H2O2含量也逐渐增加, 且随着胁迫时间的增加, H2O2含量随之而上升(图2)。金心吊兰和野生型全绿吊兰的边缘部分H2O2含量总是高于各自的中心部分, 都在第6天达到最高含量。在30%浓度胁迫下, 随着胁迫时间的延长, 野生型全绿吊兰边缘部分H2O2含量增幅最大, 达到90.2%。而金心吊兰黄白色部分变化幅度较小, 仅发生小幅变化。
随着胁迫时间的增加, 在不同浓度PEG-6000胁迫下, 金心吊兰边缘的绿色部分和黄白色部分的
10%, 20%和30%浓度PEG-6000处理后, 金心吊兰和野生型全绿吊兰叶片中的MDA含量随着浓度的增加而一直上升。随着胁迫天数的增加, 金心吊兰和野生型全绿吊兰叶片中的MDA含量一直上升, 并在第6天达到最大值(图4), 金心吊兰的边缘与中心部分分别为各自胁迫处理前实验组的3.7, 5.0, 6.2倍和2.9, 3.2, 7.2倍, 野生型全绿吊兰的边缘与中心部分分别为各自胁迫处理前实验组的4.7, 5.3, 6.8倍和5.8, 6.7, 7.8倍。从图中可以看出边缘部分显著高于中心部分的MDA含量(P< 0.05), 表明边缘部分的膜脂过氧化程度更强, 受到的破坏更严重。
不同浓度PEG-6000胁迫后, SOD活性曲线显示(图5), 随着胁迫时间的增加, 金心吊兰与野生型全绿吊兰的SOD活性都出现了先上升后下降的趋势, 在第4天达到最大值。金心吊兰和野生型全绿吊兰的边缘部分的SOD活性高于中心部分(P< 0.05)。金心吊兰边缘部分在10%, 20%和30%胁迫下SOD活性增幅分别为45.5%, 54.9%和57.5%。而金心吊兰黄白色部分增幅稍大于其边缘部分, 分别为64.6%, 69.9%和72.5%。在野生型全绿吊兰边缘部分的SOD活性增幅也小于中心部分。
不同浓度PEG-6000胁迫后, POD活性变化趋势显示(图6), 金心吊蓝绿色部分的POD活性显著高于中心黄白色部分(P< 0.05)。随着胁迫时间的增加, 金心吊蓝绿色部分与中心黄白色部分的POD活性先上升后下降的趋势, 都在第4天达到最大值, 分别是各自胁迫处理前POD活性的14.4, 17.5, 30.2倍和4.6, 6.9, 7.9倍。野生型全绿吊兰边缘部分与中心部分也呈现出先上升后下降的趋势, 在开始胁迫时候中心部分的POD活性高于边缘部分, 第4天时, 在30%胁迫浓度下, 野生型全绿吊兰边缘部分POD活性小于中心部分。这可能是在胁迫初期, 金心吊兰体内产生了过量的活性氧自由基
用模糊函数隶属法对金心吊兰及其野生型全绿吊兰的边缘和中心部分H2O2含量,
| 表1 耐旱指标隶属值及耐旱性综合评价 Table 1 Subordinate function values of drought resistances and comprehensive evaluation of four samples |
当植物受到逆境胁迫时, 体内活性氧产生与清除机制失衡, 造成细胞中活性氧迅速积累, 对植物膜脂、蛋白质和其他细胞组分造成伤害, 乃至细胞死亡[16]。本研究中用不同浓度的PEG-6000模拟干旱胁迫, 通过金心吊兰及其野生型全绿吊兰的边缘与中心部分
金心吊兰及其野生型全绿吊兰的边缘与中心部分的
叶绿素是植物进行光合作用的物质基础, 在光合作用中起着吸能和转能的作用。叶绿素含量的高低在很大程度上反映了叶片光合作用的强弱, 并在一定程度上可以作为叶片衰老的指标[21]。本研究中, 吊兰叶片的抗旱性与叶绿素含量呈负相关, 即叶绿素含量较高的部分抗旱性较差(表1)。Yuan等[22]研究发现和野生型相比较, 叶绿素缺少的大麦(Hordeum vulgare)突变体(NYB)对干旱不敏感, 这与本研究的结果相似。金心吊兰叶片的叶绿素含量为215.6 μ g/g, 全绿野生型吊兰叶片的叶绿素含量为367.2 μ g/g, 全绿野生型吊兰叶片的叶绿素含量是金心吊兰叶片的1.7倍(数据未列出), 金心吊兰叶片含有较低的叶绿素含量, 具有较强的抗旱性。
叶绿体是植物细胞内活性氧产生的主要部位, 当植物面临环境胁迫时, 叶绿体、线粒体和过氧化物酶体就会产生过量的活性氧, 从而导致植物对各种胁迫做出应答, 过量的活性氧会与蛋白质, 脂质等发生反应, 破坏植物细胞, 严重会引起植物的死亡[5]。金心吊兰及其野生型全绿吊兰叶片边缘和中心部分的叶绿体如图1所示, 其分布表现出明显的位置效应, 边缘部分的数量多于中心部分。
金心吊兰及其野生型全绿吊兰叶片的抗旱性呈现位置效应, 同一植株同一叶片的不同叶绿素含量区域, 对干旱胁迫的耐受性不同。本研究中, 金心吊兰中心部分的抗旱性高于其边缘部分(表1)。吊兰叶片抗旱性具有位置效应的原因可能是在其叶片的中部存在大量的维管组织[8], 主要用于水分和养料的运输。另一方面, 中心部分的叶绿素含量低, 捕获的光能少, 其产生的对自身有害的活性氧自由基也就偏少, 从而面临较低水平的氧化胁迫。关于植物叶片位置相应对抗逆性的影响, 是否具有普遍意义有待进一步研究。
通过隶属函数分析法对金心吊兰及其野生型全绿吊兰的抗旱能力进行综合评价得出:金心吊兰抗旱性高于野生型全绿吊兰, 使得金心吊兰比野生型全绿吊兰更不容易受到干旱胁迫的影响, 这为金心吊兰作为绿化中选择适当的干旱地区栽培提供了一定的理论依据。但是在吊兰体内的抗氧化分子机制如何响应干旱胁迫, 有待进一步研究。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|