作者简介:胡可(1986-),男,四川江油人,硕士。E-mail: djydjy_122@163.com
木质素作为维管植物的重要成分之一,主要存在于细胞的次生壁中。然而,木质素却是许多工农业加工过程的限制因素,例如在化学制浆、牧草消化以及木质纤维转化为生物酒精等过程中。肉桂酰辅酶A还原酶(CCR)和肉桂醇脱氢酶(CAD)是催化木质素单体生物合成最后两步的关键酶。本研究根据NCBI中黑麦草 CCR和 CAD基因序列设计特异引物并添加相应酶切位点,从野生型多年生黑麦草cDNA分离克隆 CCR和 CAD基因片段,分别构建了含正反方向目的片段的植物表达干扰载体p23-iCCR和p23-iCAD。通过根癌农杆菌EHA105介导转入多年生黑麦草胚性愈伤组织,经过巴龙霉素筛选和PCR检测获得导入了干扰 CCR和 CAD基因片段的转基因株系i-CCR和i-CAD。常规方法测定相对木质素含量,结果显示,与对照相比,有9株i-CCR植株和11株i-CAD 植株木质素含量显著降低,分别平均降低了34.67%,33.86%,且生长正常。本研究表明通过干扰 CCR和 CAD基因表达,可以获得低木质素含量的多年生黑麦草,为进一步培育易消化吸收的黑麦草提供了良好的种质资源。
Lignin, one of the main components in vascular plants, is mainly present in the walls of secondarily thickened cells. However, it is a limiting factor in a number of agro-industrial processes, such as chemical pulping, forage digestibility, and lignocellulosic-to-bioethanol conversion. Cinnamoyl CoA reductase (CCR) and cinnamyl alcohol dehydrogenase (CAD) are two key enzymes that catalyse the penultimate and ultimate steps respectively in the biosynthesis of monolignols. Based on the CCR and CAD gene sequences of perennial ryegrass ( Lolium perenne) from NCBI, specific primers were designed to add appropriate restriction enzyme sites to amplify and clone the two gene fragments from cDNA of perennial ryegrass. Two RNA interference (RNAi) vectors (p23-iCCR and p23-iCAD) were constructed using inverse repeat fragments. The constructs were introduced into embryogenic calli of perennial ryegrass by Agrobacterium-mediated transformation with EHA105. They were screened using paromomycin and detected by PCR, and independent i-CCR and i-CAD transgenic plants were obtained. Analysis of relative lignin content was conducted by conventional methods. The lignin content was distinctly reduced compared with that of wild controls in 9 plants of i-CCR and 11 plants of i-CAD transgenic plants. The lignin content of these i-CCR and i-CAD plants was reduced by 34.67% and 33.86% respectively. The transgenic plants had normal morphology and grew well. This study showed that low-lignin-content perennial ryegrass could be obtained by silencing CCR and CAD gene expression and has provided novel germplasms for breeding digestible and improved absorption ryegrass.
木质素是一种复杂的芳香族化合物多聚体, 主要存在于植物细胞的次生壁, 与纤维素和半纤维素共价结合, 赋予细胞壁强度和硬度, 为植物组织提供机械支持, 使得植株向上生长。木质素还使植物的脉管组织具有疏水性, 便于水分和营养物质的长距离运输[1], 还能保护植株避免病原体入侵[2]。在大多数被子植物中, 木质素主要由愈创木基木质素(G-lignin)和紫丁香基木质素(S-lignin)这两种木质素单体亚单位构成, 它们分别来自松柏醇和芥子醇, 第三种木质素单体亚单位对羟基苯基木质素(H-lignin)来自香豆醇, 它在单子叶植物中相对较多, 而在双子叶植物中较少[1]。图1为木质素合成途径[3, 4]。
木质素作为维管束植物细胞壁的主要成分, 长期以来被认为不利于饲料品质、造纸和纤维素燃料的生产[5]。例如, 在制浆造纸工业中, 需通过严格的化学工艺从木材中去除木质素以获得纯的纤维素纤维[6]。在草料消化和生产乙醇时木质素也是主要的限制因子[7]。因此, 低木质素含量的牧草或者木材的培育, 是育种的方向之一。如今大部分研究主要是通过基因工程手段降低植株的木质素含量或者改变其组成。
木质素单体作为组成木质素的亚单位, 产生于苯丙氨酸途径的一个分支(图1)[3, 4], 肉桂酰辅酶A还原酶(cinnamoyl CoA reductase, CCR)和肉桂醇脱氢酶(cinnamyl alcohol dehydrogenase, CAD)是催化木质素单体生物合成最后两步的关键酶。许多研究通过在不同植物中抑制这两种酶的表达降低了木质素含量或是改变了木质素的组成[1]。
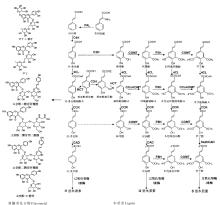 | 图1 苯丙烷和木质素单体生物合成途径, 重点显示了木质素单体的合成途径[3, 4]Fig.1 Phenylpropanoid and monolignol biosynthetic pathways mainly showing biosynthesis pathways of monolignols |
CCR是木质素特异途径的关键酶之一, 在木质素的生物合成中起着重要作用, 它以5种羟基肉桂酸的CoA 酯(对-香豆酰辅酶A、咖啡酰辅酶A、阿魏酰辅酶A、5-羟基阿魏酰辅酶A和芥子酰辅酶A)作为底物催化生成相应的肉桂醛。CCR1基因表达受影响的拟南芥(Arabidopsis thaliana)突变体, 木质素含量降低的同时表现出外形矮小、衰老延缓的性状[8]。CCR下调的转基因杨树(Populus tremula× Populus alba)木质素含量可降低50%, 其中S-lignin比G-lignin减少得更多, 另外半纤维素、果胶和木聚糖的合成也减少, 外层木质部表现出橙棕色且着色不均, 并且伴随着纤维素比例的增加, 改善了制浆特性[9]。CCR下调的烟草(Nicotiana tabacum)木质素含量降低, 而CAD下调植株的木质素中含有更多的醛类物质, 转录和代谢研究表明木质素合成途径与其他代谢途径相关联[10]。玉米(Zea mays) CCR1基因插入突变体(Zmccr1-), CCR1基因的表达量只有野生型的31%, 其木质素含量有所下降且结构明显改变, H-lignin含量明显下降, S/G略有上升, 并且消化性能提高, 但未影响植株的生长发育[11]。另外, 由于苯丙氨酸代谢途径不仅生成木质素, 还生成其他的植物次生代谢物, 如类黄酮、羟基苯乙烯、单宁酸等酚类化合物, 因此, 可通过降低木质素的生物合成来促进有益的可溶性酚类化合物生成。在干扰CCR基因的转基因番茄(Solanum lycopersicum)中, 木质素含量降低, 同时茎和叶中可溶性酚类物质的总含量增加, 组分分析显示绿原酸和芦丁等含量增加, 果实中酚类物质总量没有增加, 但是组分发生改变, 相应地提高了番茄提取物的抗氧化能力[12]。
CAD催化木质素单体生物合成的最后一步, 将3种肉桂醛(对-香豆醛、松柏醛和芥子醛)还原生成相应的3种肉桂醇。Saathoff 等[13]通过RNAi下调柳枝稷(Panicum virgatum)中CAD表达, 发现这些植株茎中催化松柏醛和芥子醛的CAD活性下降, 总木质素含量和表皮素含量也明显降低, 且经过氢氧化铵预处理和纤维素酶消化的研磨样品释放出的葡萄糖也多于野生型对照。Fornalé 等[14]利用RNAi下调玉米CAD基因表达, 结果显示在不同组织中CAD下调的程度不同, 转基因植株细胞壁的成分发生变化, 茎的细胞壁总木质素含量未受影响, S/G比例稍有下降, 并且积累了更多的纤维素和木聚糖, 而中脉的细胞壁总木质素含量和多糖含量下降, 转基因植株与野生型相比表型没有改变, 但更容易降解, 乙醇产量也较高。RNAi下调亚麻(Linum usitatissimum)中的CAD后, 木质素前体物质含量显著提高, 木质素、果胶和半纤维素含量降低, 转基因植株的弹性增加[15]。RNAi下调CAD1的转基因烟草, 植株生长发育正常, 木质素含量未受影响, 仅G-lignin略有减少[16]。还有研究将拟南芥2种CAD基因(CAD C和CAD D)的突变体和CCR1的突变体杂交后发现其木质素含量比野生型减少了31%, 木质素结构也发生改变, 但植株严重矮化并伴有雄性不育症状[17]。
综上所述, 利用RNAi技术并结合转基因方法, 在多种植物中, 可以通过降低木质素合成途径中相应酶的表达而获得木质素含量降低或者木质素组成改变的转基因植物。RNAi是由双链RNA 分子介导的、在mRNA 水平关闭相应基因表达的过程。因为RNAi 技术简单易行, 抑制基因表达效率高, 已被广泛应用于真核生物基因功能的研究[18]。
多年生黑麦草(Lolium perenne)是禾本科黑麦草属(Lolium)植物, 是优良的牧草和草坪草, 但自交不亲和, 传统育种困难而复杂。随着现代生物技术的发展, 转基因技术已成为黑麦草遗传改良的有力工具, 可通过RNAi方法和转基因技术获得木质素含量降低的黑麦草[4]。
本研究在本实验室已建立的多年生黑麦草转化体系上[19], 优化转化方法, 通过根癌农杆菌(Agrobacterium tumefaciens)介导的RNAi技术, 降低多年生黑麦草中CCR、CAD基因表达, 以期获得低木质素含量的多年生黑麦草新材料, 为进一步培育高消化利用率的多年生黑麦草提供种质资源。
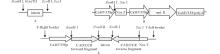
多年生黑麦草品种“ 雅晴” , 由百绿草业公司惠赠。本实验在中国科学院成都生物研究所于2010年9月至2012年4月期间进行并完成。根癌农杆菌EHA105由本实验室保存。植物表达载体p2355由中国科学院成都生物研究所马欣荣实验室在pCAMBIA2301基础上构建, 外源基因由多克隆位点区插入; 中间载体pSK-int由四川省农业科学院黄维藻博士惠赠。载体示意图见图2。
根据NCBI中的黑麦草CAD(登录号:AF472591.1)和CCR(登录号:AF278698.1)基因cDNA序列, 选取其中约200300 bp的片段, 应用Primer 6.0软件, 分别设计CAD和CCR正、反向目的片段的上下游2对引物(表1), 正向片段和反向片段引物的扩增序列相同, 而酶切位点不同, 以使目的片段定向插入载体中。
| 表1 用于扩增CAD、CCR正、反向片段的寡核苷酸引物 Table 1 Sequences of oligonucleotide primers used for amplification of CAD, CCR fragments |
预期CAD片段长度256 bp, 加酶切位点12 bp, 共计268 bp; CCR片段长度194 bp, 加酶切位点12 bp, 共计206 bp。
提取新鲜的野生型黑麦草叶片总RNA, 用 RT-PCR试剂盒(TaKaRa)反转录成cDNA, 作为扩增目的片段的模板。用引物cad-1和cad-2、ccr-1和ccr-2分别PCR扩增出CAD和CCR的正向片段(表1)。扩增条件为94℃ 5 min; 94℃ 45 s, 55℃ 45 s, 72℃ 45 s, (35 个循环); 72℃ 7 min。扩增产物经1%琼脂糖凝胶电泳, 切下目的条带用DNA Gel Extraction Kit(上海生工)回收后与pMD19-T载体(TaKaRa)连接, 筛选重组子并测序(上海生工), 测序结果用DNAMAN(版本5.2.2)软件进行分析。
以含有CAD或CCR正向片段的重组pMD19-T载体为模板, 分别以cad-3和cad-4、ccr-3和ccr-4为引物, PCR扩增出CAD和CCR的反向片段(表1), 再分别克隆到pMD19-T载体中, 筛选重组子, 酶切验证并测序分析。
含有正向目的片段的重组pMD19-T载体分别经BamH I和Hind III双酶切, 分别回收小片段, 与经相同酶切的中间载体pSK-int连接, 筛选重组子并酶切验证。再将含CAD或CCR反向片段的重组pMD19-T载体分别用EcoR I和Sac I双酶切后, 回收小片段分别插入已经含有CAD或CCR正向片段的重组中间载体相应位点, 筛选重组子, 酶切验证。分别获得含有干扰片段的中间载体pSK-iCAD和pSK-iCCR, 具有发卡结构的干扰片段分别称为iCAD和iCCR。
将重组中间载体分别用BamH I和Sac I双酶切后, 分别获得iCAD 或iCCR目的片段。将目的片段分别插入p2355载体相应位点, 利用变性碱裂解法和双酶切法鉴定重组子。构建的携CAD或CCR目的片段反向重复结构的植物表达载体, 分别命名为p23-iCAD和p23-iCCR, 干扰片段由花椰菜花叶病毒35S启动子(CaMV35Sp)驱动。
热激法将载体p23-iCAD和p23-iCCR分别导入根癌农杆菌EHA105感受态细胞中, 保存于液氮备用。
选取成熟的多年生黑麦草“ 雅晴” 种子, 经过表面灭菌后接种于MS基本培养基[20]中萌发生长。无菌苗可以通过组织培养快速繁殖并长期保存, 每15 d转接1次, 培养基为MS+6-BA 1 mg/L。待试管苗生长到一定长度、分蘖达10个以上时, 取茎节分生区并纵切后置于MS+2, 4-D 5 mg/L愈伤组织诱导培养基中, 诱导愈伤组织生长, 并每隔15 d继代1次, 共继代4次。
将分别含有p23-iCAD和p23-iCCR的根癌农杆菌EHA105均匀涂布在含有50 mg/L Km和20 mg/L Rif的LB平板上, 待长出菌苔后, 刮取适量菌体接种于含200 μ mol/L AS的液体愈伤组织诱导培养基中, 28℃, 200 r/min培养3 h左右, OD600为0.20.5即可用于转化。愈伤组织预先用细胞凋亡抑制剂CHO(100 μ mol/L)处理3 h。侵染前, 菌液中加入适量(10 μ L/mL)10%非离子去污剂F68水溶液。愈伤组织于菌液中浸没5 min后, 置于无菌滤纸上吸去附着的菌液, 然后转入含滤纸(每皿加134 μ L灭菌水)的培养皿进行共培养, 22℃。共培养3 d后, 将愈伤组织接入含200 mg/L抗生素Timentin的除菌诱导培养基中, 2426℃培养。7 d后, 将愈伤组织接入含50 mg/L巴龙霉素(paromomycin)的筛选继代培养基(MS+2, 4-D 3 mg/L)中, 2426℃培养, 14 d筛选继代1次, 共3次。上述培养均为暗培养, 培养基配方参见文献[19]。
之后将生长良好的愈伤组织接入含2 mg/L 6-BA、20 μ g/L 2, 4-D、25 mg/L巴龙霉素的分化培养基。待长出苗后, 移入含50 mg/L巴龙霉素的1/2 MS培养基生根培养。待长出根后, 移入含MS+0.1 mg/L IAA+50 mg/L巴龙霉素的筛选培养基进行最后一轮筛选。分化再生培养条件为2426℃, 16 h光/8 h暗培养。2周之后将发育良好的植株移出, 大棚盆栽。
愈伤组织诱导、继代、分化, 以及植株再生培养基, 均参见本实验室配方并优化[19]。在共培养及选择、分化培养过程中, 均添加5 mg/L AgNO3。共培养后Timentin持续添加至再生苗移入盆钵前。
使用CTAB法提取植株叶片总DNA作为模板, PCR鉴定CAD、CCR基因目的片段。扩增目的片段上游引物在CaMV35S启动子上, 下游引物分别为cad-2和ccr-2, 产物为正向片段并包括部分启动子序列。预期扩增片段长度分别约为CAD 400 bp, CCR 300 bp。
CaMV35S启动子上的引物35S-1:GACGCACAATCCCACTATCCTTC。反应条件与1.2相同。
根据PCR鉴定结果, 选取PCR阳性植株和野生型植株, 采用紫外分光光度法测定其相对木质素含量[21]。取各独立的转基因植株全叶片, 置于50℃干燥过夜后研磨成粉末, 每株分成3份, 每份0.006 g, 分别放入10 mL离心管中, 加入25%溴乙酰-乙酸溶液 (w/w) 0.5 mL和高氯酸 0.02 mL, 盖紧管口, 于80℃恒温水浴 40 min, 每隔10 min振荡试管。将反应液完全移入已装有2 mol/L NaOH 1 mL和2.5 mL冰乙酸混合液的10 mL容量瓶内, 振荡, 充分混匀, 并用冰乙酸定容至10 mL。以冰乙酸为空白溶液, 用多功能读数仪(Varioskan Flash spectral scanning multimode reader, Thermo公司)在波长260 nm测定吸光度。利用260 nm处木质素的吸光度作为相对木质素含量。采用数据学软件SPSS 12进行统计学分析。
Lignin%=Abs× Liters× 100%/(Wsample× Astandard)[21]
式中, Abs为样品溶液木质素吸光度, Liters为样品溶液定容体积(L), Wsample为样品的绝干重量(g), Astandard为黑麦草木质素标准吸光率。根据公式可知, 木质素含量与其吸光度呈正相关。
以多年生黑麦草“ 雅晴” cDNA为模板扩增获得的目的片段, 经克隆测序, 结果表明, 片段长度与预期有差异。CAD片段, 预期长度是256 bp, 实际长度为367 bp, 与预期相差111 bp; CCR预期长度是194 bp, 实际长度为296 bp, 相差102 bp。均不包括添加的酶切位点。
通过DNAMAN(版本5.2.2)软件对测序结果与NCBI中的黑麦草CAD基因序列(登录号:AF472591.1)和CCR基因序列(登录号:AF278698.1)进行比对, 并分析结构, 结果表明获得的片段均包含一段内含子序列。内含子序列长度即是差异的长度, 分别为111和102 bp。去掉内含子, cDNA序列与NCBI数据库中目的基因片段序列同源性分别为92.19%和99.48%(图3和图4)。获得的CAD基因与NCBI中AF472591.1序列存在一定差异, 氨基酸序列比对分析, 同源性为87.06%。结果表明获得的片段为CAD和CCR基因片段。
 | 图3 CAD片段同源性分析 (102212为内含子)Fig.3 The sequence alignment of CAD fragment (102— 212 indicate the intron) |
获得的目的片段分别以正反方向插入到载体pSK-int质粒内含子两侧, 构建了重组中间载体pSK-iCAD和pSK-iCCR。用BamH I/Sac I分别双酶切pSK-iCAD和pSK-iCCR, 回收目的片段iCAD和iCCR, 分别插入相同酶切的p2355载体相应位点, 构建了含干扰片段的植物表达载体p23-iCAD和p23-iCCR。iCAD片段长909 bp(正向片段373 bp、内含子163 bp、反向片段373 bp, 其中包含酶切位点12 bp), iCCR片段为767 bp(正向片段302 bp、内含子163 bp、反向片段302 bp, 其中包含酶切位点12 bp), 由CaMV35S启动子驱动。
用BamH I/Sac I双酶切p23-iCAD和p23-iCCR分别得到909和767 bp长的目的片段(图5), 表明CAD和CCR基因正、反向目的片段已经插入到p2355质粒的相应位点, 植物表达载体p23-iCAD和p23-iCCR构建完成(图2)。
选择生长状态良好、质地致密均一的黑麦草愈伤组织(图6A)经过农杆菌浸染(图6B), 再通过3轮巴龙霉素共计6周筛选后(图6C), 进行分化(图6D)和生根培养 (图6E), 检测鉴定获得转基因植株(图6F)。
携p23-iCAD质粒农杆菌转化多年生黑麦草, 从约3 600个共培养的愈伤组织中, 获得65株正常生长的抗性植株, 138个未分化的抗性愈伤组织, 以及30株抗性白化苗。携p23-iCCR质粒农杆菌转化多年生黑麦草, 从约3 600个共培养的愈伤组织中, 获得78株正常生长的抗性植株, 145个未分化的抗性愈伤组织, 以及32株抗性白化苗。未分化的抗性愈伤组织和白化苗没有应用价值, 淘汰, 未进行后续研究。
观察显示, 转基因植株与野生型相比, 外观表型上没有明显差异, 生长正常(图6F)。
利用抗性植株叶片总DNA作为模板进行PCR验证, 由于CAD和CCR克隆片段分别比预期多出111和102 bp内含子序列, 因此扩增片段亦比预期分别长111和102 bp。扩增CAD 基因正向目的片段的引物为上游CaMV35S启动子引物55-1和cad-2, 片段长度约为500 bp(图7); 扩增CCR基因正向目的片段的引物为上游CaMV35S启动子引物355-1和ccr-2, 片段长度约为400 bp(图8)。
获得的干扰CAD基因的转基因株系命名为i-CAD, 干扰CCR基因的命名为i-CCR。
根据PCR验证结果, 分别对PCR阳性植株和野生型对照进行相对木质素含量测定。目前对i-CAD阳性和i-CCR阳性各测定了20个独立的转基因植株。提取叶片木质素, 在260 nm测定吸光度(图9)。由于木质素含量与吸光度呈正相关, 因此以野生型的吸光度作为对照, 转基因植株的吸光度与之相比较, 测定相对木质素含量。结果显示, 其中, i-CAD植株有11株、i-CCR植株有9株木质素含量明显降低。图9分别显示了9个木质素含量降低的植株。
与野生型对照相比, CAD干扰植株木质素含量降低了26.40%45.04%, 平均降低了33.86%; CCR干扰植株木质素含量降低了28.58%50.18%, 平均降低了34.67%。经过方差分析, CAD干扰植株和CCR干扰植株的相对木质素含量与野生型相比差异极显著(P< 0.01), 表明RNA干扰木质素合成途径中的CAD、CCR后, 转基因植株叶片总木质素含量明显降低。
观察表明, 木质素降低的转基因植株与对照相比, 外观形态上没有明显差异, 生长正常(图6F), 但是触摸感觉较柔软。
多年以来人们都是通过化学和生化角度来研究木质素潜在的合成途径, 而如今则更多的是利用经典的正向遗传筛选和有针对性的反向遗传学方法。目前在知道基因或者基因组序列的情况下, 反向遗传学技术更加广泛地应用在基因功能研究及新材料的创制中, 例如RNAi、反义抑制、插入突变体的表征分析等手段来进行研究[22]。其中, RNAi可以高效、特异性地使目的基因转录后沉默或抑制目标基因表达, 从而获得功能丧失性突变个体用于基因功能的研究, 这已成为研究基因功能及转基因育种的重要方法。在植物基因功能研究中, 利用含有目标基因正向和反向重复序列片段能形成发卡结构的RNA(hpRNA)来沉默内源基因, 是应用于转基因诱导基因沉默最高效的方法[23]。这种RNA干扰方法效率高、作用持久、可稳定遗传给子代[24]。
本研究中, 预期扩增的片段为cDNA序列, 但是结果获得的片段含有一段约100 bp的内含子。可能是提取的RNA中混有DNA, 因此扩增出了含有内含子的片段。通过对木质素含量的测定, 表明含有内含子的干扰片段没有影响对目的基因表达的沉默, 亦有可能参与了对目的基因的沉默作用。近年来的研究表明, 内含子也参与了基因的表达调控[25]。构建的载体正、反向片段中均包含目的基因内含子, 内含子片段在RNAi过程中也会配对形成双链互补的小分子RNA, 可能会对目标基因调控产生影响。获得的CAD基因片段的外显子与NCBI中参考的序列AF472591.1核苷酸序列同源性为92.19%, 差异相对较大, 氨基酸序列比对分析, 同源性为87.06%。推测获得的片段可能是CAD基因家族中1个基因的片段。由于植物木质素合成酶系存在多基因家族现象[26], 其中CAD是典型的以家族形式出现[27]。NCBI数据库中目前已公布了3个黑麦草CAD的cDNA序列(登录号:AF010290.1、AF472591.1、AF472592.1)和1个黑麦草CCR的cDNA序列(登录号:AF278698.1)。干扰该基因的表达, 在转基因植株中, 导致了木质素含量的显著降低。因此, 本研究获得的CAD片段可能是该家族中一个基因的片段。
由于黑麦草属于单子叶禾本科植物, 并非农杆菌的天然受体, 遗传转化较为困难, 愈伤组织再生频率低[28], 因此需要对受体材料和转化方法加以改进。有研究利用黑麦草幼苗分蘖处分生区诱导获得的愈伤组织作为受体获得了较高的遗传转化效率[29]。还有研究通过改进转化方法, 极大地提高了二穗短柄草(Brachypodium distachyon) [30]和假俭草(Eremochloa ophiuroides)[31]的转化效率。在此基础上, 并结合本实验室建立的方法, 再次优化了转化方法。在农杆菌侵染愈伤组织前, 还用细胞凋亡抑制剂CHO对愈伤组织进行预处理, 以减轻农杆菌侵染愈伤组织后对其造成的褐化坏死, 并在侵菌时加入非离子去污剂F68, 以利于农杆菌的附着和增加细胞膜的通透性。
黑麦草作为优良的牧草和草坪草在我国的种植和应用越来越广泛, 新材料的培育具有重要意义。降低黑麦草木质素含量, 有利于提高饲草的利用率和消化率。因此本研究应用RNAi技术分别抑制了多年生黑麦草木质素合成途径中的关键酶CCR和CAD, 以获得木质素降低的转基因黑麦草。结果显示, 通过导入干扰CCR和CAD基因的片段, 能获得木质素显著降低的转基因植株, 表明CCR、CAD在黑麦草木质素合成途径中起关键作用, 同时也表明可以通过RNAi技术培育低木质素含量的多年生黑麦草。获得的转基因植株生长发育正常, 未出现倒伏、褐化等异常, 表明利用RNAi技术适度抑制黑麦草木质素合成, 能够得到生长发育正常的转基因植株。本结果与Tu等[4]的研究报道相似。Tu等[4]RNAi下调CCR(与本研究不同的干扰片段)或COMT(咖啡酸-3-O-甲基转移酶)的转基因多年生黑麦草在温室和田间均表现出总木质素含量和G-lignin、S-lignin、H-lignin三种单体的含量同时降低, 但S/G没有明显下降, 这些木质素含量降低的转基因植株的消化品质得到改善并且未对生长发育产生明显不利影响。当木质素正常合成代谢途径受阻时, 可能有其他次生代谢物填充于木质素构架中, 使得植物体内的生理功能不受影响[32]。
本研究获得的转基因植株中, 约50%的植株总木质素含量显著降低, 其余的与对照相比, 未见明显降低。许多研究表明, 外源基因的导入, 常有表达发生沉默的现象[32]。而且木质素生物合成途径极其复杂, 受时间、空间和环境因素影响较大[32], 因此有部分转基因植株木质素含量没有变化。在进一步进行育种研究中, 需筛选木质素含量降低的植株为育种材料。
当木质素正常合成代谢途径受阻时, 会有其他次生代谢物产生[32]。一些研究显示, 降低木质素含量, 能增加转基因杨树[9]、柳枝稷[13]、玉米[14]等纤维素含量。最新研究发现, 在水稻(Oryza sativa)中转入拟南芥的一种转录因子SHINE (SHN), 使得木质素含量降低了45%, 组分也发生变化, 并且纤维素含量增加了34%, 但植株表型和强度却没有改变[34]。推测木质素含量降低, 可能产生一种补偿作用, 而使纤维素含量增加, 使植株仍然保持一定的强度。本研究获得的木质素含量降低的转基因多年生黑麦草, 是否会增加纤维素含量, 有待研究。
但是某些问题值得关注, 木质素能保护植株避免病原体入侵, 木质素降低可能会引起植株对病原菌的抗性降低[5]。我们获得的转基因低木质素含量的植株抗病能力是否改变, 有待进一步研究。
同时, 一些问题也需要进一步探讨, 例如在黑麦草转化株总木质素含量降低的同时, 木质素的组成结构是否也发生改变; 抑制木质素的合成是否会引起其他生理组成的变化; 转基因植株后代的表型是否正常; 如何进一步提高遗传转化效率等等。相信随着木质素生物代谢途径研究的不断深入和生物技术的发展, 人们能更好地对其加以利用, 以利于工农业的发展。
缩写:MS培养基: MS medium; Murashige and Skoog培养基: Murashige and Skoog medium; 2, 4-D:二氯苯氧乙酸 2, 4-dichlorophenoxyacetic acid; 6-BA:6-苄氨基嘌呤6-Benzylaminopurine; IAA:吲哚乙酸Indole-3-acetic acid; AS:乙酰丁香酮 Acetosyringone; Km:硫酸卡那霉素 Kanamycin; Rif:利福平Rifampin; Timentin:特美汀, 青霉素替卡西林钠-克拉维酸钾 Ticarcillin Disodium-Potassium Clavulanat。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|