作者简介:崔岩(1986-),女,蒙古族,内蒙古赤峰人,硕士。E-mail:cuiyan0405@126.com
利用稀释平板分离法从甘肃国营条山农场马铃薯连作田植株根围土样中分离到1株真菌菌株,经形态学特征、ITS序列分析将其鉴定为俄罗斯木霉(
A
马铃薯( Solanum tuberosum)是世界第四大粮食作物[ 1],也是重要的饲用作物。马铃薯的地上茎叶和地下块茎可以直接作为饲料使用,马铃薯加工过程中的薯皮、薯渣也大量用作饲料。
甘肃是马铃薯种植大省。近年来,随着对马铃薯需求的不断增加,种植面积持续扩大,马铃薯连作栽培在甘肃已很普遍。据报道,连作可导致作物生长发育不良、品质及产量下降、抗病能力降低[ 2]。已有研究结果显示,随着马铃薯连作年限的增加,马铃薯根际土壤中镰刀菌数量呈上升趋势[ 3]。由镰刀菌( Fusarium spp.)引起的干腐病和立枯丝核菌( Rhizoctonia solani)引起的黑痣病已成为甘肃马铃薯生产的主要问题[ 4, 5],其中干腐病由茄病镰刀菌( F. solani)和接骨木镰刀菌( F. sambucinum)等病原所致[ 4, 5, 6, 7, 8, 9],亟待研究解决。
利用有益微生物和微生物代谢产物是防治农作物病害的有效防治技术与方法[ 10]。微生物是土壤生态系统的重要组成部分[ 11, 12]。在农业生态系统中,耕作层及作物根围土壤中具有丰富的微生物类群,不乏一些有益微生物资源。木霉属( Trichoderma)真菌是土壤习居菌的主要成员,其中很多木霉菌种对土传病原真菌具有较强的拮抗作用,广泛应用于土传植物病害的生物防治中[ 10, 13]。土壤中的木霉还能促进植物生长和加速有机氯等农药的降解[ 13]。因此,木霉菌成为世界各国植物病害防治中应用最广泛的生防菌之一。
为发掘马铃薯连作田已有的木霉菌资源,获得对马铃薯干腐病和黑痣病等土传病害具有生防作用的木霉菌资源,我们从马铃薯连作田根际周围耕作层土壤中分离获得的一株木霉菌株,通过培养特性观察和形态学研究,结合rDNA-ITS 序列分析进行了鉴定,明确了该菌种对马铃薯干腐病菌和黑痣病菌的拮抗作用,为开发利用木霉菌资源和马铃薯土传病害的生物防治提供了依据。
2011年7月,从甘肃国营条山农场马铃薯连作试验田以五点取样法采集马铃薯植株周围0~20 cm耕作层土样,采集的土样混合均匀后装入无菌袋中并编号,带回实验室在-20℃冰箱中保存备用。
1.2.1 供试培养基
1/4马铃薯葡萄糖琼脂培养基(1/4PDA):马铃薯50 g、葡萄糖4.5 g、琼脂17 g、水1000 mL,倒平板前加入氯霉素0.01%,丙酸钠10 mmol/L;马铃薯葡萄糖琼脂培养基(PDA):马铃薯200 g、葡萄糖17 g、琼脂17 g、水1000 mL;水琼脂培养基(WA):琼脂17 g、水1000 mL;麦芽浸膏琼脂培养基(MA):麦芽浸粉30 g、大豆蛋白胨3 g、琼脂15 g、水1000 mL;马铃薯葡萄糖培养液(PDB):马铃薯200 g、葡萄糖16 g、水1000 mL。
1.2.2 木霉菌的分离、纯化与保存
在无菌条件下,采用稀释平板分离法进行木霉菌菌株的分离[ 14, 15]。取充分混匀的土样小样与无菌蒸馏水按照1∶19的比例加入无菌三角瓶中,振荡使土样与无菌水充分混匀,并将土壤悬浮液逐级稀释为10-1,10-2,10-3 g/mL的浓度。根据预试验结果,取10-3 g/mL浓度的土壤悬浮液0.5 mL注入1/4PDA培养基平板上,迅速推平,于25℃恒温培养。每个土样重复20个平板。培养5 d后,挑取菌落特征与木霉菌相似的菌落于PDA平板上纯化,获得编号为GAU1-X-2的一株菌株。将纯化后的菌株于WA培养基平板上保存备用。
1.3.1 培养性状观察
在无菌条件下,将活化后的GAU1-X-2木霉菌株在PDA平板活化后,用6 mm打孔器打成菌饼,分别接种于PDA培养基和MA培养基平板中央,重复3次。25℃恒温黑暗条件下培养,逐日观察待鉴定菌株在两种培养基平板中的菌落形态、气生菌丝状况、颜色变化、色素形成等,以48 h的菌落平均直径计算日生长速率。
1.3.2 显微形态观察
在菌落开始生长到菌落颜色出现明显变化期间,逐日挑取培养物制片,观察菌丝、分生孢子梗和瓶梗等形态学特征,参照有关资料对GAU1-X-2菌株进行形态学分类鉴定[ 16, 17, 18, 19]。
1.3.3 分子鉴定
DNA提取:将活化后的GAU1-X-2木霉菌株接种在PDB培养液中,25℃、120 r/min,振荡培养48~72 h,收集菌丝,用十六烷基三甲基溴化铵(CTAB)法提取木霉基因组DNA[ 20],通过1%的琼脂糖凝胶电泳检测DNA质量。
ITS-PCR扩增和测序分析:用转录延伸因子EF-1α基因的引物对EF1-728F、EF1-986R[ 21]进行PCR扩增,引物由上海生工合成。引物对序列为:EF1-728F (5-CATCGAGAAGTTCGAGAAGG-3')和EF1-986R (5-TACTTGAAG-GAACCCTTACC-3')。PCR反应包括:2×Master PCR Mix 25 μL,10 μmol/L的引物1 μL,模板DNA 1 μL,ddH2O加至50 μL。PCR扩增条件为:预变性94℃ 4 min;94℃变性30 s,55℃退火30 s,72℃延伸2 min,进行35个循环;72℃延伸10 min,4℃保存。PCR扩增产物于1%的琼脂糖凝胶电泳检测,用成像系统成像,并送上海生工公司测序。
序列同源性比较和聚类分析:将待测木霉菌株的测序结果与GenBank 核苷酸数据库中的序列进行检索比对(BLAST),利用DNAstar软件将待测菌株的序列与GenBank中比对后同源性不低于95%的登记菌株的序列进行多序列同源性分析,邻接法构建系统发育树。
1.4.1 供试品种及来源
选用5个马铃薯品种的块茎进行木霉菌株GAU1-X-2对马铃薯块茎致腐能力影响的研究。5个品种分别为费乌瑞它( Favorite)、陇薯3号、陇薯6号、青薯2号、青薯9号,其块茎均由甘肃条山农场提供。
1.4.2 接种及评价方法
以GAU1-X-2木霉菌株培养物接种不同马铃薯品种的块茎,以该菌株对马铃薯块茎有无致腐能力为依据评估GAU1-X-2木霉菌株对马铃薯块茎的影响。具体接种方法参考李金花等[ 4]的进行:将新鲜健康的5个马铃薯品种的块茎分别用清水冲洗,用75%的酒精擦拭其表面,消毒3 min后,从块茎表面从上往下切取一四面体,将在PDA上培养72 h的GAU1-X-2木霉菌株打成直径为6 mm的菌饼,置于切开的底部穴窝中,再盖上四面体块茎组织,以接种PDA培养基圆片为空白对照,每个马铃薯品种重复3个块茎。处理块茎置于25℃、相对湿度90%的恒温恒湿培养箱中培养,7 d后观察马铃薯块茎接种部位是否有腐烂出现。若接种菌株不能导致马铃薯块茎穴窝中出现腐烂,且与空白对照一致,则认为所接木霉菌株对马铃薯无致腐能力,视为对马铃薯安全;反之,若接种部位出现腐烂,则认为所接木霉菌株对马铃薯有致腐能力,为不安全。
1.5.1 供试靶标病原菌
供试靶标病原菌菌株4株,分别为1株茄病镰刀菌( F. solani,编号为FSI)菌株、1株接骨木镰刀菌( F. sambucinum,编号为FSM)菌株和2株立枯丝核菌( R. solani,编号为RS1和RS2)菌株,所有病菌菌株均分离于马铃薯干腐病与黑痣病块茎,其中菌株RS2由澳大利亚悉尼大学惠赠,其余3株由甘肃农业大学植物病理学实验室提供。
1.5.2 拮抗作用测定方法
采用对峙培养法进行。将PDA上培养4 d的GAU1-X-2木霉菌株和靶标病原菌分别用打孔器打成直径为6 mm的菌饼,将木霉菌菌饼和病原菌菌饼分别接种在新的PDA平板两侧,两菌饼相距4 cm,以只接病原菌不接木霉菌为对照。每处理重复5次。所有处理在25℃恒温培养5 d后,观察记录木霉菌和病原菌的菌落半径,计算拮抗系数[ 15, 22]。
拮抗系数=(对照靶标病原菌菌落半径-对峙培养的靶标病原菌菌落半径)/对照靶标病原菌菌落半径
根据纯培养菌落特性、分生孢子梗和瓶梗的形态学特征以及ITS序列,将菌株GAU1-X-2鉴定为俄罗斯木霉( T. rossicum),这是我国首次发现并报道该菌种,为我国新记录种[ 16, 17, 18, 19]。
2.1.1 培养特性及形态学特征描述
菌株GAU1-X-2在PDA培养基上可产生气生菌丝,菌落正面绒毛状至毡状,背面反面灰白色,在PDA平板的边缘能快速形成灰绿色至暗绿色产孢区;在MA培养基上常不产生气生菌丝,但也有能产生的,菌落正面绒毡状,背面反面暗黄色,后期在MA平板边缘形成颜色较浅的淡绿色产孢子区( 图1)。在25℃下,在MA 和PDA上的菌落日平均生长速度分别为21.0和24.0 mm/d。
分生孢子梗宽且直,初次分枝一般成对或者3个排列为轮枝状,再次分枝不规则;分枝末端着生瓶梗的细胞为短圆柱形或稍微膨大;瓶梗常在最后一次分枝上形成,很少单生,安瓿形,瓶梗排列紧密;分生孢子椭圆形至短圆柱形,两端圆;菌丝有融合现象( 图1)。根据菌株GAU1-X-2的培养特性和形态特征,确定其分类地位为半知菌亚门丝孢纲丝孢目粘孢菌类的木霉属真菌。
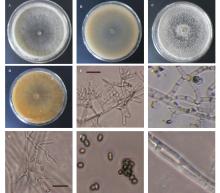 | 图1 菌株GAU1-X-2的菌落及形态特征Fig.1 Characteristics of the colony on media and the morphology of GAU1-X-2 isolate |
2.1.2 分子鉴定
用CTAB法提取的菌株GAU1-X-2的基因组DNA用1%琼脂糖凝胶电泳检测DNA 质量,得到比较单一的条带,电泳条带明亮,带型较宽,DNA 含量较高( 图2)。经PCR扩增后得到大小为300 bp左右的片段( 图3),由上海生工测序后菌株GAU1-X-2得到了大小为301 bp的碱基序列。
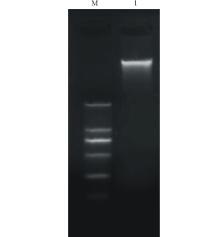 | 图2 菌株GAU1-X-2基因组DNA 凝胶电泳图Fig.2 The agarose gel electrophoresis of DNA of GAU1-X-2 M:分子量标准GM335 DNA Marker D;1: GAU1-X-2 基因组DNA Genomic DNA of GAU1-X-2. |
将测序得到的序列与GenBank核苷酸数据库中已有的木霉菌ITS 序列进行比对,菌株GAU1-X-2与GenBank上登录号为HQ342222( T. rossicum)、JN133575( T. rossicum)、HQ342224 ( T. barbatum)、AY937424( T. rossicum)的菌株同源性均达98%,与登录号为EU280062( T. rossicum)、EU280064( T. rossicum)、EU280066( T. rossicum)、AY937441( T. rossicum)的同源性达95%。
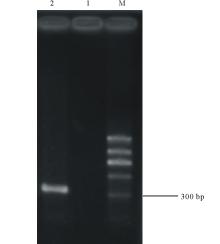 | 图3 菌株GAU1-X-2基因组DNA PCR扩增产物凝胶电泳检测图Fig.3 The agarose gel electrophoresis of PCR products of GAU1-X-2 M:分子量标准GM335 DNA Marker D;1:阴性对照Negative control; |
将以上GenBank 核苷酸数据库中的参比菌株和筛选到的菌株GAU1-X-2的序列用DNAStar软件绘制聚类分析图。结果表明,菌株GAU1-X-2与登录号为EU280062( T. rossicum)位于聚类图的同一分枝,聚为一类( 图4)。
综合GAU1-X-2木霉菌株的培养特性、形态学特征和分子鉴定结果,将马铃薯连作田土壤中获得的菌株GAU1-X-2鉴定为俄罗斯木霉( T. rossicum),为我国木霉新记录种。
将俄罗斯木霉菌株GAU1-X-2分别有伤接种5个马铃薯品种的块茎来检测该菌株对马铃薯块茎的致腐能力,结果显示:菌饼接种马铃薯块茎7 d后,接种GAU1-X-2菌株的块茎其接种部位与对照一致,没有出现因为致病而导致的腐烂和霉层形成,证明俄罗斯木霉菌株GAU1-X-2对马铃薯块茎无导致腐烂的能力,是安全的。
以俄罗斯木霉菌株GAU1-X-2为拮抗待测菌株,以分离于马铃薯干腐病与黑痣病块茎的1株茄病镰刀菌( F. solani)菌株、1株接骨木镰刀菌( F. sambucinum) 菌株和2株立枯丝核菌( R. solani)菌株为靶标病原菌,采用对峙培养法在PDA平板上培养,结果表明,俄罗斯木霉菌株GAU1-X-2对马铃薯镰刀菌干腐病的优势病菌茄病镰刀菌( F. solani)和接骨木镰刀菌( F. sambucinum)的拮抗系数为0.70,对2株马铃薯黑痣病菌立枯丝核菌( R. solani)的拮抗系数分别为0.71和0.77,说明俄罗斯木霉菌株GAU1-X-2对两种马铃薯病害的4株病原菌均有较好的拮抗作用。
2:GAU1-X-2基因组DNA扩增产物PCR products of GAU1-X-2.
木霉菌( Trichoderma spp.)为世界性分布。传统上,木霉被认为是一类典型的土壤真菌[ 23]。虽然个别木霉菌可以引起蘑菇污染和人类的病害[ 18],但大多木霉菌因其强大的生态竞争能力和对许多病原菌的抑制作用而被认为是有良好应用价值的生防菌,备受世界各国的广泛关注和研究,并作为生防因子用于防治多种作物病害[ 18, 23, 24]。我国幅员辽阔,地理气候和环境条件复杂多样,蕴藏着丰富的木霉菌生防资源,目前国内已报道的木霉种有25种[ 18]。
本研究在开展甘肃马铃薯连作田土壤中木霉菌资源调查的研究中,对获得的一株木霉菌株GAU1-X-2利用培养特性、形态特征和分子鉴定技术相结合将其鉴定为俄罗斯木霉( T. rossicum)。这是在我国首次分离到该菌种,为中国新记录种。该种属于木霉中的Pachybasium组、Clade Stromaticum进化枝,最早从俄罗斯的苹果园土壤中分离到,目前仅在个别国家有报道[ 19, 25]。
木霉菌传统的分类鉴定一般通过形态学来进行,但有些木霉种为介于已确定的种与种之间的中间类型,部分种之间在形态上又存在相似性,这给木霉的鉴定和分类带来很大困难。传统的分类学研究强调各分类单位在生殖结构上的分化特征和形态上的异同,当木霉菌物是无性个体时,种间的区分界限很难确定[ 17]。目前木霉的分类和鉴定工作主要是通过形态学特征和核酸序列分析相结合来进行[ 18]。
利用木霉菌对植物病害进行生物防治在国内外已有很多报道。本研究获得的俄罗斯木霉( T. rossicum)GAU1-X-2菌株系从马铃薯连作田土壤中分离得到,为确定其对马铃薯生产的安全性和生防价值,分别进行了GAU1-X-2菌株对马铃薯块茎的致病性测定和对来源于甘肃马铃薯镰刀菌干腐病的两种优势病原菌和黑痣病菌的拮抗试验,结果表明该菌株对马铃薯块茎无致害作用,证实俄罗斯木霉( T. rossicum)GAU1-X-2菌株对马铃薯安全;同时,菌株GAU1-X-2对靶标病原菌的拮抗作用明显,拮抗系数均较高,有很好的生防利用价值。查阅文献,发现有关于俄罗斯木霉( T. rossicum)对核盘菌( Sclerotinia sclerotiorum)引起的病害的防治作用的报道[ 26],但未见对接骨木镰刀菌( F. sambucinum)、茄病镰刀菌( F. solani)、立枯丝核菌( R. solani)的拮抗作用的研究报道。关于俄罗斯木霉( T. rossicum)GAU1-X-2菌株对靶标病原菌的拮抗机制及利用仍待进一步研究。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|


