作者简介:胡澍(1989-),女,陕西西安人,硕士。E-mail:hushumemory2008@126.com
通过野外取样,对黄土丘陵沟壑区坡沟系统5种立地环境(阳坡沟谷地和沟间地、峁顶、阴坡沟间地和沟谷地)下19种主要物种叶片的膜脂过氧化指标丙二醛(MDA)含量,3种抗氧化酶即超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性,及2种非酶抗氧化物质即还原型谷胱甘肽(GSH)和类胡萝卜素(Car)含量进行了测定与分析,旨在探讨不同物种适应不同立地环境的抗氧化特性。结果表明:各立地环境下物种间的MDA积累量均呈极显著差异( P<0.01),说明各立地环境的胁迫均导致供试物种遭受不同程度的膜脂过氧化作用,其中互生叶醉鱼草的膜脂过氧化水平最高,猪毛蒿的最低;在不同立地环境间,白羊草、达乌里胡枝子、阿尔泰狗娃花和狼牙刺的各抗氧化酶活性和非酶抗氧化物质含量均无显著差异( P>0.05),中华隐子草、糙隐子草、长芒草、草木樨状黄芪、糙叶黄芪、甘草、菊叶委陵菜、猪毛蒿、铁杆蒿、茭蒿、沙棘、杠柳和互生叶醉鱼草存在显著( P<0.05)或极显著( P<0.01)差异,说明在不同立地环境下,前者均采用多种抗氧化酶和非酶抗氧化物质协同抵御胁迫的策略,后者则调用不同抗氧化酶或非酶抗氧化物质发挥主要抵御作用;由于植物科属和碳同化途径的差异,其抗氧化特性也存在差异:菊科和豆科植物分别主要通过CAT和SOD减轻活性氧的伤害,禾本科植物则能以较高的SOD、POD活性和Car含量维持较低的膜脂过氧化水平,C4植物比C3植物具有较高的GSH和Car含量。隶属函数法综合评价表明,中华隐子草的抗氧化能力最强,互生叶醉鱼草的最弱。
This study investigated antioxidant properties of main plant species on 5 different site classes (sunny or shady gully and inter-gully land or hilltops)) in the hilly-gullied Loess Plateau. From field sampling, the activities of the antioxidant enzymes-superoxide dismutase (SOD), peroxidase (POD) and catalase (CAT), the contents of two non-enzymatic antioxidants-reduced glutathione (GSH) and carotenoid (Car), and the malondialdehyde (MDA) levels of leaf tissues of nineteen species were determined. There were highly significant differences in MDA accumulation among species on each site ( P<0.01). This indicated that the test species suffered varying degrees of membrane lipid peroxidation, with Buddleja alternifolia and Artemisia scoparia being highest and lowest respectively. There were significant differences in antioxidant enzyme activity or non-enzymatic antioxidant levels among sites for each test species, except for Bothriochloa ischcemum, Lespedeza davurica, Heteropappus altaicus and Sophora davidii, which suggests that these four species possessed upregulation of antioxidant enzymes and non-enzymatic antioxidant synthesis regardless of different site stresses, while Cleistogenes chinensis, Cleistogenes squarrosa, Stipa bungeana, Astragalus melilotoides, Astragalus scaberrimus, Glycyrrhiza uralensis, Potentilla tanacetifolia, A. scoparia, Artemisia vestita, Artemisia giraldii, Hippophae rhamnoides, Periploca sepium and B. alternifolia regulated their antioxidant enzymes or non-enzymatic antioxidant levels. From the botanical family perspective, antioxidant properties of the test species were distinct. CAT and SOD were respectively produced by five composite and five leguminous plant species to reduce damage from reactive oxygen species. Four graminaceous plants were able to attain high SOD, POD activities and Car contents to maintain a low level of membrane lipid peroxidation. Because of different carbon assimilation pathways, antioxidant properties of the test species were also distinct. In particular, C4 plants had higher GSH and Car contents than C3 plants. As assessed by a multivariate ‘subordinate function value’ method, the overall ranking for antioxidant capacity of the nineteen species was as follows: C. chinensis>C. squarrosa>A. melilotoides>S. davidii>A. scaberrimus>B. ischcemum>S. bungeana>L. davurica>P. tanacetifolia>H. altaicus>C. lancifolia>H. rhamnoides>P. sepium>G. uralensis>A. scoparia>D. indicum>A. vestita>A. giraldii>B. alternifolia.
黄土丘陵沟壑区光照强度大, 暴雨、径流集中, 黄土质地疏松, 养分流失严重, 加之人为破坏活动强烈, 对该区植物往往构成光照、水分和养分等生态因子的胁迫。因此, 选择抗性较强的物种对该区植被和生态修复具有重要意义。胁迫往往导致植物体内活性氧积累, 诱发或加快细胞膜脂过氧化作用[1], 破坏细胞膜结构与功能。然而, 植物在长期进化中形成了清除活性氧的防卫系统[2], 包括抗氧化酶与非酶抗氧化物质。若抗氧化酶的活性或非酶物质的含量较高, 能保持相对稳定甚至显著升高, 则可维持较低的膜脂过氧化水平, 减轻活性氧的伤害[3]。植物在胁迫条件下的膜脂过氧化反应和抗氧化系统的变化已广泛应用于植物对胁迫的反应机理研究, 并且具有重要的应用价值, 可为较强抗性的物种选择提供理论基础[4, 5]。目前, 研究植物自身抗氧化系统对生态因子胁迫的响应机制, 多采取某生态因子胁迫下的盆栽或试管控制试验[6, 7, 8], 然而在自然气候条件下, 各生态因子胁迫对植物抗氧化系统的影响不是孤立的, 而是综合的、相互联系的。因此, 本研究选择在黄土丘陵沟壑区沟坡的自然立地环境下进行取样, 探讨不同立地环境各生态因子综合胁迫下主要物种的抗氧化策略, 并综合评价其抗氧化能力, 为选择加快该区植被和生态修复的适宜物种提供抗氧化特性方面的依据。
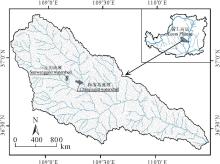
本研究选取了黄土丘陵沟壑区延河流域安塞县境内的2个小流域三王沟和陈家坬作为重复(图1)。研究区属温暖半干旱大陆性气候, 年平均气温8.8~10.2℃, 年日照时数2300~2400 h, 年平均降雨量520 mm左右, 6-9月降水量占年降水量的75%以上, 多以暴雨形式出现, 且局部雷暴雨发生频繁, 强度大[9]; 海拔1056~1443 m, 土壤类型以黄绵土为主; 天然草地、退耕草地、有林地和灌木林地共占流域面积的81%左右, 表现出森林草原带的基本特征。乔木主要为一些散生树种, 如小叶杨(Populus simonii)、榆树(Ulmus pumila)和杜梨(Pyrus betulifolia)等, 灌木多为森林带的一些优势种和次优势种, 如狼牙刺(Sophora davidii)、黄刺玫(Rosa xanthina)和紫丁香(Syringa oblata)等, 还有以铁杆蒿(Artemisia vestita)、茭蒿(Artemisia giraldii)、白羊草(Bothriochloa ischcemum)、长芒草(Stipa bungeana)和达乌里胡枝子(Lespedeza davurica)等优势种组成的草原植被[10]。
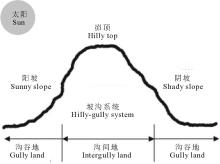
在所选小流域分别选取阳坡沟谷地、阳坡沟间地、峁顶、阴坡沟间地和阴坡沟谷地5种立地环境(图2), 每个小流域每种立地环境选取3个重复样地。
依据王力等[11]的土壤干层分级标准和全国第二次土壤普查养分分级标准[12], 由图3可知, 峁顶和阳坡土壤分别存在轻度和中度干层现象, 5种立地环境的土壤有机质和全氮均处于极缺乏状态。各立地环境由于地形和土壤侵蚀的差异, 造成光热和降水的再分配, 因而其光照、土壤水分和养分等生态因子也存在差异, 即光照在阳坡沟谷地强, 在阳坡沟间地和峁顶更强, 越过峁顶从阴坡沟间地到阴坡沟谷地逐渐变弱; 土壤含水量、有机质和全氮含量从阴坡沟谷地最高, 到阴坡沟间地越过峁顶到阳坡沟间地降到最低, 到阳坡沟谷地又呈升高趋势(图3)。 因此, 各生态因子对植物的综合胁迫程度应为阴坡沟谷地< 阴坡沟间地< 峁顶< 阳坡沟谷地< 阳坡沟间地。
通过对样地内出现的物种的重要值进行计算, 选择重要值较高的物种作为采集对象, 包括8科15属19种。于2012年7月25日-8月8日12:00-15:00, 即光强最大, 气温与土温最高时采集对环境变化最为敏感的植物营养器官— — 叶片[13], 并要求其生长良好无损伤, 禾本科植物采集从顶叶向下的第3或4片叶, 双子叶植物采集从顶上第1枝向下第4枝的枝中叶, 且每个物种在其样地均采集3个重复。采集后迅速放入液氮罐, 带回实验室于-80℃冰箱保存待测。
超氧化物歧化酶(SOD)是植物最重要的抗氧化酶之一, 能歧化分子氧活化的第一个中间物即超氧阴离子(
采用SPSS 16.0分别对各立地环境下不同物种间和各物种在不同立地环境间的指标值进行单因素方差分析, 再选用LSD作多重比较。
采用隶属函数法综合评价供试物种的抗氧化能力[24]。首先求出各指标在各物种中的隶属函数值, 即Xu, Xu=(X-Xmin)/(Xmax-Xmin), X为供试物种某一指标的测定值, Xmax、Xmin分别为所有供试物种中该指标的最大值和最小值, SOD、POD、CAT、GSH和Car指标均适用于此公式, 其隶属函数值大, 则其活性或含量较高; 若某一指标与抗氧化能力呈负相关, 则由反隶属函数计算其隶属函数值, 即Xu=1-(X-Xmin)/(Xmax-Xmin), MDA指标适用于此公式, 其隶属函数值大, 则其膜脂过氧化水平较低。然后求出各物种所有指标的平均隶属函数值, 以此来评定抗氧化能力的强弱。
各立地环境下不同物种间的MDA积累量均存在极显著差异(P< 0.01), 在阴坡沟谷地和阳坡沟间地, 均为茭蒿的MDA积累量最大, 在阴坡沟间地、峁顶和阳坡沟谷地, 均为互生叶醉鱼草的MDA积累量最大; 在阴坡沟谷地, 糙叶黄芪的MDA积累量最小, 在阴坡沟间地和阳坡沟谷地, 均为草木樨状黄芪的MDA积累量最小, 在峁顶和阳坡沟间地, 均为猪毛蒿的MDA积累量最小, 表明各立地环境的胁迫均导致供试物种遭受不同程度的膜脂过氧化作用。此外, 互生叶醉鱼草的MDA隶属函数值在所有供试物种中最小(表1), 因而它的膜脂过氧化水平最高, 而猪毛蒿的MDA隶属函数值最大, 膜脂过氧化水平最低。
| 表1 供试物种在不同立地环境下的MDA含量及其隶属函数值 Table 1 MDA contents (on different sites) of the test species and corresponding subordinate function values |
| 表2 供试物种在不同立地环境下的抗氧化酶活性和非酶抗氧化物质含量及其隶属函数值 Table 2 Antioxidant enzyme activities and non-enzymatic antioxidant contents (on different sites) of the test species and corresponding subordinate function values |
由表1还可知, 铁杆蒿、茭蒿、狼牙刺、白羊草、杠柳、阿尔泰狗娃花、长芒草和中华隐子草在不同立地环境间的MDA积累量差异均不显著(P> 0.05), 而其他供试物种(除披针叶苔草和野菊外)的呈显著(P< 0.05)或极显著(P< 0.01)差异。菊叶委陵菜的MDA积累量从阴坡沟谷地到峁顶降低幅度不大, 再到阳坡沟谷地呈显著升高的趋势(P< 0.05), 甘草的MDA积累量从阴坡沟间地到峁顶极显著地降低(P< 0.01), 越过峁顶到阳坡沟谷地再到阳坡沟间地又逐渐升高。而糙隐子草、草木樨状黄芪、互生叶醉鱼草和沙棘的MDA积累量从阴坡到峁顶极显著升高, 再到阳坡又极显著降低(P< 0.01)。
各立地环境下不同物种间的各抗氧化酶活性和非酶抗氧化物质含量差异基本上呈极显著水平(P< 0.01)。SOD活性在阴坡沟谷地、阴坡沟间地和阳坡沟谷地均为达乌里胡枝子最高, 茭蒿最低; POD活性在阴、阳坡均为糙叶黄芪最高, 而披针叶苔草、达乌里胡枝子、甘草、菊叶委陵菜和沙棘在不同立地环境的POD活性均很低, 近于0 μ g/(g FW· min); CAT活性在阴坡沟间地和峁顶均为互生叶醉鱼草最高; GSH含量在阴坡沟谷地、阴坡沟间地和阳坡沟谷地均为茭蒿最大, 长芒草最小; Car含量在峁顶和阳坡沟间地均为糙隐子草最大, 在阴坡沟间地和阳坡均为糙叶黄芪最小。
隶属函数值则表示各抗氧化酶或非酶抗氧化物质在不同立地环境的平均表现。由表2可知, 达乌里胡枝子的SOD隶属函数值相对于其他供试物种最大而茭蒿的最小, 糙叶黄芪的POD隶属函数值最大, 互生叶醉鱼草的CAT隶属函数值最大而糙隐子草的最小, 茭蒿的GSH隶属函数值最大而长芒草的最小, 糙隐子草的Car隶属函数值最大而野菊的最小; 4种禾本科和5种豆科植物的SOD隶属函数值均大于5种菊科和其他科植物, 4种禾本科植物的POD和Car隶属函数值也均高于5种菊科植物, 菊科植物阿尔泰狗娃花的CAT隶属函数值仅低于互生叶醉鱼草, 野菊、铁杆蒿和茭蒿的CAT隶属函数值也较高。从表2还可以发现, C4植物中华隐子草、糙隐子草和白羊草比C3植物长芒草、狼牙刺、披针叶苔草、沙棘、阿尔泰狗娃花和猪毛蒿具有较高的GSH和Car隶属函数值。总体来讲, 豆科植物的SOD活性较高, 菊科植物的CAT活性较高, 禾本科植物的SOD、POD活性和Car含量均较大, C4植物的GSH和Car含量均较大。
由表2还可知, 白羊草、达乌里胡枝子、阿尔泰狗娃花和狼牙刺, 它们的各抗氧化酶活性和非酶抗氧化物质含量在不同立地环境间的差异均不显著(P> 0.05), 而多数供试物种的存在显著(P< 0.05)或极显著(P< 0.01)差异。
所有供试物种中, 禾本科植物中华隐子草的平均隶属函数值最大, 表明其抗氧化能力最强, 禾本科植物糙隐子草、白羊草和长芒草及豆科植物草木樨状黄芪、糙叶黄芪、达乌里胡枝子和狼牙刺的平均隶属函数值较大, 抗氧化能力较强, 其次为蔷薇科植物菊叶委陵菜、菊科植物阿尔泰狗娃花、莎草科植物披针叶苔草、胡颓子科植物沙棘和萝藦科植物杠柳, 而豆科植物甘草及菊科植物猪毛蒿、野菊、铁杆蒿和茭蒿的平均隶属函数值较小, 表明其抗氧化能力较弱, 马钱科灌木互生叶醉鱼草的平均隶属函数值最小, 抗氧化能力最弱(图4)。这几种豆科植物(除甘草外)的抗氧化能力较强也间接地反映了该研究区贫瘠的土壤养分状况, 因为豆科植物具有固氮耐瘠的生物学特性。
茭蒿的MDA隶属函数值略高于互生叶醉鱼草, 膜脂过氧化水平很高, 究其原因可能是:茭蒿的生境以阳坡居多[25], 所以它的生境类型可能就决定了它会遭受高强度的生态因子的胁迫, 其相对其他供试物种最低的SOD隶属函数值和最高的GSH隶属函数值, 也可从侧面反映茭蒿的膜脂过氧化水平较高。狼牙刺和白羊草膜脂过氧化水平较高的原因也可能与茭蒿相似, 狼牙刺只在阳坡出现, 白羊草不在阴坡出现。相反, 野菊只在阴坡沟谷地出现, MDA隶属函数值较高, 且Car隶属函数值相对其他供试物种最低, GSH隶属函数值也只略高于长芒草, 说明野菊遭受该立地环境的胁迫本身就小, 尤其是光氧化胁迫, 因而膜脂过氧化水平不高, Car和GSH也就表现不活跃。有研究表明, 过度干旱(20%~30%)不利于甘草的生长[26], 那么根据图3中显示的各立地环境的土壤含水量, 表明本研究区甘草遭受的水分胁迫较大, 可能导致的膜脂过氧化作用就大。糙叶黄芪的膜脂过氧化水平高于草木樨状黄芪的原因可能是, 草木樨状黄芪的根深, 而糙叶黄芪横走的根状茎较浅[27], 所以糙叶黄芪可能对表层土壤水分条件较为敏感, 遭受水分胁迫的伤害也就大于草木樨状黄芪。
在不同立地环境间, 铁杆蒿、茭蒿、狼牙刺、白羊草、杠柳、阿尔泰狗娃花、长芒草和中华隐子草的MDA积累量均无显著差异, 但其内源保护酶和非酶物质的表现有所不同。对于铁杆蒿和茭蒿来讲, 其SOD活性很低, 无法起到第一道防线的作用, Car含量较小, 叶绿体膜受损也不能得到及时修复, 虽然CAT活性和GSH含量较高但POD活性较低, 清除H2O2有限, 因而MDA含量未能随立地环境胁迫的加剧明显降低, 且MDA对SOD活性有不可逆的抑制作用[28]。而狼牙刺和白羊草能保持较高且相对稳定的SOD、POD活性和Car含量, 使膜脂过氧化作用不再加剧。已有研究认为12.8%的贝壳沙含水量是杠柳SOD的耐受阈值[29], 那么本研究区不同立地环境的土壤含水量均接近或超过了该阀值, 所以杠柳SOD抑制膜脂过氧化的作用可能受到限制, 势必导致活性氧的爆发, 因而无法从实质上减轻膜脂过氧化作用。中华隐子草的Car含量较高且从阴坡沟间地到阳坡沟谷地再到阳坡沟间地稳定升高, POD隶属函数值较高, GSH隶属函数值也仅低于茭蒿; 阿尔泰狗娃花和长芒草的CAT隶属函数值仅低于互生叶醉鱼草, 活性也相对稳定; 长芒草还能保持较高且稳定的SOD和POD活性, 因此对膜脂过氧化发挥着较强且持续的抑制作用。
糙隐子草、草木樨状黄芪、互生叶醉鱼草和沙棘的MDA积累量随立地环境胁迫加剧表现出先升高后降低的极显著趋势, 说明从阴坡开始, 胁迫使细胞受损, MDA不断积累, 到海拔高、光照强、空气流速快的峁顶, 抗氧化酶与非酶物质的迅速增加或相对稳定有利于受损细胞的修复, 胁迫造成的损伤还未达到不可逆转的程度, MDA含量得以降低。即植物在经历了一定的、适度的胁迫, 将诱导体内产生一系列防卫性生理变化, 这些变化的共同结果限制了伤害的发展, 因而MDA含量有所降低[30]。还有学者研究表明, 活性氧对有机体的损伤机理主要与DNA损伤有关, 特别是mtDNA的过氧化损伤[31]。因此, 随着立地环境胁迫加剧, 植物内源保护酶活性与非酶物质含量的变化与MDA含量的增高可能是植物受损的原因, 其深层次的机理问题还需进一步研究。
在不同立地环境间, 白羊草、达乌里胡枝子、阿尔泰狗娃花和狼牙刺的各抗氧化酶活性和非酶抗氧化物质含量均无显著差异, 表明随着立地环境的变化, 其抗氧化酶活性和非酶抗氧化物质含量能保持相对稳定, 协同一致地抵御不同立地环境的胁迫。加之白羊草的SOD、POD、GSH和Car隶属函数值较高, 达乌里胡枝子的SOD、GSH和Car隶属函数值较高, 阿尔泰狗娃花的CAT隶属函数值较高, 以及狼牙刺SOD、POD和Car隶属函数值较高, 它们的这些抗氧化酶或非酶抗氧化物质在清除活性氧和抑制膜脂过氧化上发挥着主要作用。而多数供试物种的存在显著或极显著差异, 说明它们在不同立地环境采取的抗氧化策略不同。如糙隐子草的SOD活性和GSH含量在阴坡沟间地最大, 因而在阴坡沟间地就主要靠SOD清除活性氧源头
所测4种灌木间的抗氧化能力差异较大, 可能存在以下原因, 互生叶醉鱼草的抗氧化能力最弱, 一方面是由于其抗氧化系统的抑制作用不强, POD活性和GSH、Car含量从阴坡沟间地到峁顶再到阳坡沟谷地极显著地升高(P< 0.01), MDA含量虽在阳坡沟谷地得以极显著地降低(P< 0.01), 但相对于其他供试物种仍最高; 另一方面可能是它的叶片解剖特征[32]不利于其抗氧化系统抑制水分胁迫导致的活性氧积累。在阴坡沟间地, 杠柳的CAT活性远大于沙棘, 但前者到阳坡沟谷地极显著地降低(P< 0.01), 而后者到峁顶极显著地升高(P< 0.01), 在阳坡沟间地远超于前者; 两者的Car含量均显著下降(P< 0.05), 但沙棘的Car含量始终远大于杠柳。且沙棘相对于杠柳适宜的土壤含水量范围较大(11.9%~17.2%), 还具备较强的从土壤中吸取水分的能力[33], 所以其抗氧化系统受水分胁迫的影响较小。狼牙刺的耗水作用强烈, 用水深度约2.5 m, 且它只在阳坡出现, 接收的光照强度大, 即使水分、光照对狼牙刺构成较大的胁迫, 它也可有效地调控抗氧化系统抵御伤害, 并积极地通过不同的密度、物种组成及植被盖度来适应特定的水分条件[34], 从而表现出较强的抗氧化能力。
同科植物间由于种属差异, 也表现出不同的抗氧化能力。同为菊科植物, 阿尔泰狗娃花的MDA隶属函数值低于猪毛蒿, 但具有较高且稳定的SOD、POD和CAT活性及Car含量, 因而阿尔泰狗娃花具有较高的抗氧化能力。同为豆科植物, 草木樨状黄芪和糙叶黄芪在各立地环境下的POD活性均远大于达乌里胡枝子和甘草(P< 0.01), CAT活性也高于后两者。然而, 达乌里胡枝子的SOD隶属函数值相对于其他草本植物最高, 这与已有研究结果即SOD在达乌里胡枝子抗性机理形成方面发挥着主要作用[35]相符。而且从阴坡沟间地越过峁顶到阳坡沟谷地再到阳坡沟间地, 达乌里胡枝子的SOD活性一开始变化不显著(P> 0.05), 直到阳坡沟间地才明显降低, 而甘草的先降低后升高, 却始终低于前者, 所以草木樨状黄芪和糙叶黄芪的抗氧化能力最强, 其次为达乌里胡枝子, 甘草最弱。同为禾本科植物, 长芒草的GSH和Car含量均显著低于糙隐子草和白羊草(P< 0.05)。且在长芒草根系分布区土壤水分下降很快[36], 随着干旱的加剧, 长芒草的叶片组织含水量也明显降低, 而糙隐子草和白羊草能维持较高水平, 水分利用效率反而提高[37, 38]。因此, 糙隐子草和白羊草的这种水分利用特性更利于其抗氧化系统抵御水分胁迫, 使其较长芒草表现出更强的抗氧化能力。
披针叶苔草与野菊虽生长于同一生境(阴坡沟谷地), 却表现出不同的抗氧化能力。披针叶苔草的MDA隶属函数值低于野菊, 但具有较高的CAT活性和GSH、Car含量, 因而比野菊表现出较强的抗氧化能力。
关于该隶属函数法评价抗氧化能力的准确性, 与所选的物种与抗氧化指标体系都有关。相对于本研究, 王勇[39]研究的物种为铁杆蒿、茭蒿、猪毛蒿和黄花蒿(Artemisia annua), 测定的指标包括了MDA、SOD、POD、CAT、Car和抗坏血酸(Vc), 评价它们在干旱胁迫下的抗氧化能力为黄花蒿> 茭蒿> 猪毛蒿> 铁杆蒿, 与本研究结果不同。单长卷等[5]在评价白羊草、长芒草、冰草(Agropyron cristatum)和无芒隐子草(Cleistogenes songorica)在干旱胁迫下的抗氧化能力时, 还增加了脱氢抗坏血酸还原酶(DHAR)、单脱氢抗坏血酸还原酶(MDHAR)和谷胱甘肽还原酶(GR)等指标, 得出白羊草比长芒草具有更高的抗氧化能力, 却与本研究结果一致。目前, 本研究只涉及了抗氧化系统中最主要的抗氧化酶与非酶物质, 还应增测活性氧和参与抗坏血酸-谷胱甘肽循环的一些酶类指标, 并对供试物种各个细胞器的抗氧化酶和非酶物质进行比较性研究, 从而进一步揭示它们抗氧化特性的异同且提高评价抗氧化能力的准确性。
本研究中, 各立地环境的胁迫均导致供试物种遭受不同程度的膜脂过氧化作用。不同物种在不同立地环境胁迫下采取的抗氧化策略也不同:白羊草、达乌里胡枝子、阿尔泰狗娃花和狼牙刺采用多种抗氧化酶和非酶抗氧化物质协同抵御胁迫的策略; 而中华隐子草、糙隐子草、长芒草、草木樨状黄芪、糙叶黄芪、甘草、菊叶委陵菜、猪毛蒿、铁杆蒿、茭蒿、沙棘、杠柳和互生叶醉鱼草则调用不同抗氧化酶或非酶抗氧化物质发挥主要抵御作用。由于植物科属和碳同化途径的差异, 其抗氧化特性也存在差异:菊科和豆科植物分别主要通过CAT和SOD减轻活性氧的伤害, 禾本科植物则能以较高的SOD、POD活性和Car含量维持较低的膜脂过氧化水平, C4植物比C3植物具有较高的GSH和Car含量。
植物抗氧化能力的强弱主要取决于各生态因子的胁迫程度和植物的抗氧化特性。铁杆蒿、茭蒿和猪毛蒿作为该研究区的优势种, 抗氧化能力并不高, 这间接地反映了植物对环境的适应性是植物个体综合适应的结果[10], 抗氧化能力的强弱只是从侧面反映了它们与生境的关系。将供试物种的抗氧化特性与今后的光合特性、水分利用特性及形态解剖特征等研究结合, 可阐明它们适应该区不同立地环境的生理生态机制, 并综合评价其抵抗不同立地环境胁迫的能力, 这对选择适宜物种用于该区的植被和生态修复具有重要意义。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|