作者简介:韩宝贺(1988-),男,黑龙江大庆人,在读硕士。E-mail:A15904594049@163.com
以白三叶为试验材料,对其进行不同浓度Cd2+(0, 100, 200, 300, 400, 500 μmol/L)胁迫7 d,结果表明,随Cd2+浓度增加,白三叶各营养器官Cd积累量随之升高,各器官对Cd的富集能力表现为:根>叶>茎;同时,富集在叶片部分的Cd对白三叶叶片产生了毒害作用,使叶肉细胞的细胞壁着色加深,栅栏组织细胞以及海绵组织细胞的形状、大小及细胞排列的疏密程度发生改变。Cd2+胁迫后,白三叶叶片叶绿素含量显著降低( P<0.05),叶片的MDA含量呈上升趋势,且与Cd2+浓度之间存在剂量效应关系;整个胁迫过程中,SOD,POD和CAT活性则呈先升高后降低的趋势。相关性分析结果表明,Chl a和Chl b含量与Cd2+浓度间呈极显著负相关;MDA含量与Cd2+浓度间呈极显著正相关;SOD,POD,CAT之间呈极显著正相关,三者发挥协同作用以抵抗逆境毒害,体现了白三叶对重金属Cd的适应性。
Cadmium (Cd) toxicity was investigated in Trifolium repens using accumulation ability microstructure physiological. T. repens were treated with Cd2+(0, 100, 200, 300, 400, 500 μmol/L) for 7 days. Cd accumulation in different organs of T. repens gradually increased with the increase in the concentration of Cd. The accumulation content of different organs followed the sequence: roots>leaves>stems. Meanwhile, Cd accumulation in the leaves produced certain toxicity: cell walls of mesophyll cell stained deepening, the shape, size, and density were also changed. In response to Cd2+, more MDA and ROS contents were produced in leaves than untreated of T. repens. Compared with untreated, the photosynthetic pigments contents decreased significantly ( P<0.05). After Cd2+ treated, the content of MDA generally increased, and there is a dose-response relationship between the concentration of Cd. Throughout the process of stress, SOD, POD, CAT activity increased initially and then decreased. Correlation analysis showed that: the content of Chl a and Chl b were significantly negatively correlated with Cd2+ concentration. While the content of MDA was highly significant positively correlated with Cd2+ concentration. The activity of SOD, POD and CAT were highly significant positively among each other. Above three play synergistic role to reduce injury. These physiological indicators reflect T. repens adaptability to Cd2+ stress.
近年来, 随着经济和工农业生产的飞速发展, 工业“ 三废” 排放量日益增加, 农业生产中化肥和农药的过量喷施, 以及城市建设进程的进一步加快, 使得重金属污染愈加严重[1], 其中, 尤属镉土壤污染最为严重。镉(Cd)是生物生长发育的非必需元素, 具较高毒性且极易被吸收, 其本身具有高移动性和高毒害性, 极小浓度即可产生极大毒害, 被认定是危害最严重的重金属污染物[2]。我国受重金属Cd污染的草地及耕地面积超过2000万 hm2, 这不仅严重影响了作物的产量, 且进入土壤环境中的Cd离子, 一旦积累在植物的可食用部位, 便通过食物链影响到人类健康, 会导致神经和肾功能异常, 骨骼病变, 并能引发骨痛病、肺气肿、高血压等多种疾病, 因而重金属污染问题日益突出[3]。
白三叶(Trifolium repens)属于豆科(Leguminosae)车轴草属(Trifolium), 又称白花苜蓿, 白车轴草, 具有优良的牧草品质, 产量高, 生长适应性强, 过去多作为牧草栽培[4]。由于白三叶具有分枝多, 根系发达, 生物量大, 再生速度快, 适应性强, 成坪迅速等优点, 使其成为观赏型草坪和绿地建植的主要草种。最主要的是, 在实际应用中, 白三叶已经被证明在重金属污染土壤中具有良好的修复效果[5], 但当细胞内的重金属离子超过一定阈值时, 细胞结构便会产生一定的损伤。结构是功能的基础, 结构变化是植物一系列生理活动异常的细胞学基础[6], 因此, 研究植物受重金属毒害后, 细胞结构的变化, 以及Cd2+胁迫对白三叶生理生化的影响, 可以从细胞学上揭示重金属毒害白三叶的机理, 从生理学上阐述白三叶通过生理生化反应缓解Cd毒害的科学依据, 对于开展白三叶抗重金属耐性机制的研究具有应用价值。
目前, 关于白三叶的研究主要集中在抗逆性(盐碱胁迫、干旱胁迫、高温胁迫)、化感作用, 也有对其在植物修复中可能发挥的作用进行探讨[7, 8, 9]。Cd2+胁迫白三叶的研究更是处于对种子及幼苗的抗性进行研究的初级阶段[10], 系统地阐述白三叶对Cd富集能力以及Cd2+胁迫对白三叶显微结构及其生理特性的影响, 尚未见报道。本试验模拟不同浓度Cd2+对白三叶的胁迫, 通过测定白三叶地上部分和地下部分的Cd含量, 比较不同浓度Cd2+处理下, 白三叶对Cd的吸收能力和转运能力, 从而为白三叶富集Cd潜力的评价提供基础数据; 比较Cd2+胁迫下叶细胞显微结构的异同, 并研究了白三叶在Cd2+胁迫后的生理响应, 以期探讨白三叶抗Cd的耐性机制。
参照《牧草种子检验规程》GB/T2930.4-2001系列国家标准[11], 确定25℃为白三叶种子的适宜萌发温度, 恒温培养箱无光照条件下发芽。萌发后, 播种于培养钵(高20 cm、底径15 cm、口径20 cm)中, 基质为蛭石∶ 细砂=1∶ 1混合而成, 每盆15株, 共60盆, 用Hoagland完全营养液定时定量浇灌培养, 期间各项管理措施一致, 在温室中培养30 d, 待植物幼苗长出3片真叶, 进行Cd2+处理。试验于2013年10月至2014年3月进行。
1.2.1 试验设计 采用室内盆栽试验, 模拟Cd胁迫。Cd2+以溶液形式加入到培养钵中, 重金属离子浓度依据中华人民共和国国家土壤环境质量标准(GB15618-2008) 3级土壤环境标准量进行配制, Cd2+浓度梯度分别为100, 200, 300, 400, 500 μ mol/L, 每个梯度均采用Hoagland完全培养液配制而成, 同时设置对照处理, 对照组施以Hoagland完全培养液, 处理时间为7 d。
1.2.2 植物体含Cd量测定 重金属测定采用原子吸收光谱仪(Thermo-ICE3000), 采集待测白三叶的地下和地上(茎和叶)部分, 自来水冲洗以去除粘附于植物样品上的蛭石和细砂, 再用去离子水冲洗2~3次, 沥去水分, 在105℃下杀青30 min后于70℃烘箱中烘至恒重, 烘干后样品用陶瓷研钵研碎, 洁净密封保存。测定方法按照黄朝表等[12]及GB/T17141-1997方法测定[13], 同时配制空白试剂作为对比, 数据为3次重复的平均值。
1.2.3 叶片显微结构观察 采集待测白三叶的叶片, 用含70%酒精的FAA固定液固定, 固定时间均为24 h以上。然后根据Feder和 O’ Brien的方法[14], 将材料置于乙二醇甲基丙烯酸酯(GMA)中渗透3次, 前2次各为1 d, 第3次不少于5 d, 然后将装有材料和GMA的胶囊, 于60℃温箱聚合24 h, 用Leica Ultralcut R切片, 厚度为2~3 μ m。切片采用高碘酸-Schiff试剂/甲苯胺蓝(PAS/TBO)法染色[15], 烘干切片, 加拿大树脂封片。装片经Olympus BX53显微镜观察, Olympus DP26照相。
1.2.4 生理指标测定 待测生理指标的测定方法依次为:丙二醛(malondialdehyde, MDA)采用硫代巴比妥酸法测定[16], 超氧化物歧化酶(superoxide dismutase, SOD)活性采用NBT还原法测定[17], 过氧化物酶(peroxidase, POD)活性采用愈创木酚比色法测定[18], 过氧化氢酶(catalase, CAT)活性采用紫外吸收法测定[19]。各处理组的生理指标均重复测定3次。
所有数据用Excel 2003和SPSS 17.0软件制表和统计学分析。主要分析指标计算方法为:1)转运系数=植物地上部分元素的含量/地下部分同种元素含量。2)根系对重金属的滞留率(%)[20]=[(地下部分重金属含量-地上部重金属含量)/地下部分重金属含量]× 100。
从表1可见, 各器官(根、茎和叶部)对Cd的吸收能力有较大差别。总体而言, 同一浓度时, 各器官对Cd元素的富集量差异显著, 对Cd的富集能力表现为:根> 叶> 茎; 相同器官的Cd含量, 随着Cd2+浓度的增加, 呈先上升后趋于平稳的趋势。100 μ mol/L与对照组相比, 地下和地上部分的Cd富集含量均急剧增加, 增幅分别为123.8%和40.4%。当Cd2+浓度达到400 μ mol/L时, 地下和地上部分(指茎和叶部)Cd含量增幅减缓, 基本持平。本试验中, 白三叶地下和地上部分的Cd富集量均在500 μ mol/L时, 达到最大, 分别为3.490和0.910 mg/L, 地下部分吸收能力大于地上部分, 且不同Cd2+浓度之间Cd富集量差异显著(P< 0.05)。
| 表1 白三叶植株体对重金属的富集情况 Table 1 Cd content, translocation factor and root retention rate in T. repens |
转运系数(translocation factor, TF)表征植物将重金属由根部转移到地上部的能力, 可间接衡量植物对重金属的耐性[21]。由表1可知, 白三叶不同营养器官之间显示出了较大差别。本试验中, 胁迫浓度为100 μ mol/L时, TF最高(平均值为0.313), 表明此浓度时, 根部具有较强的Cd转移能力。胁迫浓度为200, 300, 400和500 μ mol/L的TF分别为0.202, 0.234, 0.262, 0.261, 差异不显著。
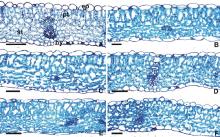
对照组白三叶叶片(图1A)的上、下表皮均由1层细胞组成, 上表皮细胞较大, 下表皮细胞较小, 细胞排列紧密。栅栏组织由单层长柱状细胞排列而成, 排列较为紧密。海绵组织细胞为圆形或椭圆形, 较稀疏。
白三叶在不同浓度Cd2+处理下, 上、下表皮细胞、栅栏组织细胞以及海绵组织细胞的形状、大小及排列紧密程度, 较对照组相比均出现了明显变化, 并且随着受Cd2+胁迫的时间延长、浓度越高, 栅栏组织和海绵组织变化会越明显。其中, 在较低浓度(100 μ mol/L)时, 白三叶叶片各结构未发生明显的变化(图1B); 从200 μ mol/L开始, 叶片结构变化明显(图1C)。在Cd2+供应水平达到200 μ mol/L时, 叶肉细胞的细胞壁着色加深, 这可能与Cd元素的积累有关, 此时, 叶肉细胞的结构仍较为清晰; 300 μ mol/L时叶肉细胞排列疏松, 栅栏组织长柱状细胞缩短变粗, 形态极不规则(图1D); 在高浓度Cd2+胁迫下(400和500 μ mol/L), 叶肉细胞发生收缩扭曲, 且细胞间隙明显变大, 尤其是海绵组织扭曲程度大, 厚度越来越小, 收缩严重(图1E, F)。
Cd2+胁迫后, 白三叶叶片的Chl a, Chl b和总叶绿素的含量逐渐降低(表2)。本试验中, 随着Cd2+浓度的升高, Chl a的含量下降显著, 各处理组的含量差异显著(P< 0.05), 在最高处理浓度500 μ mol/L处理下, Chl a含量降至0.814 mg/g, 为对照的73.93%。Chl b的含量在100~300 μ mol/L Cd2+胁迫下变化幅度较小, 较对照无显著差异, 其中在低Cd2+浓度(100, 200 μ mol/L)时, Chl b的含量略升高。400 μ mol/L时, Chl b的含量下降, 在500 μ mol/L时, 降至最低, 仅为对照的57.59%, 且Cd2+对叶绿素b的影响大于叶绿素a。总叶绿素的含量也呈下降趋势, 而Chl a/Chl b的变化却恰恰相反。在低Cd2+胁迫下, Chl a/Chl b较对照降低, 但随Cd2+浓度的升高, 其比值亦逐渐升高, 在500 μ mol/L达到2.951, 较对照组差异显著(P< 0.05)。
| 表2 Cd2+胁迫对白三叶叶片光合色素含量的影响 Table 2 Influence of Cd2+ stress on photosynthetic pigment content in T. repens leaves |
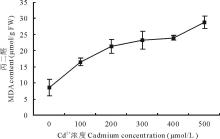
2.4.1 Cd2+胁迫对白三叶叶片MDA含量的影响 植物受到逆境胁迫时, 通常会发生膜脂过氧化作用, 而MDA是其最终分解的主要产物之一。MDA含量常用于评价植物体细胞膜的损伤程度, 含量越高, 说明植物细胞膜结构损伤越严重, 是一个重要的逆境生理指标[22]。由图2可知, 白三叶叶片的MDA含量呈上升趋势。经过不同浓度Cd2+胁迫7 d, 白三叶叶片的MDA含量变化相关方程为Y=3.5903X+7.8473(R2=0.9085), 由此可知, MDA含量变化与Cd2+浓度呈正相关。100 μ mol/L处理下, MDA含量为16.52 μ mol/g FW, 是对照的193.22%, 差异显著(P< 0.05)。200, 300, 400 μ mol/L处理下, MDA含量分别为21.35, 23.25, 23.99 μ mol/g FW, 较对照组差异显著(P< 0.05), 但三者间无显著差异。在500 μ mol/L处理下, 白三叶叶片的MDA含量达到28.82 μ mol/g FW, 较对照升高了337.08%, 与其余各处理组间差异显著(P< 0.05)。
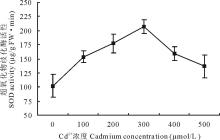
2.4.2 Cd2+胁迫对白三叶叶片SOD活性的影响 经过Cd2+胁迫7 d, 各试验组间的SOD活性, 随着胁迫浓度的升高, 呈先升高后降低的趋势(图3)。较对照组而言, 不同处理分别上升了150.28%, 173.68%, 202.16%, 156.21%, 133.77%, 且各试验组间SOD活性均显著高于对照组(P< 0.05)。100 μ mol/L胁迫7 d, 白三叶叶片SOD活性迅速升高, 在300 μ mol/L处理下, 其活性达到了206 μ g/(g FW· min), 在500 μ mol/L时, 降至136 μ g/(g FW· min), 但仍显著高于对照组(P< 0.05)。
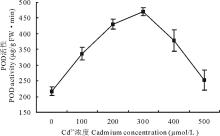
2.4.3 Cd2+胁迫对白三叶叶片POD活性的影响 从图4可知, 胁迫7 d后, 各试验组间POD活性发生了明显的变化, 整体的变化趋势为先上升后下降。从整个胁迫过程分析, 除500 μ mol/L处理外, 各组间活性均较对照组差异显著(P< 0.05)。低浓度Cd2+(100, 200 μ mol/L)胁迫, 即可使白三叶叶片POD活性急剧上升, 升高幅度为对照的155%和198%, 在300 μ mol/L处理下, POD活性达到470 μ g/(g FW· min), 为对照组的2.16倍, 此后, POD活性下降, 至500 μ mol/L时, 下降至252 μ g/(g FW· min), 仅为对照组的1.16倍, 与对照组活性差异不显著。
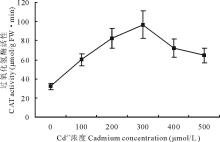
2.4.4 Cd2+胁迫对白三叶叶片CAT活性的影响 白三叶叶片的CAT活性在Cd2+胁迫后的变化趋势与SOD和POD一致, 即随着Cd2+胁迫浓度的增加, CAT活性先升高后降低(图5)。0~500 μ mol/L处理组的平均CAT活性分别为32.13, 60.11, 82.67, 96.67, 72.11, 64.44 μ mol/(g FW· min)。
2.4.5 Cd2+胁迫下, 白三叶各生理指标间的相关性分析 对Cd2+胁迫下, 各项生理指标的相关性进行分析(表3)。Chl a和Chl b含量与Cd2+浓度之间呈极显著负相关(P< 0.01), Chl a和Chl b含量间呈极显著正相关(P< 0.01); MDA含量与Cd2+浓度之间呈极显著正相关(P< 0.01), MDA含量与Chl a和Chl b含量之间呈极显著负相关(P< 0.01); MDA含量与SOD活性呈显著正相关(P< 0.05), 与CAT活性呈极显著正相关(P< 0.01); 而SOD, POD, CAT三者间呈极显著正相关(P< 0.01)。
| 表3 Cd2+浓度、叶绿素、膜脂过氧化指标以及抗氧化酶之间的相关性分析 Table 3 Correlation analysis among Cd2+ concentration, chlorophyll, MDA and antioxidant enzyme |
重金属累积能力是重金属污染土壤修复时植物种选择的一个重要指标[23]。目前, Cd超富集植物标准的认定, 广泛采用Tang等[24]提出的参考值(100 mg/kg)。白三叶已经被证明对Cd具有很强的富集力, 是一种Cd超富集植物[9], 但本研究所测白三叶的Cd富集量与之相距甚远。究其原因, 可能是胁迫时间短所致, 可进一步延长胁迫时间至30~60 d, 来进一步印证白三叶对Cd的富集能力。
Cd在白三叶体内的分布有2种情况, 一是积累在根部; 另一种是把根系吸收的重金属进一步运输到地上部, 并通过蒸腾作用或叶的脱落, 从植物体排出, 减少Cd对白三叶的毒害[25]。本试验表明, 白三叶对重金属Cd具有一定的累积作用, 且同一浓度时, 各器官对Cd的富集能力表现为:根> 叶> 茎, 根部TF为0.202~0.313。与王春光等[26]的同一树种不同器官内重金属富集量的结论一致, 所以, 在白三叶短期内受Cd胁迫的情况下, 根部滞留是白三叶积累Cd的主要方式, 其含量为1.238~3.490 mg/L, 滞留率最高可达83.13%; 而地上部分Cd积累量较低, 为0.404~0.910 mg/L。因而, 白三叶在短期Cd胁迫的条件下, 其防御措施可能是通过降低Cd向地上部分的迁移量, 来减轻过量Cd对地上部分其他各器官的毒害, 从而提高其Cd耐性, 与夏汉平和束文圣[20]关于香根草(Vetiveria zizanioides)和百喜草(Paspalum notatum)抗重金属的耐性分析是一致的。
值得一提的是, 适当处理浓度(100 μ mol/L)更有利于白三叶对Cd的吸收, 浓度过高则加重Cd对植物的毒害, 因影响其生理代谢, 从而影响植物根对重金属离子的吸收; 而处理浓度过低, 因没有达到植物对重金属吸收的要求, 植株体的重金属含量也不会达到最大[27], 所以才会出现在400, 500 μ mol/L时, Cd的富集量最多, 而二者的TF却低于100 μ mol/L。
随着胁迫的时间延长, 对白三叶的毒害日趋明显, 积累在叶片部分的Cd会使细胞结构产生一定的损伤[28, 29]。白三叶叶肉组织在低Cd2+条件下结构不受影响, 但随Cd2+浓度升高, 叶肉组织形态和排列发生改变。白三叶在高Cd2+胁迫下叶肉细胞排列疏松, 栅栏组织细胞收缩, 但海绵组织逐渐退化, 利于光合作用产生大量有机酸, 同时增加蒸腾作用使Cd大量运输到叶片与有机酸结合, 以提高植物对Cd积累能力, 这与前人关于重金属对植物形态的研究结果一致[30, 31, 32]。高Cd2+胁迫下叶片上表皮细胞发生扭曲变形, 可能是由于蒸腾作用使Cd在上表皮沉积较多, 从徐根娣等[33]的研究中得到证实, 这可能是白三叶适应Cd胁迫的一种机制。
3.3.1 Cd2+胁迫对叶片光合作用相关指标的影响 已有研究表明, 叶绿素含量会随重金属的胁迫而下降[34, 35]。本试验中, 随Cd2+浓度的升高, 白三叶叶片的Chl a, Chl b和总叶绿素的含量均降低。其原因可能是Cd2+胁迫通过干扰α -氨基-γ -酮戊二酸的合成和抑制叶绿素酸酯还原酶的活性, 使叶绿素的合成受阻[36, 37, 38]。而Cd2+胁迫对Chl a/Chl b的影响因植物种类的不同而异。例如:小麦(Triticum aestivum)叶片Chl a/Chl b随Cd2+升高而下降[39], 棉花(Gossypium hirsutum)则增大[40]。低Cd2+引起白三叶叶片的叶绿素b含量增加, 与金山等[41]对白三叶的研究一致, 但其机理有待于进一步研究。
3.3.2 Cd2+胁迫对叶片膜脂过氧化程度的影响 Bowler等[42]指出植物在逆境中, 打破活性氧的代谢平衡, 从而启动膜脂质过氧化作用或膜脱脂作用, 影响膜的功能。Abhay等[43], Ortega-Villasante等[44], 苏金为和王湘平[45], 李慧等[46]在对土人参(Talinum paniculatum)、紫花苜蓿(Medicago sativa)、茶树苗和草莓的研究中报道:Cd2+胁迫下, 植物体内MDA含量急剧增多。本试验中, MDA含量与Cd2+浓度间呈极显著正相关, 存在明显的剂量-效应关系。在低Cd2+胁迫下, 即已出现膜脂过氧化作用, 表明白三叶叶片细胞膜对Cd极为敏感, 且随着Cd2+浓度增加, 过氧化作用越来越明显。
3.3.3 Cd2+胁迫对叶片抗氧化物酶活力的影响 环境胁迫会造成植物体内活性氧的大量积累, 诱导一系列抗氧化反应[47, 48]。本试验中, SOD, POD, CAT三者呈极显著正相关, 低Cd2+胁迫下, 白三叶通过升高SOD, POD和CAT活性来防止活性氧造成的毒害, 说明三者发挥协同作用, 维持植物体内氧自由基动态平衡, 体现了白三叶对Cd的适应性; 但这种能力是有限度的, 在300 μ mol/L时, 白三叶叶片SOD, POD和CAT活性都急剧下降, 此时白三叶体内活性氧的形成和清除系统之间的平衡被打破。这与刘慧芹等[49]、赵梅等[50]、Weng等[51]关于逆境时植物能通过各抗氧化酶活性协调变化来缓解毒害的结果一致。
重金属对植物的毒害作用非常复杂, 其毒害效应与重金属种类、重金属浓度有关, 且不同植物也有差异, 甚至同一植物的不同器官对重金属胁迫的反应也存在差异。可以肯定的是, 植物受到重金属胁迫, 细胞结构及生理生化反应等都会受到影响, 它们之间相互联系和相互制约。今后, 可进一步对分子水平的机理进行研究, 如信号转导途径以及分子生物学, 充分了解重金属耐受植物的抗性机理。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|