作者简介:刘文瑜(1985-),女,甘肃兰州人,在读博士。E-mail:yu850721.lemon@163.com
本试验以蒺藜苜蓿种子为材料,预先用0.1,0.3和1.0 mmol/L 硝普钠(SNP, NO 供体)浸种,通过计算相关萌发指标,测定种子萌发过程中各项生理指标及抗氧化系统酶活性,研究外源NO对2.0% NaCl胁迫下蒺藜苜蓿种子萌发生理特性及活性氧代谢的影响。结果表明,0.1 mmol/L SNP能显著缓解盐胁迫对蒺藜苜蓿种子造成的伤害,使蒺藜苜蓿种子的发芽率、发芽势、发芽指数和活力指数分别提高了333.40%,79.64%,171.93%和100.00%;种子可溶性糖、可溶性蛋白和脯氨酸含量分别提高了21.1%,42.3%和123.1%,淀粉含量降低了17.7%,淀粉酶活性提高了29.7%,丙二醛(MDA)和超氧阴离子(
Medicago truncatula seeds were pre-soaked with 0.1, 0.3 and 1.0 mmol/L sodium nitriprusside [SNP, a nitric oxide (NO) donor] solution to study the effects of nitric oxide on seed germination, physiological characteristics and active oxygen metabolism of M. truncatula under 2.0% NaCl stress. Damage to M. truncatula seeds caused by 2.0% NaCl stress was significantly alleviated in the presence of 0.1 mmol/L SNP. The seed germination percentage, germination energy, germination index and vigor index were increased 333.40%,79.64%,171.93% and 100.00%, respectively; while soluble sugar, protein and proline contents in seeds were increased by 21.1%, 42.3% and 123.1%, respectively. Starch content was decreased by 17.7%, amylase activity was increased by 29.7%, and MDA and
土壤盐害已成为影响植物种子萌发、作物生长和产量的主要生物胁迫之一[1]。盐害可导致植物体内超氧阴离子、过氧化氢和羟基自由基的积累, 大量积累的活性氧引起脂质、蛋白质和核酸氧化进而造成细胞损伤[2]。植物则通过提高抗氧化系统酶活性, 减轻盐胁迫的伤害[3]。
一氧化氮(nitric oxide, NO)是广泛存在于植物体内的气体小分子信号物质。植物体内NO的合成主要依赖于一氧化氮合酶(NOS)和硝酸还原酶(NR)[4]。NO在植物体内是致毒还是起到保护作用取决于胞内环境、作用部位。一方面当胞内NO浓度高时, NO可作为一种自由基参与反应而破坏生物大分子的结构与功能, 对生物体产生氧化损伤; 另一方面当胞内活性氧浓度较低时, NO可中断活性氧链式反应, 对细胞起到保护作用[5]; 另外NO在植物生长发育过程中起到关键作用, 包括破除种子休眠[6]、植物体新陈代谢[7]、气孔运动[8]、光合作用[9]、呼吸作用[10]、成花生理[11]等; 在旱害、盐害、冷害以及病原菌侵染等逆境胁迫应答中也起着重要作用[12]。硝普钠(SNP)是现已广泛使用的外源NO供体, 0.5 mmol/L SNP可以释放约2.0 μ mol/L的NO[12]。研究发现, 低浓度的硝普钠(SNP)处理明显缓解盐胁迫下水稻 (Oryza sativa)幼苗根组织丙二醛(malondialdehyde, MDA)的积累, 显著提高可溶性蛋白含量, 并诱导根系抗坏血酸过氧化物酶(ascorbate, APX)、过氧化物酶(peroxidase, POD)和超氧化物歧化酶(superoxide dismutase, SOD)活性的上升, 而高浓度SNP处理效果则相反[13]; 外源NO能提高干旱胁迫下小麦(Triticum aestivum)幼苗叶片中SOD、POD和过氧化氢酶(catalase, CAT)活性, 降低超氧阴离子(
蒺藜状苜蓿(Medicago truncatula)为豆科苜蓿属一年生植物, 因其种子荚果螺旋紧密, 外被尖刺, 形似蒺藜, 因此称为蒺藜状苜蓿, 也称为截叶苜蓿或截形苜蓿。蒺藜状苜蓿原产地中海地区, 在澳大利亚南部许多较为干旱的地区种植蒺藜苜蓿已非常普遍, 我国主产区为河南、河北、山东、安徽、江苏、四川、山西、陕西等省[16]。由于蒺藜苜蓿与紫花苜蓿等豆科植物遗传关系近, 基因组小, 生长周期短, 有较高的生物多样性; 另外, 蒺藜苜蓿固氮效率高, 其次生代谢产物丰富, 因此, 在近年的比较基因组学研究中发挥着重要作用[17], 而有关蒺藜苜蓿耐盐机制尚未见报道; 同时, 由于近年来土壤盐渍化加剧, 提高蒺藜苜蓿耐盐性迫在眉睫。为此, 本文通过外源NO处理2.0% NaCl胁迫下蒺藜苜蓿种子, 对蒺藜苜蓿种子萌发及种子萌发过程中可溶性糖、可溶性蛋白、淀粉、脯氨酸、MDA含量、
试验以蒺藜苜蓿品种“ WM5106” 为材料。由扬州大学提供, 千粒重为3.086 g, 室温避光贮存备用。
本试验于2013年4-5月在甘肃农业大学生命科学技术学院植物生理实验室进行。挑选大小一致、饱满且无病虫害的种子, 用0.2%HgCl2溶液浸泡消毒5 min, 蒸馏水冲洗5~6次后, 分别做如下处理, 处理一:分别用不同浓度的NaCl (0, 0.2%, 0.5%, 1.0%, 1.5%, 2.0%)溶液处理; 处理二:分别用蒸馏水, 0.1, 0.3, 1.0 mmol/L SNP溶液浸泡48 h后, 用2.0% NaCl处理, 即CK、2.0% NaCl、0.1 mmol/L SNP+2.0% NaCl、0.3 mmol/L SNP+2.0% NaCl、1.0 mmol/L SNP+2.0% NaCl。将处理后的种子置于垫有双层滤纸的培养皿(φ =9 cm)中, 每皿50粒种子, 每个处理均重复3次。以蒸馏水为对照(CK), 每皿中分别加入8 mL对应的溶液, 将所有培养皿置于温度(25± 1)℃, 12 h光照/12 h黑暗、湿度80%恒温培养箱中, 培养7 d后统计幼苗相关萌发指标; 分别在对处理二(CK、2.0% NaCl、0.1 mmol/L SNP+2.0% NaCl、0.3 mmol/L SNP+2.0% NaCl、1.0 mmol/L SNP+2.0% NaCl)进行处理后的第0, 2, 4, 6天测定相关生理指标, 并做POD同工酶电泳。
1.2.1 种子发芽指标 萌发处理后以胚根长为种子长的2倍, 胚芽与种子等长作为萌发标准, 每天统计发芽的种子数后计算发芽率、发芽势、发芽指数和活力指数(发芽指数与种子平均鲜重的乘积再除以测试种子的数量)。计算公式如下:
发芽率(GP)=7 d发芽种子数/测试种子总数× 100%[18]
发芽势(GE)=前3 d发芽种子数/种子总数× 100%[18, 19]
发芽指数(GI)=∑ (Gt/Dt)[20]
式中, Dt为日发芽种子数, Gt为与Dt相应的每天的发芽种子数。
活力指数(VI)=GI× 第7天正常幼苗平均鲜重[21]
式中, 幼苗鲜重为称取5株幼苗的重量。
1.2.2 生理指标测定 可溶性糖采用蒽酮比色法测定[22]; 可溶性蛋白采用考马斯亮蓝比色法测定[23]; 脯氨酸采用酸性茚三酮法测定[24]; 淀粉采用蒽酮比色法测定[22]; 淀粉酶活性采用3, 5-二硝基水杨酸法测定[23]; 丙二醛(MDA)采用硫代巴比妥酸(TBA)比色法测定[24]; 超氧阴离子(
1.2.3 过氧化物同工酶分析 采用不连续系统聚丙烯酰胺凝胶垂直板电泳[32, 33]; 染色采用改良的联苯胺染色法[33, 34]。
每个指标测定重复3~5次。采用SPSS 17.0软件进行数据分析, 数据结果以“ 平均值± 标准误” 表示, 用Sigma Plot 12.5 作图。
蒺藜苜蓿种子采收当年种子硬实率较高, 达到70%~80%[35]。从表1 可知, 与对照相比, 随着NaCl浓度的升高, 蒺藜苜蓿种子的发芽率 (G)、发芽势 (GE)、发芽指数(GI)和活力指数 (VI)均呈现先上升后下降的变化趋势, 不同处理间差异显著(P< 0.05)。其中, 0.5%NaCl处理的蒺藜苜蓿种子的G、GE、GI和VI显著高于对照和其他处理, 分别比对照提高了100.04%, 257.51%, 28.52%和161.54%; 而2.0%NaCl处理的蒺藜苜蓿种子的G、GE、GI和VI最低, 分别比对照降低了78.57%, 49.85%, 65.77%和92.31%。
从表2 可知, 盐胁迫下蒺藜苜蓿种子的G、GE、GI和VI显著低于对照(CK)(P< 0.05), G、GE、GI和VI分别比CK降低了78.57%, 49.85%, 65.77%和92.31%。0.1和0.3 mmol/L SNP预处理显著提高了盐胁迫下蒺藜苜蓿种子的G、GE、GI和VI, 其中, 0.1 mmol/L SNP预处理后, 蒺藜苜蓿种子的G、GE、GI和VI比单独盐处理下提高了333.40%, 79.64%, 171.93%和100.00%; 1.0 mmol/L SNP预处理下蒺藜苜蓿种子的G和GI显著低于单独用盐处理, 且二者间GE和VI差异不显著。表明盐胁迫显著抑制了蒺藜苜蓿种子的萌发, 低浓度的SNP溶液可以明显促进盐胁迫下蒺藜苜蓿种子的萌发, 而高浓度的SNP溶液则起到抑制作用。
| 表1 不同浓度NaCl 对蒺藜苜蓿种子萌发的影响 Table 1 Effects of different concentrations of NaCl on seed germination of M. truncatula |
| 表2 外源NO对盐胁迫下蒺藜苜蓿种子萌发的影响 Table 2 Effects of exogenous nitric oxide on seed germination of M. truncatula under NaCl stress |
如图1A 所示, 盐胁迫下蒺藜苜蓿种子萌发过程中可溶性糖含量显著降低, 并且随发芽处理时间的延长呈现先上升后下降再上升的变化趋势, 在处理的第2、4、6天, 分别比CK降低了22.3%, 33.1%和27.0%。SNP预处理提高了盐胁迫下种子萌发过程中可溶性糖含量, 在第2天不同处理下可溶性糖含量达到最大值, 不同浓度SNP与盐一起处理的比单独用盐处理的分别提高了21.1%, 12.6%和5.9%。
如图1B所示, 对照和其他处理下蒺藜苜蓿种子萌发过程中可溶性蛋白含量随萌发时间的延长先升高后降低, 并在第2天达到最大值。与CK相比, 盐胁迫下种子萌发过程中可溶性蛋白含量显著下降, 在处理的第2~6天分别比CK降低了27.8%, 32.4%和41.1%。与2.0% NaCl处理相比, 在处理的第2~6天内, 不同浓度SNP预处理显著提高了盐胁迫下种子萌发过程中可溶性蛋白的含量, 其中0.1 mmol/L SNP预处理效果最佳, 比单独盐胁迫处理分别提高了42.3%, 20.0%和54.6%。
如图1C所示, 随着发芽时间的延长, 蒺藜苜蓿种子萌发过程中脯氨酸含量先上升后下降, 在处理的2~6 d内不同处理间差异显著。盐胁迫处理显著增加了种子萌发过程中脯氨酸含量, 并在第4天达到最大值, 比CK增加了19.4%, 而后缓慢下降, 在整个处理过程中都始终高于CK。与2.0% NaCl处理相比, 不同浓度SNP预处理显著提高了盐胁迫下种子萌发过程中脯氨酸含量, 在处理的第6天, 0.1, 0.3和1.0 mmol/L SNP预处理的种子内脯氨酸含量比单独用盐处理的分别提高了123.1%, 74.3%和52.0%。
外源NO对NaCl胁迫下蒺藜苜蓿种子淀粉含量和淀粉酶活性的影响见图2。从图2A中可以看出, 各处理下蒺藜苜蓿种子内淀粉含量随着发芽时间的延长呈现逐渐下降的变化趋势。在整个处理过程中, 用不同浓度SNP与盐一起处理的种子内淀粉含量始终高于CK, 但又均显著低于单独用盐处理; 在处理的第2天, 各处理组种子内淀粉含量差异不显著; 在处理的第4天, 各处理下蒺藜苜蓿种子内淀粉含量迅速下降, 在处理的第6天, 各处理下种子内淀粉含量仍持续下降并达到最低点; 其中, 0.1 mmol/L SNP与盐一起处理的种子内淀粉含量比单独用盐处理降低了17.7%。
 | 图2 外源NO 对盐胁迫下蒺藜苜蓿种子萌发过程中淀粉含量(A)和淀粉酶活性(B)的影响Fig.2 Effects of exogenous NO on the starch content(A) and amylase activity(B) in germinating M. truncatula seeds under NaCl stress |
如图2B所示, 随着发芽时间的延长, 蒺藜苜蓿种子内淀粉酶活性逐渐升高。种子萌发过程中, 用不同浓度SNP预处理的种子内淀粉酶活性始终显著高于单独用2%NaCl处理, 但又均显著低于CK。在处理的第6天, 用0.1, 0.3和1.0 mmol/L SNP预处理的种子内淀粉酶活性比单独用2%NaCl处理分别高29.7%, 19.1%和7.5%。说明用SNP浸种缓解了NaCl胁迫对蒺藜苜蓿种子内淀粉酶活性的抑制作用, 提高种子内淀粉酶活性, 从而促进淀粉的水解, 诱导种子的萌发。
由图3A 可知, 随着发芽时间的延长, 蒺藜苜蓿种子萌发过程中MDA 含量逐渐升高, 整个处理过程中, 各处理间差异显著。与CK相比, 盐胁迫下种子萌发过程中MDA 含量显著上升, 在第6天达到最大值, 比CK高84.4%。SNP预处理显著抑制了盐胁迫下种子萌发过程中MDA含量的增加, 在处理的第6天, 0.1, 0.3和1.0 mmol/L SNP与盐一起处理的比单独用盐处理的减少了21.8%, 18.2%和13.5%。
由图3B可知, 随着发芽时间的延长, 蒺藜苜蓿种子萌发过程中
以上结果说明盐胁迫促进了蒺藜苜蓿种子萌发过程中活性氧的积累, 而SNP预处理后显著缓解了盐胁迫对蒺藜苜蓿种子萌发造成的氧化损伤。
1) SOD 活性:外源NO对NaCl胁迫下蒺藜苜蓿种子萌发过程中SOD活性的变化如图4A所示。从图中可以看出, 随着发芽时间的延长, 各处理下种子内SOD活性呈现先升高后降低的变化趋势。种子萌发的过程中, 对照组种子内SOD活性变化较缓, 在第2天有小幅上升, 到第6天有小幅下降; 而种子在经过单一的NaCl处理后, SOD活性在第2天到第4天快速上升, 同时期经不同浓度SNP处理的种子内SOD活性也呈现迅速上升的变化趋势, 其中, 0.1 mmol/L SNP预处理下种子内SOD活性最高, 比单独用NaCl处理显著提高了90.8%, 即使到处理结束时, SOD活性虽有下降, 但是仍比单独用NaCl处理高43.9%。说明SNP预处理种子可以在一定程度上提高种子萌发过程中SOD活性。
2) POD活性:如图4B所示, 随着发芽时间的延长, 对照组(CK)和其他4种处理下蒺藜苜蓿种子内POD活性呈先升高后下降的变化趋势。在整个萌发过程中, CK种子内POD变化较为平缓。在第4天, 各处理下种子内POD活性快速上升, 各处理间差异显著(P< 0.05), 并达到最大值, 而且不同浓度SNP+2.0% NaCl处理种子内POD活性显著高于单独用2.0%NaCl处理, 其中, 以0.1 mmol/L SNP处理下种子内POD活性最高, 比单独使用2.0%NaCl处理高30.6%, 处理的第6天, 不同浓度SNP+2.0%NaCl处理的种子内POD活性呈现不同程度的下降, 但是仍显著高于单独用2.0%NaCl处理和CK。
3) CAT活性:图4C显示, 随着发芽时间的延长, 在正常条件下, 蒺藜苜蓿种子内CAT活性呈现相对稳定的变化趋势(P> 0.05); 而在整个处理过程中, 其他各处理下种子内CAT活性随着处理时间的延长呈现先升后降的变化趋势。其中, 在处理的第2天, 各处理间CAT活性差异不显著; 在第4天, 各处理的种子内CAT活性迅速上升并达到最大值, 而且不同浓度SNP+2.0%NaCl处理种子内CAT活性显著高于单独用2.0%NaCl处理, 其中, 以0.1 mmol/L SNP处理下种子内CAT活性最高, 比单独使用2.0%NaCl处理高123.9%, 处理的第6天, 不同浓度SNP+2.0%NaCl各处理下种子内CAT活性虽有不同程度下降, 但是仍显著高于单独用2.0%NaCl处理和CK。
 | 图4 外源NO 对盐胁迫下蒺藜苜蓿种子萌发过程中SOD(A)、POD(B)、CAT(C)及APX (D)活性的影响Fig.4 Effects of exogenous NO on the SOD (A), POD (B), CAT (C) and APX (D) activities in germinating M. truncatula seeds under NaCl stress |
4) APX 活性:图4D显示, 盐胁迫显著提高了蒺藜苜蓿种子萌发过程中APX的活性, 并且随着发芽时间的延长逐渐升高, 在第4天达到最大值, 比CK提高了71.1%, 以后缓慢下降, 整个处理过程中, CK中APX活性变化缓慢。与单独用盐处理相比, SNP与盐一起处理显著提高了种子萌发过程中APX的活性, 在处理的第6天, 0.1, 0.3和1.0 mmol/L SNP与盐一起处理比单独用盐处理的增加了60.3%, 51.5%和39.7%。
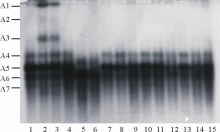
如图5所示, 共出现了7条酶带。其中, A5为共有酶带, 酶带宽且颜色深。CK的第4和6天出现了A1、A2和A3 3条酶带, 其中A1和A3酶带较宽且颜色较深, 但A2酶带颜色浅; 无论CK、盐胁迫或SNP与盐复合处理, 在整个处理过程中均出现了A4酶带, 但带较细且颜色浅; 盐胁迫下A6酶带颜色加深且带变宽, 而正常条件下A6酶带颜色较浅, SNP预处理的A6酶带颜色比CK深, 却比单独用盐处理的浅; 用CK或SNP预处理的种子萌发过程中出现了A7酶带, 但颜色较浅。
种子是植物为躲避恶劣环境以进行种群延续的一种重要机制[36], 种子萌发是植物生活史中的关键过渡阶段(从种子到幼苗)[37, 38]。种子发芽率、发芽势、发芽指数和活力指数均可以反映种子发芽能力。一般情况下, 发芽率与种子生活力是一致的, 因此在生产上通常将种子的发芽率作为鉴定种子质量的重要指标之一; 发芽指数反映了种子发芽的速率和整齐程度, 种子活力是种子在较广范围内迅速生长及生长整齐度的指标[39]。研究表明低浓度的盐胁迫对种子萌发和幼苗生长有促进作用, 高浓度则有抑制作用[40]。本试验结果表明用0.2%~1.0% NaCl处理蒺藜苜蓿种子后均可以提高种子发芽率, 其中以1.0%的处理最好, 而1.5%和2.0%NaCl浸种后种子的发芽率低于对照, 说明低浓度的NaCl可以促进蒺藜苜蓿种子萌发, 而高浓度NaCl对种子萌发起到抑制作用。
SNP是一种常用的外源NO供体。NO作为一种信号分子和活性氧清除剂, 能调节植物对生物和非生物胁迫的适应及反应[41]。汤绍虎等[41]研究发现0.1 mmol/L SNP可以显著促进渗透胁迫下黄瓜(Cucumis sativus)种子的萌发和幼苗生长; Kopyra[42]以外源NO 供体SNP处理羽扇豆(Lupinus luteus)种子, 有效提高了盐胁迫下种子的萌发率、萌发速率及胚根的长度。本试验结果表明, 0.1和0.3 mmol/L SNP预处理蒺藜苜蓿种子, 可以显著提高盐胁迫下种子的发芽率、发芽势、发芽指数和活力指数, 而1.0 mmol/L SNP预处理后种子的各项萌发指标反而低于单独用盐处理。说明低浓度的NO可以促进盐胁迫下蒺藜苜蓿种子的萌发, 而高浓度的NO对种子萌发起到抑制作用。
种子萌发过程中需要物质和能量来维持其旺盛的生命活动[43]。种子在萌发期间所需的养料和能量主要来自贮藏物质的转化和利用[44]。种子内主要的贮藏物质为淀粉、脂肪和蛋白质。这些物质在种子萌发过程中水解为简单的营养物质, 并运转到生长部位作为构成新组织的成分和产生能量的原料[45]。周万海等[46]研究表明盐胁迫下添加外源NO可以使甘农4号和阿尔冈金2个苜蓿品种淀粉酶活性显著提高, 淀粉含量降低, 可溶性糖含量升高; 郑春芳等[47]研究表明0.1 mmol/L SNP预处理能显著提高小麦叶片可溶性糖和可溶性蛋白含量。本试验结果表明盐胁迫显著降低了淀粉酶活性, 抑制了淀粉的水解, 抑制了可溶性糖和可溶性蛋白含量的增加; 而0.1和0.3 mmol/L SNP预处理后显著降低了种子内淀粉含量, 提高了淀粉酶活性, 增加了可溶性糖和可溶性蛋白含量。说明外源NO增强了盐胁迫下种子内淀粉酶活性, 促进了种子内淀粉的水解, 淀粉仅作为一种暂时的贮藏物质, 不断的水解为可溶性糖以满足种子萌发生长所需要的营养物质。
脯氨酸在植物渗透调节中起着重要作用, 可以清除活性氧, 提高抗氧化能力, 稳定生物大分子结构, 降低细胞酸性, 解除氨毒等[48, 49]。樊怀福等[48]研究表明0.01~0.40 mmol/L SNP 能显著缓解盐胁迫对黄瓜植株造成的伤害, 提高叶片脯氨酸含量, 其中以0.1 mmol/L SNP 缓解效果最好。本试验结果表明盐胁迫下蒺藜苜蓿种子萌发过程中脯氨酸含量显著上升, 不同浓度SNP预处理后促进了种子萌发过程中脯氨酸含量的积累, 其中以0.1 mmol/L SNP 促进效果最明显。说明外源NO预处理促进了盐胁迫下种子萌发过程中脯氨酸的积累, 从而缓解了盐胁迫对种子萌发造成的抑制作用。
植物种子萌发需要的物质与能量是由胚乳和糊粉层贮藏的营养物质分解和氧化磷酸化提供的, 能量代谢过程中会产生大量的活性氧, 从而对细胞和组织造成氧化损伤[50]。植物的保护酶体系在缓解胁迫方面起着重要作用, 它可以清除体内的活性氧, 以避免过量活性氧对植物的伤害[51]。SOD 作为膜保护的第一道防线, 能以
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [4] |
|
| [5] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [41] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [56] |
|
| [57] |
|
| [58] |
|