作者简介:王晓娟(1988-),女,四川南充人,在读硕士。E-mail:wangxiaoj12@126.com
以‘拉丁诺’白三叶为试材,采用药理学实验,探讨一氧化氮(NO)信号在外源亚精胺(Spd)诱导抗氧化酶活性及其基因表达中的作用。研究结果显示,20 μmol/L的外源Spd可显著提高白三叶叶片硝酸还原酶(NR)和一氧化氮合酶(NOS)活性,诱导白三叶离体叶片NO积累,并且具有时间效应,在处理第2 h达到最大值;50 μmol/L NO清除剂牛血红蛋白(Hb)、5 mmol/L 硝酸还原酶(NR)抑制剂偏钒酸钠(NaVO3)以及200 μmol/L一氧化氮合酶(NOS)抑制剂NG-硝基-L-精氨酸甲酯盐酸盐(L-NAME)处理均可不同程度地逆转Spd诱导的NO含量的升高。外源Spd亦可提高白三叶叶片超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)的活性及其基因的相对表达量,而Hb、NaVO3和L-NAME不同程度地抑制了Spd诱导的SOD、POD、CAT、APX酶活性及其基因表达。以上结果表明:Spd可能通过激活硝酸还原酶和一氧化氮合酶途径诱导产生NO,且NO信号参与了Spd调控白三叶叶片抗氧化酶活性及其基因表达。
A pharmacological experiment was designed to investigate the function of nitric oxide (NO) in the spermidine-induced antioxidant enzyme activities and gene expression in white clover (Ladino). Treatment with exogenous spermidine (Spd) at 20 μmol/L significantly improved ( P<0.05) the nitrate reductase (NR) and nitric oxide synthase (NOS) activities in leaves of white clover and NO content reached a maximum after 2 h of Spd treatment. However, treatments that included 50 μmol/L bovine hemoglobin (Hb) (NO-scavenger), 5 mmol/L partial sodium vanadate (NaVO3) (a NR-inhibitor) and 200 μmol/L NG-nitro-L-arginine methyl ester hydrochloride (L-NAME) (a NOS-inhibitor) inhibited the accumulation of NO in Spd-treated white clover. Exogenous Spd treatment can also enhance the activities of superoxide dismutase (SOD), peroxidase (POD), catalase (CAT) and ascorbic acid peroxidase (APX) and the relevant gene expression in leaves. Hb, NaVO3 and L-NAME inhibited the Spd-induced enzyme activities of SOD, POD, CAT, APX and gene expression to different degrees. These results suggest that Spd induced NO by enhancing antioxidant enzyme activities and expression of related genes in white clover, and that NO production is probably regulated from the NR and NOS pathways.
多胺(polyamines, PAs)为生物体代谢过程中产生的具有较高生物活性的物质, 是一类低分子量脂肪族含氮碱。高等植物中常见的多胺主要有腐胺(putrescine, Put)、尸胺(cadaverine, Cad)、精胺(spermine, Spm)和亚精胺(spermidine, Spd)等[1]。研究表明, 在逆境胁迫下, PAs能够诱导抗氧化酶基因的表达, 提高抗氧化酶活性, 调节体内活性氧(ROS)代谢平衡, 有效缓解氧化压力[2]。在番茄(Lycopersicon esculentum)、黄瓜(Cucumis sativus)的研究中发现, 外源Spd通过降低超氧阴离子(O2-)产生速率、过氧化氢(H2O2)与丙二醛(MDA)含量, 提高抗氧化酶活性以增强幼苗的抗渗透胁迫能力[3, 4]。PAs诱导烟草(Nicotiana tabacum)、冰叶日中花(Mesembryanthemum crystallinum)中超氧化物歧化酶(SOD)、过氧化物酶(POD)基因的表达, 以提高植物抗氧化保护[5, 6]。此外, PAs还具有保护生物大分子结构和生理功能、诱导可溶性渗透调节物积累并参与逆境胁迫信号传递等功能[2]。
一氧化氮(nitric oxide, NO)作为广泛存在于动植物和微生物中的信号分子, 在植物生长、发育及逆境胁迫中发挥重要作用。国内外众多研究表明NO在植物体内具有广泛的生理效应, NO参与植物呼吸作用、根和叶片的生长发育、种子萌发、气孔关闭、光形态建成、细胞程序性死亡、植物组织的成熟和衰老以及植物抗逆反应等[7, 8]。外源NO预处理可以提高干旱胁迫下植物叶片的保水性, 降低离子渗漏率, 诱导气孔关闭以及增加胚胎发育后期丰富蛋白编码基因的转录, 从而提高植物耐旱性[9]。植物体内NO的合成主要包括硝酸还原酶(NR)和一氧化氮合酶(NOS)途径, 及其他非酶促生成途径[8]。如水分胁迫可诱导玉米(Zea mays)叶肉细胞中NO积累, 而NR和NOS抑制剂均可抑制NO含量的升高[10]; 激动素(KT)和玉米素(ZT)通过激活NR和NOS活性, 促进NO产生, 从而延缓离体小麦(Triticum aestivum)叶片衰老过程中叶绿素和可溶性蛋白含量的降低, 抑制丙二醛(MDA)的积累[11]。
有关PAs诱导NO的产生, 在植物种子萌发、生长发育中已有相关报道。白旭等[12]的研究显示, 外源PAs尤其是Spd在促进莴苣(Lactuca sativa)种子早萌过程中可能与诱导NO的产生有关; PAs可促进拟南芥(Arabidopsis thaliana)幼苗组织释放NO[13]。我们实验室最新研究表明, 外源Spd可以提高白三叶抗氧化酶活性, 但是其作用机理目前还不清楚。NO信号是否参与Spd诱导抗氧化酶活性, NR和NOS作为植物体内合成NO的关键酶是否参与Spd诱导NO信号的产生, 以及Spd调控不同类型抗氧化酶基因的表达模式鲜有报道。本研究以白三叶(Trifolium repens)为材料, 采用NO清除剂牛血红蛋白(Hb)[11]、NR抑制剂偏钒酸钠(NaVO3)[14]以及NOS抑制剂NG-硝基-L-精氨酸甲酯盐酸盐(L-NAME)[11]结合亚精胺(Spd)处理离体叶片, 探讨外源Spd诱导白三叶叶片NO信号产生的途径, 以及诱导的NO在Spd激活抗氧化酶活性及其基因表达中的作用。以期为深入理解Spd参与调控植物抗氧化防御的生理和分子机制奠定基础。
供试材料白三叶品种为‘ 拉丁诺’ (Ladino), 种子购于成都绿草原种子有限公司。选择籽粒饱满大小一致的白三叶种子, 经0.1% HgCl2消毒3 min, 立即用蒸馏水冲洗数次, 均匀撒播在预先消毒的盛有石英砂的塑料育苗盆中, 置于光照培养箱中进行培育。培养条件为:光照昼夜温度23℃/19℃, 时长各为12 h, 相对湿度70%。发芽7 d后, 采用Hoagland全营养液培养幼苗, 每天更换营养液。待幼苗长至30 d(2片成熟叶片)时剪取叶色一致、嫩度相同、长势相当的白三叶叶片, 于蒸馏水中浸泡1 h以洗脱伤害, 然后进行各种处理。其中亚精胺(Spd)浓度为20 μ mol/L; 一氧化氮清除剂牛血红蛋白(Hb), 浓度为50 μ mol/L[11]; 硝酸还原酶抑制剂偏钒酸钠(NaVO3), 浓度为5 mmol/L[14]; 一氧化氮合酶抑制剂NG-硝基-L-精氨酸甲酯盐酸盐(L-NAME)浓度为200 μ mol/L[11]。
试验首先以CK(对照, 蒸馏水)和20 μ mol/L Spd溶液分别浸泡离体叶片1, 1.5, 2, 4, 6 h后取样, 测定样品中NO含量的变化, 筛选出NO含量测定的最佳时间点为处理的第2 h。在NO清除剂与NO合成酶的抑制剂效应中, 将离体叶片分别用各种抑制剂预处理2 h[14], 即将叶片分别用Hb、NaVO3和 L-NAME溶液浸泡2 h。
为了研究Spd 与NO清除剂和NO合成酶抑制剂对白三叶叶片NO含量以及抗氧化酶活性及其基因表达的影响, 试验设5个处理: 1)CK(对照, 蒸馏水); 2)Spd; 3)Spd+Hb(Hb浸泡叶片2 h后再转移到Spd溶液继续浸泡); 4)Spd+NaVO3(NaVO3浸泡叶片2 h后再转移到Spd溶液继续浸泡); 5)Spd+L-NAME(L-NAME浸泡叶片2 h后再转移到Spd溶液继续浸泡); 分别在处理后第2 h测定NO含量及抗氧化酶基因表达, 在处理后第8 h测定抗氧化酶活性。因植物细胞中NO合成的酶促途径主要包括NR和NOS两条途径, 所以在探讨Spd诱导NO合成的途径时, 试验分为两个部分。研究NR是否参与Spd诱导NO合成设4个处理:1)CK(对照); 2)NaVO3; 3)Spd; 4)Spd+NaVO3(材料处理方法同上); 处理2 h测定硝酸还原酶活性。研究NOS是否参与Spd诱导NO合成设4个处理, 1)CK(对照); 2)L-NAME; 3)Spd; 4)Spd+L-NAME(材料处理方法同上); 处理2 h测定一氧化氮合酶活性。上述处理均设4个重复, 置于温度23℃, 全光照的恒温培养箱条件下进行。
NO含量和NOS活性均采用试剂盒测定[15], 试剂盒购自南京建成生物工程研究所。取0.1 g处理过的叶片加0.9 mL 0.9% NaCl匀浆:12000 r/min离心10 min , 取上清沸水浴3 min; 12000 r/min离心5 min, 取上清用于NO含量检测。在550 nm波长下测定吸光度值, 考马斯亮兰法测定蛋白质含量, 计算每克蛋白含NO的量。取0.1 g处理过的叶片加0.9 mL 0.9% NaCl(含0.5 mmol/L 二硫苏糖醇DTT、1 mmol/L苯甲基磺酰氟PMSF)匀浆; 12000 r/min离心10 min, 取上清为NOS提取液。按照试剂盒说明考马斯亮兰法测定蛋白质含量, 在530 nm波长下测定吸光度值, 酶活性定义:每毫克组织蛋白每分钟生成1 nmol NO为1个活性单位。
NR活性采用试剂盒测定并有所改进[16], 试剂盒购自南京建成生物工程研究所。取0.1 g处理过的叶片加0.9 mL匀浆介质:4000 r/min 离心10 min, 取上清液待测。空白管, 标准管以及测定管按照试剂盒说明的步骤加样, 对照管稍加改进:0.2 mL上清液加入1 mL双蒸水37℃避光水浴准确反应30 min, 然后加1 mL显色剂, 混匀, 蒸馏水调0, 在540 nm、1 cm光径比色测定吸光度值。考马斯亮兰法测定蛋白质含量。酶活性定义:每毫克组织蛋白在37℃的条件下每分钟还原1 μ mol硝酸盐为亚硝酸盐为1个酶活性单位。
粗酶液的提取:取0.1 g处理过的叶片, 加0.9 mL 150 mmol/L pH值为7的磷酸缓冲液匀浆:4℃下15000 r/min离心20 min, 上清液即为粗酶提取液。超氧化物歧化酶(superoxide dismutase, SOD)活性采用核黄素-NBT法测定[17]。过氧化物酶(peroxidase, POD)和过氧化氢酶(catalase, CAT)参照Chance 和 Maehly[18]的方法并略有修改。POD 活性测定:反应体系中加入0.925 mL的HAc-NaAc(乙酸-醋酸)缓冲液, 再加入0.5 mL的愈创木酚和25 μ L的粗酶液, 混匀后加入50 μ L的H2O2启动反应, 在460 nm处测定吸光值, 每10 s记录1次吸光值, 共记录8次。CAT活性测定:反应体系中加入0.95 mL的PBS, 再加入0.5 mL的H2O2(混匀), 最后加入0.05 mL的粗酶液, 充分混匀后在240 nm处测定吸光值, 每10 s记录1次吸光值, 共记录8次。抗坏血酸过氧化物酶(ascorbate peroxidase, APX)活性参照Nakano和Asada[19]的方法进行测定。可溶性蛋白含量采用考马斯亮蓝法测定[20]。
采用qRT-PCR 的方法分析白三叶叶片中的抗氧化酶的转录水平。白三叶叶片总RNA提取参照捷倍斯公司试剂盒(Plant RNA Kit)说明书, 提取的总RNA参照美国Bio-Rad Laboratories公司反转录试剂盒(iScriptTM cDNA Synthesis Kit)说明书进行反转录获得cDNA第一链。以白三叶肌动蛋白基因(β -Actin)为内参, 根据白三叶POD基因, GenBank中已知的红三叶(T. pratense)SOD基因、蚕豆(Vicia faba)CAT基因和蒺藜苜蓿(Medicago truncatula)APX基因序列设计引物, 引物设计如表1。以获得的cDNA第一链为模板进行qRT-PCR扩增。 qRT-PCR在Bio-Rad公司的iQ Multicolor 实时定量PCR检测系统中进行。β -Actin、Cu/Zn SOD、CAT和POD基因反应程序为:94℃ 3 min; 94℃ 30 s, 57℃ 30 s, 72℃ 1 min, 30个循环; 72℃ 5 min。APX基因反应程序为:94℃ 3 min; 94℃ 30 s, 62.5℃ 30 s, 72℃ 1 min, 30个循环; 72℃ 5 min。
| 表1 试验中所用到的引物 Table 1 All primers used in this experiment |
采用Excel 2003进行绘图与数据处理; SAS 8.0软件进行方差分析和显著性检验(P< 0.05)。基因表达分析均以对照为参照进行相对表达比较。
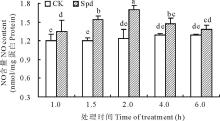
如图1所示, 在一定时间范围内, 以蒸馏水浸泡(CK)的白三叶叶片中NO含量均无显著变化, 而20 μ mol/L Spd处理的白三叶叶片NO含量呈先增加后减少的趋势, 且在处理后第2 h达到最大值。在不同时间点Spd处理的白三叶叶片NO含量均高于对照, 大部分达到显著, 表明Spd能够诱导叶片NO合成。据此, 在探讨NO的产生途径时, 以处理后2 h为NO含量测试时间点。
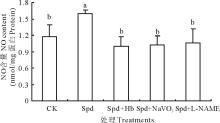
为了进一步探讨Spd诱导NO产生的途径, 观测了NO清除剂及合成抑制剂对NO含量的影响。与CK比较, Spd处理明显提高了白三叶叶片内源NO含量, NO清除剂Hb处理, NO含量则降低了60.64%。同样, NR抑制剂NaVO3和NOS抑制剂L-NAME处理, NO含量亦显著降低。由此可见, Hb、NaVO3和L-NAME可显著抑制Spd引起的白三叶叶片NO的产生, 推测NR和NOS均参与了Spd诱导NO的合成(图2)。
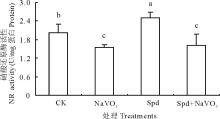
由图3可看出, NR抑制剂NaVO3处理使NR活性比对照降低31.38%, 证明NaVO3可抑制叶片NR活性。与CK相比Spd处理使白三叶叶片NR活性提高了23.95%, 达到显著水平, 表明Spd能够有效激活NR活性。Spd+NaVO3处理NR活性较NaVO3单独处理有所提高, 表明NaVO3可抑制叶片NR活性而Spd能够部分恢复NR活性。
由图4可看出, NOS抑制剂L-NAME处理使NOS活性比对照降低了53.87%, 证明L-NAME可抑制叶片NOS活性。Spd处理的白三叶叶片NOS活性比CK提高了27.07%, 达到显著水平, 表明Spd亦能有效激活NOS活性。Spd+L-NAME处理较单独L-NAME处理显著提高, 表明L-NAME可抑制叶片NOS活性而Spd能够完全恢复NOS活性。
外源Spd诱导白三叶叶片抗氧化酶活性如图5所示。外源Spd处理的白三叶叶片的SOD(图5A)、CAT(图5C)、APX(图5D)3种抗氧化酶活性显著高于CK, 提高幅度分别为36.66%, 49.63%和24.21%, 而Hb、NaVO3和L-NAME可显著抑制Spd引起的3种抗氧化酶活性的增加。与CK相比, Spd亦明显提高了POD活性(图5B), 但未达显著水平, 同样Hb、NaVO3和L-NAME使POD活性恢复到CK水平。以上表明, Spd提高白三叶叶片抗氧化酶活性需要NO的参与。
qRT-PCR分析结果表明, Spd处理使白三叶叶片Cu/Zn SOD、POD、CAT和APX 四种抗氧化酶基因的相对表达量比CK分别上调了62.56%, 60.62%, 85.19%和80.35%, 均达到显著水平。而Hb、NaVO3和L-NAME皆明显下调了由Spd引起的Cu/Zn SOD、POD、CAT和APX四种抗氧化酶基因的相对表达量(图6)。由此可以推测, NO参与了Spd调控白三叶叶片抗氧化酶基因的表达。
2006年Tun等[13]首次报道了PAs在拟南介幼苗中诱导合成NO, 同时通过巴西松(Araucaria angustifolia)的悬浮培养, 发现PAs中的Put能够诱导胚细胞产生NO[21], PAs预处理亦可诱导干旱胁迫下黄瓜幼苗产生NO[22]。本试验的结果显示, 外源Spd能够诱导白三叶离体叶片NO产量升高, 并且具有时间效应, 在第2 h达到最大值, 而Hb、NaVO3和L-NAME明显阻止由Spd诱导的NO含量的升高, 可以推测NR和NOS途径均参与了NO的产生。同时, 外源Spd处理的白三叶叶片, 其NOS和NR活性显著增强, 而NaVO3和L-NAME具有显著的抑制作用, 表明外源Spd可能通过激活NR和NOS代谢, 进而促成NO的大量产生, 而Spd能否诱导NR和NOS基因表达, 有关深入机制有待进一步研究。
植物在遭受非生物胁迫的过程中ROS积累增多, 清除自由基的相关酶活性降低, 使植物体内ROS代谢平衡被破坏[23]。Spd提高逆境胁迫下抗氧化酶活性, 有效清除活性氧, 从而减轻氧化压力已有较多报道。外源Spd通过提高大豆(Glycine max)幼苗抗氧化酶活性以延缓大豆叶片叶绿素、蛋白质的降解速度[24], PAs通过介导抗氧化系统降低超氧阴离子(O2-)产生速率, 从而增强水稻(Oryza sativa)植株耐盐性[25] 。盐胁迫下, 外源Spd和Spm通过上调粗齿冷水花(Ulva fasciata)中FeSOD基因表达, 以提高抗氧化保护[26], 我们已有研究表明, 外源Spd能够提高干旱胁迫下白三叶抗氧化酶活性, 延缓O2-、H2O2积累, 减轻膜脂过氧化(论文发表中)。在本试验中, 外源Spd亦可以提高正常条件下白三叶叶片抗氧化酶活性, 并且上调相应抗氧化酶基因的表达, 从而进一步探索了Spd在抗氧化保护中可能存在的分子机制。
在本研究中, Hb、NaVO3和L-NAME除显著抑制Spd诱导白三叶NO产生外, 同时也明显降低由Spd提高的抗氧化酶活性, 并下调相应抗氧酶基因的表达。结合其他相关报道, 外源NO能够显著诱导盐胁迫下紫花苜蓿(Medicago sativa)叶片SOD、POD和CAT活性提高[27], 内源NO亦能影响CAT 和SOD基因的转录水平[28], 我们可以推测, NO参与了Spd调控白三叶抗氧化酶活性及相关基因的表达。
综上所述, 外源Spd可以提高正常水分条件下白三叶离体叶片抗氧化酶活性及其基因表达, 提高白三叶叶片NR和NOS活性, 诱导NO信号产生。所以推测外源Spd通过激活NR和NOS途径诱导产生NO, 且NO信号参与了Spd调控白三叶叶片抗氧化酶活性及其基因表达。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [1] |
|
| [3] |
|
| [4] |
|
| [7] |
|
| [8] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [15] |
|
| [16] |
|
| [20] |
|
| [24] |
|
| [25] |
|
| [27] |
|