作者简介:孙云波(1985-),女,吉林临江人,在读硕士。E-mail: syb_0229@163.com
采用去除果荚浸种、不去除果荚浸种荚和焖种荚等方法对红芪种子预处理12 h后再行发芽试验,以不去果荚不浸种干种荚为对照,旨在探寻改善红芪种子发芽特性的种子预处理方法。结果表明,春播季节20℃/18℃自然光照条件下,各处理红芪种子发芽率随发芽天数的动态变化均呈“S型”变化趋势,符合Logistic曲线方程。红芪种荚从置发芽床后第2~6天开始,种子先后启动发芽,第14~19天发芽陆续结束。整个发芽过程中,种子各发芽指标均表现出预处理间的显著差异性,预处理使红芪种子发芽提早1~4 d,发芽高峰持续期延长2 d。去果荚浸种12 h显著加快了种子发芽进程,焖种荚处理有效延长了发芽持续期。各处理发芽指标从高到低依次为去果荚浸种12 h(发芽率80.7%,发芽势54.0%,发芽指数7.083)>不去果荚焖种荚12 h(发芽率64.0%,发芽势13.3%,发芽指数3.462)>不去果荚水浸种荚12 h(发芽率48.0%,发芽势22.0%,发芽指数3.007)>对照干种荚(发芽率34.7%,发芽势4.0%,发芽指数1.865)。以上说明种荚果皮造成的吸水障碍是限制红芪种子发芽的主要因素,播种前将红芪种荚浸种12 h或焖种12 h再行播种均可显著改善红芪种子发芽特性,去除果荚后再浸种效果更佳,发芽率可达80.0%以上。
Plant pod seeds of Hedysarum polybotrys were used in a germination test in order to explore the effect of seed pre-treatment methods. Several methods, such as soaking the peeled seeds, and soaking and stewing the unpeeled seed pods for 12 h, were compared with non-soaked, dry seed pods as a control. Results under natural illumination at 18-20℃ showed that germination dynamics in all pre-treatments followed S curve patterns that fitted to a logistic equation. Germination started days 2-6 and finished days 14-19. The pre-treatments showed significant differences in germination traits. The peeled and soaking pre-treatment and the soaking and stewed unpeeled-seed pods pre-treatment delayed peak germination by two days. The peeled and soaking pre-treatment significantly expedited germination while the unpeeled and stewing pre-treatment prolonged germination duration. All the pre-treatments for 12 h significantly improved germination quality compared with the control. The control had a germination rate of 34.7%, germination power 4.0% and germination index 1.865. The results for the peeled and soaked seeds were 80.7%, 54.0% and 7.083 respectively, that for the unpeeled stewed seed pods 64.0%, 13.3% and 3.462 respectively. The results thus show that pre-treating seeds by soaking or stewing can significantly improve germination quality. Improvements were highest in the peeled pre-treatment, where seeds showed over 80% germination rate.
红芪(radix hedysari)为豆科植物多序岩黄芪(Hedysarum polybotrys)的干燥根。春、秋二季采挖, 除去须根和根头, 晒干[1]。红芪味甘、微温。归肺、脾经, 具有固表止汗、生津养血等功效。用于中气下陷、表虚自汗等病症[1]。红芪与黄芪(astragali radix)同科异属[2], 两者在种荚形态上差异性较大, 红芪种荚荚果在单粒种子处缢缩呈串珠形扁葫芦状, 成熟饱满种子黑褐色, 种子与荚果皮结合紧密, 难以脱粒, 而黄芪荚果不缢缩, 种子成熟后种荚易开裂散出种子。
过去, 红芪药材主要来源于野生品, 但随着以红芪为原料的保健品和中成药的研发, 野生红芪远不能满足药材市场的需求, 人工栽培红芪受到关注, 现已形成以甘肃省陇南市武都区米仓山、安化镇一带为中心的红芪道地产区, 生产的红芪药材质量优异, 2011年获国家农产品地理标志登记产品保护[3]。红芪主要以种子播种育苗栽培为主, 生产上一般整荚播种, 由于荚果内果皮与种子连在一起, 荚膜包藏着种子, 果荚硬质, 种皮又厚, 吸水吸胀时间长, 种子在萌发过程中易烂种, 发芽率很低, 严重影响红芪规范化育苗成效。尽管对红芪种子发芽特性相关研究也有少量报道, 研究揭示成熟风干后的红芪种子具有明显的硬实和休眠特性[4, 5, 6, 7], 种子发芽期间对水分要求高, 浸种30 h以上才能达到饱和吸水状态[5], 土壤水分是影响红芪种子发芽和出苗的一个主要因素, 当土壤含水量低于9.0%时, 红芪种子不能发芽。采用使红芪种子外果皮受损的方法对促进种子发芽出苗有显著效果[6]。水浸种也可提高红芪种子发芽率[7], 鲜种子秋播红芪种子发芽率也较高[4], 说明红芪种子在成熟后风干过程中果荚和种皮加厚硬化是造成种子吸水吸胀困难的主要原因, 适宜的种子预处理可改善红芪种子的发芽特性, 提高种子发芽率。由于红芪种子一般在9月中下旬陆续成熟, 鲜种荚的果荚和种皮较嫩软, 水分易进入, 播种后发芽率虽高, 但出苗后由于有效积温低, 越冬前生长量小, 幼苗抗冻性差, 越冬返青率低, 规范化育苗成效差。因此, 探寻提高风干红芪种子发芽率的种荚预处理方法具有重要意义, 可为红芪GAP(good agricultural production)基地建设中确立播前种子预处理操作技术规程提供科学依据。
发芽试验用红芪种子为2011年9月中旬从甘肃红芪主产区陇南市农户生产田随机划分60个样点采集的红芪种荚, 经甘肃农业大学中草药栽培与鉴定系陈垣教授鉴定确认属多序岩黄芪的种荚。首先剔除杂质、瘪种和虫食种荚后手工混合均匀, 然后装入网袋挂凉在实验室靠阳通风处, 待种子自然阴干后保存于4℃冰箱中备用于发芽试验。
种子预处理试验采用单因素试验方案, 预处理因素有4个水平, 即去果荚浸种12 h, 不去果荚浸种荚12 h, 不去果荚焖种荚12 h, 以不去果荚不浸种的种荚为对照(以下去果荚简称去荚)。具体操作方法是首先用剪刀将上述备用于发芽试验的串珠种荚分成单粒荚, 随机数取大小和饱满度基本一致的带荚种子600粒, 用0.1%氯化汞对种荚表面消毒3 min, 然后用清水冲洗4次, 随机分为4组, 每组150粒, 分别置4个经灭菌并已编号的烧杯(直径9.6 cm)内, 于2012年4月29日20:00随机分别实施上述4个处理。其中, 去果荚处理中事先磨搓去除果荚, 挑选完整种子150粒, 其余处理均不去除果荚。焖种荚处理是将150粒种荚置烧杯后加水摇匀后用湿润砂子包埋杯口。同时选择规格一致的12个培养皿(直径9.6 cm)高压灭菌后备用于发芽试验。
红芪种荚经上述方法预处理后种子发芽试验在甘肃省中药材规范化生产技术创新重点实验室(原中草药栽培与鉴定实验室)20℃/18℃自然光照条件下进行。发芽试验于2012年4月30日开始, 5月20日结束。即种子经上述方法预处理结束后, 立即依次用蒸馏水冲洗3次, 将各组150粒种子依次摆放在已灭菌对应编号的3个培养皿(重复3次), 每皿50粒种子, 种子床由2层组成, 下层为脱脂棉(厚2 mm), 上层为滤纸。为了保证试验过程中的唯一差异性原则, 提高试验的精确性, 发芽试验采用随机区组设计, 3次重复, 根据实验室试验台光照条件差异划分为3个区组, 每区组摆放4个处理培养皿, 共摆放12个培养皿。加水时沿培养皿边缘加经灭菌冷却后的自来水, 以倾斜培养皿无水渗出为度, 记录加水量, 其他培养皿加水量和方法均一致。在皿底部和盖外均标记处理号及重复号, 将50粒种子均匀摆放在培养皿内。发芽过程中每隔12 h换水1次, 以胚根突破种皮1 mm左右作为种子发芽的标准, 每天早晨8:00观察记载发芽种子数, 最后计算发芽率、发芽势和发芽指数[8, 9]。
发芽率(germination rate, %)=终发芽种子数/供试种子总数× 100
发芽势(germination power, %)=发芽高峰期种子的发芽数/供试种子总数× 100
发芽指数(germination index, GI)=∑ (Gt/Dt)
式中, Gt为第t天的发芽种子数, Dt为对应的发芽天数。
图1显示出经不同方法预处理后种子发芽率随发芽持续时间的动态变化过程。各处理中, 红芪种子发芽率的动态变化过程均呈“ S型” 曲线变化趋势(图1a)。从种子置发芽床后第2~6天内各处理种子逐渐启动发芽, 随着发芽天数的延长, 发芽率均显著提高并达到最大值, 但整个发芽过程均表现出处理间的显著差异性。在发芽第6天开始, 各处理种子发芽率和每天发芽种子数均已达到显著差异性水平(F=7.143, P< 0.05), 直到发芽全部结束。在整个种子发芽过程中, 去荚浸种12 h后种子发芽率始终处于最高水平, 不处理对照种子的发芽率始终处于最低水平, 不去荚焖种12 h和不去荚浸种12 h后种子的发芽率介于两者之间。
图1b还显示, 对照不处理干种荚置发芽床后在第6天3个重复百粒种子平均仅有1粒发芽, 而种子经去荚浸种、不去荚浸种和不去荚焖种荚12 h后分别已有16, 14和7粒种子发芽。显然, 与对照相比较, 预处理显著促进了红芪种子的发芽进程(图1)。其中, 对照种子从第6天开始发芽, 第17天发芽结束, 发芽持续期为12 d; 去荚浸种12 h后种子从第2天开始发芽, 第13天发芽结束, 发芽持续期为12 d; 不去荚浸种和不去荚焖种12 h后种子均从第6天开始发芽, 但前者第14天发芽结束, 发芽持续期为9 d, 后者第18天发芽结束, 发芽持续期为13 d。各处理发芽持续期最大相差4 d。在整个种子发芽过程中, 预处理明显提早了种子发芽高峰期, 经焖种处理的种子发芽持续期明显延长。
 | 图1 种荚预处理12 h后红芪种子发芽率(a)和每天百粒种子发芽种子数(b)的动态变化过程Fig.1 Dynamics of seed germination rate (a) and the germinated seeds every day (b) in 100-seeds after pod pretreated for 12 h |
| 表1 种荚预处理后红芪种子发芽率随发芽天数的变化动态拟合Logistic方程的参数估计 Table 1 Parameter estimation based on Logistic equation fitting the dynamics of seed germination rate for H. polybotrys following pod pretreated with the germination days |
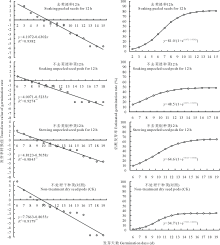
对4种方法预处理种荚后红芪种子发芽率随发芽持续天数的变化动态拟合Logistic曲线方程, 方程参数估计的各发芽参数列于表1, 直线化拟合结果和方程估测的发芽率变化轨迹见图2。显然, 对照和经种荚预处理后的红芪种子发芽率随发芽持续天数的变化动态均符合Logistic曲线方程, 方程拟合指数均达到极显著水平(P< 0.01)(图2)。方程估测的发芽参数(表1)与实际发芽过程(图1)基本相符合。根据“ S” 型曲线的变化情况, 大致可将红芪种子发芽进程分为3个时期, 即种子萌动期、发芽高峰期和发芽缓增期。各处理发芽最大速率, 即每天发芽种子数最大相差8~9粒。 利用方程参数估测的各处理发芽高峰起始范围为种子置床后第4~8天, 发芽终期范围为种子置床后第14~19天, 发芽持续期范围为种子置床后13~18 d。种子预处理使种子发芽进程提早1~5 d进入发芽高峰期, 发芽高峰持续时间延长, 不处理对照干种荚种子发芽高峰持续时间仅3 d, 而去荚浸种、不去荚焖种荚和不去荚浸种荚12 h后种子发芽高峰持续时间均较对照延长2 d(表1)。不去荚种荚经焖种处理12 h后置湿润的发芽床发芽, 发芽持续期最长, 而去荚浸种12 h后发芽持续时间最短, 发芽最为集中。显然, 浸种处理使最大发芽速率到达时间提早, 去荚后浸种效应更大。在不去荚处理中, 发芽初期焖种荚处理和浸种荚处理12 h后发芽率差异性不显著, 浸种处理的发芽率稍高于焖种处理的水平, 但随着发芽持续天数的延长, 趋势发生转化, 焖种处理12 h后的种子发芽率在发芽后第9天赶上浸种处理的水平并逐渐高出, 至发芽终期焖种处理显著高于浸种处理的水平(P< 0.05)。焖种荚处理12 h还较浸种荚处理12 h发芽持续期延长2 d左右, 两者均较对照持续期延长1~3 d, 这与实际发芽过程(图1)相吻合。各处理对红芪种子发芽进程的促进作用依次为去荚浸种12 h> 不去荚浸种荚12 h> 不去荚焖种荚12 h> 不去荚不浸种干种荚(对照)。
不同方法预处理后, 红芪种子发芽率随发芽持续天数配合Logistic方程直线化拟合结果图2显示, 各处理平均发芽率(
图1, 图2和表1显示, 各处理种子置发芽床后, 分别在第4~8天陆续进入发芽高峰期, 故以第7天的发芽率作为发芽势指标。表2显示, 种子预处理对红芪种子终发芽率、发芽势和发芽指数等质量指标均具有极显著影响(F=38.625, P< 0.001; F=55.169, P< 0.001; F=140.043, P< 0.001), 种荚预处理均改善了红芪种子的发芽特性, 改善程度因预处理的不同而异。去荚浸种12 h后种子发芽集中, 发芽期缩短(图1), 发芽指标最佳(表2), 较对照干种荚发芽率增加46.0%(P< 0.01), 发芽势增加50.0%(P< 0.01), 发芽指数增加5.218(P< 0.01), 且种子在发芽过程中未出现霉变现象。不去荚焖种荚和不去荚浸种荚12 h预处理对红芪种子发芽的促进作用次之, 两处理间种子发芽势和发芽指数均不显著(P> 0.05), 但其终发芽率间的差异性也达到显著水平(P< 0.05), 两处理发芽率均较对照水平显著提高(P< 0.05), 不去荚焖种荚12 h对终发芽率的促进作用更加显著, 尽管第7天种子发芽率仅增加9.3%, 与对照间的差异性未达到显著水平(P> 0.05), 但其终发芽率和发芽指数分别较对照增加29.3%和1.597, 与对照间的差异性均达到极显著水平(P< 0.01)。而不去皮浸种荚12 h后种子发芽势较对照显著增加18.0%(P< 0.01), 发芽率和发芽指数虽均不及焖种处理的水平, 但均较对照极显著提高, 发芽率较对照增加13.3%(P< 0.01), 发芽指数增加1.142(P< 0.01)。浸种12 h条件下, 去皮处理较不去皮处理发芽率增加32.7%(P< 0.01), 发芽势增加32.0%(P< 0.01), 发芽指数增加4.076(P< 0.01)。不去皮处理中, 加水后焖种荚和水浸种荚也均可促进种子吸水吸胀过程, 提高发芽率, 而焖种荚促进作用更佳。各处理对红芪种子发芽的促进作用从大到小依次为去皮浸种12 h> 不去皮焖种荚12 h> 不去皮浸种荚12 h> 不去皮不浸种(对照)(表2)。
| 表2 20℃/18℃自然光照条件下种荚预处理对红芪种子发芽特性的影响 Table 2 Effect of pod pretreatments on germination traits of H. polybotrys seeds under nature-illuminated condition at 20℃/18℃ |
中药资源具有明显的地域性, 地道药材或道地药材是指特定产地出产的著名优质药材[12]。红芪是甘肃省陇南市的主要地道中药材品种之一, 主要依赖种子育苗栽培繁殖, 属可再生中药资源[13]。要获得高产优质的药材, 总是从种子发芽或育苗开始[14]。因此, 种子萌发是药用植物个体生长发育过程中极其重要的环节, 它关系到成苗数及其质量, 进而影响栽培药材的产量和质量, 而种子的发芽率、发芽势和发芽指数均可反映种子发芽的速度和整齐度, 是衡量种子质量的重要指标。王进等[15]提出, 具有硬实特性的种子是充分成熟的种子, 单项的活力指标不能全面反映种子活力的变化, 需采用多种指标。
种子发芽曲线表示种子在整个发芽过程中发芽率的动态变化趋势[16], 从发芽曲线可了解种子发芽的进程和持续时间, 为育苗生产中出苗阶段田间管理提供科学依据。本研究发现, 在各处理中, 红芪种子发芽率变化动态趋势均呈“ S” 型曲线, 符合Logistic曲线方程。红芪种子发芽进程分为3个时期, 即种子萌动期、发芽高峰期和发芽缓增期。从种子置发芽床后第2~6天内各处理种子陆续开始发芽, 发芽最快时期出现在种子置发芽床后第8~10天, 第14~19天发芽陆续结束。浸种预处理有效缩短了种子萌动期, 使发芽提早1~4 d, 延长了种子发芽高峰持续期, 使种子发芽率显著提高, 去荚后浸种效果更佳。
种子的发芽受各种因素的影响, 种子的发育状况、种皮结构、后熟特性和休眠特性均是影响种子发芽的内在因素, 而种皮厚度和发芽期间的环境条件是影响种子发芽的外在因素。对具有硬实和休眠特性的种子人们常采用浸种法和砂搓破皮法促进种子吸水吸胀过程, 以改善其发芽特性, 因为种子只有在吸胀后才可产生赤霉素, 进而诱导水解酶的合成, 促进种子的萌发[16, 17]。大田条件下经砂搓的红芪种子在8 d后发芽率可达31.7%, 而未经处理的干种荚种子发芽率仅4.0%[6]。蔡子平和王宏霞[18]经温汤浸种30 min后分别采用清水、50~200 g/L聚乙二醇、1~4 g/L硝酸钾和50~600 mg/L赤霉素(GA3)等溶剂浸种12 h, 然后在室温自然光照条件下发芽试验表明, 清水浸种发芽率为21.0%, 乙二醇、硝酸钾浸种对红芪种子发芽均有抑制作用, 而GA3浸种对红芪种子萌发有促进作用, 0.400 g/L的GA3浸种后发芽率最为显著水平, 发芽率达34.0%。蔺海明等[5]研究揭示, 在培养箱自然光照条件下, 红芪种子发芽的适宜温度为20~25℃, 发芽率变幅为61.3%~67.3%。本研究在20℃/18℃自然光照条件下发芽试验表明, 干种荚发芽率为34.7%, 种荚预处理极显著改善了红芪种子的发芽特性, 去果荚后浸种效果更佳, 浸种12 h后种子发芽率达80.7%, 较干种荚发芽率增加46.0%, 发芽提早4 d。水浸种相同时间条件下, 去除果荚较不去除果荚处理发芽率增加32.7%, 发芽势增加32.0%, 发芽指数增加4.076。说明果荚造成红芪种子吸水障碍, 对红芪种子发芽具有抑制作用, 去荚后浸种使种子提前完成吸胀过程, 可能提早促进了赤霉素的产生并诱发水解酶, 最终促进种子萌发。
种子是可脱离母体的延存器官, 种子萌发是个体发育的起点。播种后种子是否迅速萌发, 达到早苗、全苗和壮苗, 这关系到能否为栽培作物的丰产打下良好的基础。种子萌发率的降低也会影响植物在群落中的多度[19]。水分是种子萌发的首要条件, 干种子含有的水分都属于束缚水, 不能作为反应的介质, 只有吸水后, 种子细胞中的原生质胶体才能由凝胶转变为溶胶, 使细胞器结构恢复, 基因活化表达萌发所需要的蛋白质, 同时, 吸水能使种子呼吸作用和代谢活动加强, 产生水解酶, 让贮藏物质水解成可溶性物质供胚发育所需要。吸水后种皮膨胀软化, 既有利于种子内外气体交换, 也有利于胚根和胚芽突破种皮生长。由于蛋白质有较大的亲水性, 蛋白质含量高的种子吸水要超过干种子的重量时才能发芽[16]。王彦荣和曾彦军[20]采用浸种法显著提高了结缕草(Zoysia japonica)种子的发芽率, 并指出天然的种子发芽抑制物大多数可能是一些简单的低分子量有机化合物, 可经水浸或水淋后自种子中渗出。红芪为豆科药用植物, 属高蛋白质含量的种子。张鹏等[21]认为, 红芪种子最适发芽地温为15~20℃, 土壤水分含量为180~240 g/kg。张杰等[7]在15℃恒温条件下试验表明, 经清水浸种后红芪种子发芽率为25.0%。本研究发现, 在20℃/18℃自然光照条件下, 不去除荚的红芪种荚经湿焖和水浸种预处理12 h后发芽特性也均得到显著改善, 焖种荚的促进作用更大, 其发芽率、发芽势和发芽指数分别为64.0%, 13.3%和3.462, 较对照干种荚极显著改善, 而水浸种荚后种子的发芽率、发芽势和发芽指数均较干种荚显著提高, 说明湿焖和浸种处理也均可软化红芪果荚, 促进种子吸水吸胀, 同样可起到与发芽诱导物质相同的促进作用, 但湿焖种荚效果更显著, 这可能是由于焖种处理要比浸种处理导致的种子吸胀损伤小的缘故, 这与王进等[15]对苦豆子(Sophora alopecuroides)和苦马豆(Swainsonia salsula)种子发芽特性的研究观点相一致, 即种子硬实破除后, 种子通过缓慢吸水, 有利于细胞膜和酶活性的修复, 避免了对种子的物理伤害和膜损伤。不去荚的种荚浸种过程中水分首先用来软化荚和种皮, 而后才用来满足种子吸水需要, 赤霉素诱发的水解酶产生可能滞后, 而不浸种干种荚在种子置发芽床后才启动荚种皮软化作用, 赤霉素诱发的水解酶产生更加延迟, 当水解酶产生时有些种胚可能已失去原有活力, 若种子萌发期间水分亏缺, 萌发率会更低。
综上所述, 厚实果荚造成的吸水障碍和发芽期间的水分条件是造成红芪种子发芽率低的主要原因。播种前将红芪种荚水浸种或保湿焖种12 h后再行播种均可显著改善红芪种子的发芽特性, 提高发芽率, 为培育壮苗奠定良好基础, 去荚后浸种效果更佳, 当年产种子次年春季发芽率可达80%以上, 该方法简单易行, 安全可靠。对浸种不同时间和机械化去皮技术的研究将是下一步研究的重点。
致谢:甘肃省武都区中药材中心协助种子采集, 甘肃农业大学生命科学技术学院郭凤霞研究员指导统计分析, 西北师范大学生命科学院2011级本科生郭爱峰参与数据录入校对, 在此一并致谢。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [1] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|