作者简介:陈晶(1984-),女,黑龙江哈尔滨人,在读博士。E-mail:ccyj15@163.com
紫花苜蓿叶片中大量的高丰度蛋白(核酮糖-l,5-二磷酸羧化/加氧酶,Rubisco)干扰了蛋白质的动态分辨率,严重影响蛋白质组学研究中功能蛋白的检测与鉴定。为了探究去除高丰度蛋白的适宜方法,本研究利用Mg/NP-40与聚乙二醇(PEG)预分离紫花苜蓿叶片蛋白,通过双向凝胶电泳法比较了不同浓度PEG对叶片高丰度蛋白的分离情况。电泳图谱显示0,15%,17.5%,20%PEG处理的蛋白质中分别可以检测到(335±17),(417±3),(445±7),(459±11)个蛋白质点,0,15%,17.5%处理组间差异显著( P<0.05),17.5%和20%PEG 处理组间没有差异( P<0.05)。然而,17.5%PEG能够检测到更多的差异蛋白质点,证明其更能有效沉淀高丰度蛋白,便于检测被Rubisco遮盖的蛋白质点。将该方法应用于紫花苜蓿叶片响应低温胁迫的蛋白质组学研究中检验其应用效果,与三氯乙酸/丙酮法提取的全蛋白相比,去除高丰度蛋白后鉴定出8个新的蛋白质差异点,证明该方法适用于实际的蛋白质组学研究。可见,Mg/NP-40与17.5%PEG法是最适宜去除紫花苜蓿叶片高丰度蛋白的方法。
The higher content of high-abundance proteins (Ribulose-l, 5-bisphosphate carboxylase/oxygenase; RuBisCo) interferes with the dynamic resolution of proteins in two-dimensional electrophoresis (2-DE), affecting the detection and identification of functional proteins in proteomics. To explore suitable methods for removing high-abundance protein, Mg/NP-40 and different concentrations of polyethylene glycol (PEG) were used for protein pre-fractionation and the treatments’ influence on the separation of proteins in alfalfa leaf was compared. The results indicated that (335±17), (417±3), (445±7) and (459±11) spots were detected in treatments of 0, 15%, 17.5% and 20% PEG respectively. There were significant differences between the 0-17.5% treatments but no significant differences were found between the 17.5% and 20% treatments. More differential protein spots were detected in the 17.5% treatment, which thus proved the most effective way of removing RuBisCo proteins. In order to inspect the applicability of this result, a proteomic study of alfalfa in response to low temperatures was under taken. Compared with total proteins extracted by TCA/acetone, eight new protein spots were identified after PEG treatment to remove high-abundance proteins. The research thus indicates that pre-fractionation with Mg/NP-40 and17.5% PEG is suitable for proteomic studies of alfalfa.
蛋白质组学是21世纪的前沿热点领域之一。近十年来, 其从高度专业化转变为常规的技术手段应用于植物学研究[1]。大量蛋白质数据的挖掘在植物基因功能分析和特殊蛋白质鉴定上发挥了重要作用, 也在一定程度上为基因组和代谢组间构建了“ 沟通” 桥梁[2]。紫花苜蓿(Medicago sativa)是多年生豆科牧草, 其丰富的蛋白质含量及优良的适应性为草业和畜牧业的可持续发展提供了有利条件[3]。对其非生物性(低温、盐碱、干旱、药害等)逆境因子应答反应和抗、耐性机理的蛋白质组学研究具有重要意义。但紫花苜蓿叶片中大量高丰度蛋白[如, 核酮糖-l, 5-二磷酸羧化/加氧酶(Rubisco)]的存在降低了蛋白质的动态分辨率, 极大地影响了逆境应答和代谢过程中功能蛋白的分析与鉴定。
Rubisco作为一种“ 超大量” 蛋白, 普遍存在于绿色植物中。在对拟南芥(Arabidopsis thaliana)和水稻(Oryza sativa)叶片的蛋白质组学研究中发现, 其高丰度蛋白Rubisco及其变体分别占蛋白总量的12%和35.3%, 极易遮盖邻近蛋白, 使一些低丰度蛋白无法被识别[4, 5]。近年来, 国内外科学家一直致力于寻求提高低丰度蛋白分辨率的方法。Cellar 等[6]利用Rubisco免疫耗竭柱去除了叶片组织中90%~98%的Rubisco, 增强了低丰度蛋白的检测和鉴定; 但该方法复杂、耗时且费用较高。Cho 等[7]发现高浓度二硫苏糖醇(dithiothretiol, DTT)可以有效去除水稻叶片中的Rubisco酶, 提高双向凝胶电泳的分辨率; 但DTT 沉淀法原理及其在其他作物中的有效性还需要进一步研究和检验[8]。另外, 也有研究发现肌醇六磷酸钠结合钙离子法可以去除植物叶片中的大部分Rubisco酶, 其在不同植物中有效性及适宜的反应温度也需要检验和筛选[8, 9]。PEG是一种直链大分子聚合物, 能够破坏蛋白质分子表面的水化层而使蛋白发生沉淀作用, 最早应用于一些细菌和病毒蛋白的提纯[10, 11]。Kim等[12]在2001年采用聚乙二醇(PEG)沉淀法预分离了水稻叶片蛋白, 去除了大部分Rubisco。此后该方法又被成功应用于拟南芥[13]、水稻[14, 15]和甜瓜(Cucumis)[16]的蛋白质组学研究中, 有效提高了低丰度蛋白的分辨率, 也是目前应用最多的去除植物高丰度蛋白的方法。与其他方法相比, PEG沉淀法更加快捷、简单、费用低廉且具有较广的适用性。到目前为止, 尚没有探究紫花苜蓿高丰度蛋白去除方法的相关报道。因此, 本试验在前人的基础上, 利用不同浓度的PEG预分离紫花苜蓿叶片蛋白, 旨在筛选去除高丰度蛋白的适宜方法; 并将该方法应用于紫花苜蓿响应低温的蛋白质组学研究中, 检测其可应用性。
紫花苜蓿WL525HQ种子由黑龙江省农业科学院草业研究所提供。2014年, 紫花苜蓿种子播种于混有草炭土∶ 蛭石=2∶ 1的塑料花盆中, 置于昼/夜温度 25℃/20℃, 光周期 16 h/8 h, 湿度约为80%, 光照强度 12000 lx的人工气候箱中。培养至60 d苗龄, 移至温度 4℃, 其他条件相同的恒温箱中处理12 h。于低温处理0和12 h时分别剪取紫花苜蓿叶片若干, 液氮速冻, -80℃保存备用。
1.2.1 蛋白质提取
取冻存叶片(低温4℃处理0 h)2 g, 于液氮中研磨成粉末后加入8 mL 预冷的Mg/NP-40蛋白提取液[0.5 mol/L pH 8.3 Tris-HCl, 2%(v/v) NP-40, 0.02 mol/L 氯化镁, 0.001 mmol/L 乙二胺四乙酸(ethylene diamine tetraacetic acid, EDTA), 0.02 mol/L DTT, 0.001 mol/L苯甲基磺酰氟(phenylmethanesulfonyl fluoride, PMSF)][5], 在冰上研磨10 min。4℃, 12000 r/min离心30 min后取上清液, 弃沉淀。上清液分为4组, 分别加入适量50%(w/v)PEG4000至终浓度为 0, 15%, 17.5%, 20%, 充分混匀后冰浴30 min。以PEG终浓度 0为对照(Control, CK), 其余3组4℃, 12000 r/min离心1 h, 分别取上清记为S1、S2、S3, 相对应沉淀记为P1、P2、P3, 加入3倍体积量-20℃预冷的10% (w/v)三氯乙酸/丙酮, 混匀, -20℃过夜。4℃, 12000 r/min离心1 h, 弃上清, 沉淀中加入3倍体积量-20℃预冷丙酮, 重悬后置于-20℃ 1 h。 4℃, 12000 r/min离心30 min, 弃上清, 沉淀冻干成粉末。
1.2.2 聚丙烯酰胺凝胶(SDS-PAGE)电泳检测
蛋白质干粉中加入裂解液[7 mol/L尿素, 2 mol/L硫脲, 4%(w/v) 3-[3-(胆酰胺丙基)二甲氨基]丙磺酸内盐(3-[(3-cholamidopropyl) dimethylammonio] propanesulfonate, CHAPS), 0.04 mol/L DTT], 振荡均匀后置于摇床上持续振荡1 h, 使蛋白完全溶解。2D-Quant 试剂盒进行蛋白质定量, 留取相应体积蛋白溶液, 其余-80℃冰箱冻存。配制12%分离胶和5%浓缩胶用于SDS-PAGE电泳检测。电泳结束后, 考马斯亮蓝R-250染色, 乙醇冰乙酸脱色至条带清晰。白光扫描仪扫描凝胶, 分析蛋白质分离情况。
1.2.3 双向电泳检测
选用13 cm IPG(pH 4~7)胶条, 蛋白质上样量为650 μ g, 加入水化液[8 mol/L尿素, 2%(w/v)CHAPS, 0.3%(w/v)DTT, 1%(v/v)IPG buffer]稀释至250 μ L。第一向等电聚焦程序为:30 V, 12 h; 200 V, 1 h; 500 V, 1 h; 1000 V, 2 h; 8000 V, 3 h; 8000 V, 45000 Vh; 1000 V, 任意。第二向12.5%聚丙烯酰胺凝胶电泳程序为:10 mA/胶条, 0.5 h; 40 mA/胶条, 2.5~4 h。双向电泳后, 考马斯亮蓝R-250染色, 10%(v/v)冰醋酸脱色后, 白光扫描仪扫描凝胶, 使用ImageMaster 2D Platinum凝胶分析软件进行比对分析。
1.3.1 蛋白质提取
叶片全蛋白提取用传统方法三氯乙酸/丙酮提取法。取冻存叶片(低温4℃处理0, 12 h)各0.5 g置于预冷的研钵中, 加入液氮充分研磨后转移至50 mL离心管中并加入三倍体积-20℃预冷的蛋白提取液[含10%(w/v)三氯乙酸、0.07%(v/v)β -巯基乙醇、1%(v/v)蛋白酶抑制剂的丙酮溶液], -20℃沉淀过夜。4℃, 12000 r/min离心1 h, 弃去上清, 保留沉淀。用三倍于沉淀体积的含有0.07%(v/v)的β -巯基乙醇的冷丙酮将沉淀重悬, -20℃沉淀1 h以上。4℃, 12000 r/min离心1 h, 弃去上清, 保留沉淀。将沉淀冻干成粉末, -80℃保存备用。
低丰度蛋白提取用Mg/NP-40+PEG法, PEG浓度为17.5% (详见1.2.1)。
1.3.2 双向电泳
选用24 cm IPG(pH 4~7)胶条, 蛋白质上样量为1000 μ g, 上样体积为450 μ L。第一向等电聚焦程序为:30 V, 12 h; 200 V, 2 h; 500 V, 2 h; 1000 V, 2 h; 8000 V, 3 h; 8000 V, 65000 Vh; 1000 V, 任意。第二向12.5%聚丙烯酰胺凝胶电泳程序为:1 W/胶条, 1 h; 13 W/胶条, 3.5~4 h。双向电泳后, 考马斯亮蓝R-250染色, 10%(v/v)冰醋酸脱色后, 白光扫描仪扫描凝胶, 使用ImageMaster 2D Platinum凝胶分析软件进行比对分析。
1.3.3 差异蛋白质点的鉴定
筛选出的差异点通过MADLI_TOF/TOF进行鉴定, 所得结果利用MASCOT软件搜索NCBI Medicago、NCBI Viridiplantae 和Uniprot数据库。
本试验中, 所有处理3次重复, 相关数据通过软件DPS进行差异显著度分析。
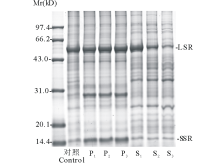
为探究不同浓度PEG对紫花苜蓿叶片高丰度蛋白的分离情况, 对各处理下蛋白质的沉淀和上清部分进行了SDS-PAGE检测。图1是以PEG浓度0%为对照组(control), 不同浓度PEG处理蛋白样品后沉淀和上清部分的SDS-PAGE电泳分析对比图。其中P1~P3与S1~S3分别对应PEG浓度15%, 17.5%, 20% 蛋白样品的沉淀和上清部分。图中对照组高丰度蛋白条带清晰, 聚集在55 kD左右处。而PEG处理后, 沉淀样P1~P3可见清晰的高丰度蛋白条带, 并且Rubisco分散为55 kD左右大亚基(large subunit of Rubisco, LSR)和14.4 kD左右小亚基(small subunit of Rubisco, SSR); 上清样S1~S3高丰度蛋白条带减弱, 其中S2和S3中高丰度蛋白下降更明显, 低丰度蛋白条带清晰稳定。可见, PEG可以沉淀富集紫花苜蓿叶片中的Rubisco, 17.5%, 20%的PEG均可用于去除高丰度。
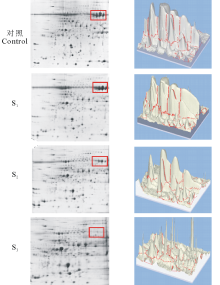
图2显示不同浓度PEG处理下蛋白质样品上清部分的双向电泳图像。图中红框内为高丰度蛋白点, 用3D图像显示丰度。对照和S1可见大量高丰度蛋白点, S2和S3中高丰度蛋白明显减少。而随着PEG浓度的升高可检测出的蛋白质点数目增多(表1), 与对照组重叠的点数减少, 17.5%和20%的PEG处理均可获得较多蛋白质点, 且二者没有显著差异(P< 0.05); 与对照组相比差异点数变化较大, 差异率分别为(33.33± 0.72)%, (56.62± 0.22)%, (52.28± 0.72)%, 差异显著(P< 0.05)。可见, 17.5%和20%的PEG均可用于提取低丰度蛋白, 与SDS-PAGE分
析结果一致, 但17.5%PEG处理下可检测出更多差异点(表1)。在图2的3D图像中, S2的蛋白质点形成相对分离的单峰图像, 可观察到清晰的蛋白点和丰度; S3则蛋白损失过多, 呈现细小尖峰图像。可见, 17.5% PEG更适宜于紫花苜蓿的高丰度蛋白的去除。
为了验证PEG沉淀法在紫花苜蓿响应低温蛋白质组学研究中的可应用性, 紫花苜蓿叶片的蛋白分别用三氯乙酸/丙酮法和17.5% PEG沉淀法进行提取, 双向电泳后经ImageMaster 2D Platinum软件分析确定响应低温的差异蛋白质点。图3为4℃处理12 h下紫花苜蓿叶片的双向电泳图谱(A为三氯乙酸/丙酮法, B为17.5% PEG沉淀法), 数字分别标注了全蛋白和低丰度蛋白响应低温的差异蛋白质点。与未处理的对照组相比, 经低温后紫花苜蓿叶片蛋白(A)中有
| 表1 不同处理下2-DE图像蛋白点统计分析 Table 1 Statistical analysis of protein spots from the PEG fractionation |
14个点蛋白质丰度变化在1.5倍以上(图3), 而PEG去除高丰度蛋白Rubisco后, 低丰度蛋白(B)中发现8个新的差异点(图3)。经MADLI_TOF/TOF鉴定, 所得结果利用MASCOT软件搜索相关数据库确定其蛋白种类(表2)。由鉴定结果可知, 紫花苜蓿叶片蛋白和低丰度蛋白中Rubisco及其变体分别占差异蛋白的50%和12.5%。去除高丰度蛋白后, 可检测出原本被遮盖或因共迁移影响的蛋白质, 其蛋白种类可见表2。可见, 17.5%的PEG可以清除大部分Rubisco, 并可应用于紫花苜蓿响应低温的蛋白质组学研究中。
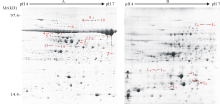 | 图3 紫花苜蓿叶片响应低温的全蛋白(A)和低丰度蛋白(B)双向电泳图 数字表示差异点编号Fig.3 2-DE gels of holoprotein (A) and low-abundance protein (B) in response to low temperature in alfalfa Digits represent spots numbers. |
| 表2 响应低温的差异蛋白鉴定结果 Table 2 Result of identified proteins in response to low temperature |
植物组织中常含有拷贝数众多的高丰度蛋白, 例如, Rubisco作为光合作用中固定CO2关键酶, 一般占蛋白总量的30%~60%, 严重影响邻近蛋白点的识别和其他蛋白点在凝胶电泳中的共同迁移, 从而降低了低丰度蛋白的分辨率[17, 18, 19]。同样的, 由于高丰度蛋白占据了样品中的一大部分, 使得在双向电泳IPG胶条上样容量一定的情况下, 低丰度蛋白的含量受到限制而不易被检测到[20]。而低丰度蛋白作为细胞或组织中的受体分子、信号分子等参与基因表达调控, 往往具有十分重要的功能[19]。因此, 如何去除高丰度蛋白以便分离鉴定低丰度蛋白一直是蛋白质组学研究中亟待解决的问题之一。在以往的文献中发现, 15%~20%PEG可以有效去除植物蛋白中大部分高丰度蛋白, 尤其是Rubisco的大亚基, 但在不同物种或组织中用于预分离的PEG浓度是不同的。在一定范围内, 高浓度PEG对蛋白质的沉淀效率高。Xi等[13]利用16%的PEG去除了拟南芥中大部分高丰度蛋白; 王莹等[21]利用20%PEG提取了水稻叶鞘中的低丰度蛋白; 钟俐等[16]研究发现15%PEG更适宜于甜瓜叶片的低丰度蛋白提取。本研究表明, 适宜的PEG浓度可以去除紫花苜蓿叶片的高丰度蛋白, 且这种筛选是十分必要的。PEG浓度过低无法有效沉淀高丰度蛋白(图2中S1); 浓度过高则易造成蛋白质过度沉淀, 蛋白质点损失(图2中S3)。本研究中, 17.5%PEG能够清除大部分高丰度蛋白, 使原本被遮盖的蛋白质点更易于被检测到; 同时避免了蛋白的过度损失。可见, 该浓度最适宜紫花苜蓿叶片高丰度蛋白的去除。
为了验证PEG沉淀法在紫花苜蓿蛋白质组学研究中的可行性, 比较了三氯乙酸/丙酮法与PEG去除叶片高丰度蛋白后响应低温的差异蛋白变化。三氯乙酸/丙酮法是提取植物蛋白质的常用方法之一[22, 23, 24, 25], 具有降低次生代谢物质的干扰、减少蛋白降解等优点[26, 27]。与其提取的蛋白相比, 17.5% PEG去除了大部分Rubisco, 并检测到8个响应低温的新蛋白质。其中Rubisco大亚基(点L1)主要参与光合作用过程中CO2的固定; 肽酰脯氨酰-顺反式异构酶(点L2)和真核翻译起始因子(点L3)参与蛋白质的翻译和折叠加工[25, 28, 29, 30]; 2-半胱氨酸过氧化物还原酶(点L4和L5)响应低温胁迫下机体内部的氧化还原平衡[31]; 5-甲基四氢蝶酰三谷氨酸高半胱氨酸甲基转移酶(点L6和L7)是一类甲基转移酶, 可为S-甲硫氨酸腺苷途径提供底物; 而放氧增强蛋白(点L8)作为获光复合体的组成元件, 能通过激发叶绿素而获得更多的光能, 并把能量转移到光化反应中心, 有助于增强低温逆境下的光合作用效率[32]。这些新发现的蛋白点在紫花苜蓿叶片中由于高丰度蛋白遮盖而无法检测到。可见, 利用17.5%PEG去除高丰度蛋白在紫花苜蓿蛋白质组学研究中有实际的应用意义, 有助于低丰度蛋白的检测。该方法也可用于紫花苜蓿生长发育或逆境应答的蛋白质组学研究, 有助于功能蛋白的分析与鉴定。
高丰度蛋白影响了紫花苜蓿叶片中低丰度蛋白的鉴定。本研究采用PEG沉淀法, 比较了0, 15%, 17.5%和20%的PEG对高丰度蛋白的分离情况, 结果显示, 17.5%的PEG最适宜用于紫花苜蓿叶片高丰度蛋白的去除。此法应用于紫花苜蓿低温应答的差异蛋白鉴定中, 获得8个新差异蛋白, 证明其适用于紫花苜蓿的蛋白质组学研究。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [3] |
|
| [8] |
|
| [16] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|