作者简介:李小冬(1984-),男,湖南邵阳人,副研究员,博士。 E-mail:lixiaodongzl@163.com
转基因技术对基因功能研究与农作物种质资源创新具有重要作用,在牧草类作物菊苣中相应的研究还处于初级阶段。本研究改进了菊苣组织培养与遗传转化方法,采用暗光培养的菊苣子叶为外植体,经农杆菌侵染后置于光照条件下进行共培养,利用子叶细胞从暗光转移到光照条件下细胞迅速分裂的特点,实现植物遗传转化。与已报道的转化方法(光照条件下的真叶外植体先进行2~3 d预培养,再进行农杆菌转化与共培养)相比,本方法出苗率与已报道方法相当,达90%以上;比不经预培养方法的出苗率要高80%~90%,能极大节省人力物力。同时本研究发现,在愈伤诱导、植物分化以及生根培养中,依次递减细胞分裂素的强度与浓度,能显著降低愈伤和再生苗的玻璃化程度,与一直采用强细胞分裂素相比,改进方法愈伤玻璃化比率下降约9%,再生苗玻璃化比例下降约16%。
Transgenic technology plays an important role in gene function analysis and crop germplasm innovation. However, transgenic studies are relatively recent in chicory. In this study we sought to improve tissue culture and genetic transformation methodology in chicory. Cotyledons grown in the dark were collected as explants. After transformation mediated by Agrobacteria, these explants were grown under illuminated conditions. The cotyledon cells divided rapidly when they were transferred from dark to light. The emergence rate of regenerated seedlings was greater than 90%, similar to that of previous studies however, the germination rate could be improved by 80%-90% if the explants were not pre-cultured. Our results were time, money and labor-saving. We also found that during callus induction, plant differentiation and root growth, decreased intensity and concentration of cytokinin significantly reduced the vitrification of callus and regenerated plantlets. Compared with continuously applied cytokinin our method decreased vitrification of callus and regenerated plantlets by about 9% and 16% respectively.
菊苣(Cichorium intybus)是菊科多年生草本植物, 又称咖啡草或咖啡萝卜。其根、叶均可食, 是一种重要制糖原料、香料、蔬菜及饲草作物[1]; 同时是一种重要的制药原料, 富含倍半萜烯内酯、糖苷、类黄酮、香豆素、花青素、有机酸与细胞分裂素等, 具有治疗腹泻、发热及呕吐功效[2, 3]。自从20世纪80年代引入我国后, 在山西、陕西、浙江、河南等地推广, 现主要分布在西北、华北、东北等暖温带地区[4, 5]。然而由于菊苣原产地在欧洲[6], 我国拥有的野生种质资源比较匮乏, 以常规育种的方法对菊苣遗传改良受到极大的限制。同时其适宜性广, 在全国各地都有种植, 但在各个区域可能面临不同的制约条件, 所以借助现代分子生物学手段实现种质创新, 是菊苣育种的一个重要环节[7]。转基因方法能够打破物种界限, 快速定向的对目标性状进行遗传改良, 加快育种进程, 是一种高效、经济的新技术。
菊苣的体外再生体系从20世纪80年代就已经开始研究, 1985年Profumo等[8]首次利用悬浮细胞系成功诱导了体细胞胚, 培育了再生植株, 科学家们利用根结[9, 10]、叶片[11, 12]、叶柄[13]、茎[14]等不同外植体都成功培育了再生植株。在随后的研究中, 通过在培养基中添加甘油、七叶树甙、硫酸腺嘌呤盐等物质提高菊苣组织培养过程中愈伤与体外再生植株形成的概率, 但转化效率仍然不高[15]。最近的研究主要集中在对组织培养过程的激素种类和浓度进行优化, 特别是强细胞分裂素噻苯隆(TDZ)和6-苄基腺嘌呤(6-BA)的应用, 显著提高了组织培养过程中愈伤诱导与植株分化的成功率[11, 14], 组培体系的成功建立为转基因研究奠定了基础。
与其他农作物相比, 菊苣转基因研究开展的相对较晚, 涉及的目标基因主要包括抗性基因npt 基因[6], 报告基因GUS[16]等, 功能基因的遗传转化仅限于抗冻基因LOL1[17]、抗坏血酸过氧化物酶APX[18]、编码Na+/H+转运蛋白的基因AtNHX1[5]以及TaNHX2[19]等。这些遗传转化方法大都采用3~4周的植株叶片或者须根作为外植体, 在农杆菌转化之前, 外植体材料需先经过一个预培养过程, 以防止农杆菌侵染杀死外植体, 操作过程较为繁琐。错过外植体最佳取样时期、预培养时间不合适以及农杆菌侵染的毒副作用都可能导致转化效率下降甚至转化失败[20]。因此, 研究更加简单、高效、稳定的菊苣转基因方法是实现对菊苣高通量遗传转化的前提与技术瓶颈。
本研究于2013年7月采用贵州省草业研究所育成的牧草品种黔引普那菊苣(Cichorium intybus cv. Puna qianying)为试验材料, 植株培养条件参考[21], 具体为光照16 h, 黑暗8 h, 生长温度22 ℃, 光照强度为230~300 μ E/(m2· s)。
按照表1的配方准备菊苣遗传转化所需所有的培养基, 并调整pH到5.8, 灭菌备用, 植物激素和抗生素在使用前加入。
| 表1 菊苣遗传转化所需培养基的配方 Table 1 Components of the medium used in this study |
挑选300粒饱满的菊苣种子, 放入50 mL离心管中, 用45 mL自来水浸泡10~15 min, 去除表面漂浮的劣质种子与自来水。加入45 mL 75%的酒精, 剧烈震荡, 消毒处理2~3 min。去除酒精, 加入45 mL市售84消毒液, 剧烈震荡, 消毒处理10 min。更换新鲜的84消毒液, 重复该步骤一次。去除84消毒液, 用45 mL灭菌水清洗种子3~5次。将消毒好的种子播种于M0培养基, 置于22 ℃黑暗培养箱培养3~5 d至种子萌发。子叶外植体制备:在超净工作台中, 剪取新生的子叶, 用手术刀将其分开并切成2~3个小块, 制备的外植体放置于暗光条件下备用。真叶外植体制备:取生长28 d的无菌苗的真叶用手术刀将其切成3~5 mm2的小块备用。
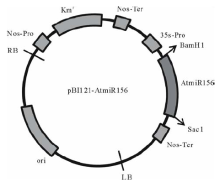
转化所用的载体为pBI121-AtmiR156过量表达载体(图1), 农杆菌菌株为GV3101, 将保存的菌种在抗性平皿(LB+50 mg/L Gent+50 mg/L Km, LB配方:酵母提取物5 g/L, 胰蛋白胨10 g/L, 氯化钠10 g/L)上划线活化, 28 ℃培养3 d, 挑取活化的含有目标质粒的农杆菌单菌落到5 mL LB+25 mg/L Gent+50 mg/L Km的液体培养基, 28 ℃, 220 r/min摇床上活化24 h。按照1:50的比例将活化的菌液接种到50 mL LB+25 mg/L Gent+50 mg/L Km的培养基中, 28 ℃, 220 r/min转速下培养8~16 h, 至菌液OD600=0.8。 取 20 mL新鲜培养的菌液, 室温5000 r/min 离心15 min。弃上清, 加入20 mL DM培养基, 用5 mL移液器轻轻将农杆菌菌体悬浮于DM培养基里。去上清, 用20 mL DM重新悬浮一次, 取2 mL悬浮菌液稀释到20 mL DM培养基中, 农杆菌准备完成, 在2 h内使用效果不受影响。
将准备好的外植体与农杆菌一起放到无菌培养皿中, 浸染15~20 min, 隔4~5 min轻轻摇晃培养皿一次, 使农杆菌与外植体充分接触。去除转化菌液, 将侵染好的外植体转到M1培养基中, 每皿60~70个外植体, 置于人工气候室, 24 ℃的条件下共培养2~3 d。用加100 mg/mL头孢霉素的无菌水清洗共培养的外植体2~3次, 然后将共培养的外植体均匀放置于M2培养基上培养至长出绿色愈伤。将绿色愈伤转到M3培养基中, 每星期继代一次, 直至绿芽长至2~5 cm。将再生植株从愈伤组织上切下, 插入到M4培养基中生根培养15~20 d, 直到根系发育完成。将培养瓶盖打开, 加入5~10 mL无菌水, 在人工气候室开盖炼苗5~7 d, 将无菌苗取出, 洗净根部的琼脂, 移栽到泥炭土:蛭石=1:1的基质中, 置于人工气候室培养。
采用天根DNA提取试剂盒(DP305-2)提取转化植株的DNA, 采用上海生工 2× Taq PCR反应试剂盒检测表达载体上NPT基因, 上游引物NPTF [5'-GTGCCCTGAATGAACTGC-3'], 下游引物NPTR [5'-CAATATCACGGGTAGCCA-3']组合进行PCR检测。配制PCR反应混合物:2× Taq PCR Mixture, 10 μ L; NPTF(10 mmol/L), 1 μ L; NPTR(10 mmol/L), 1 μ L; DNA, 2 μ L; dd H2O, 6 μ L。反应程序如下:94 ℃ 3 min, 94 ℃ 30 s, 58 ℃ 45 s, 72 ℃ 30 s, 30循环, 72 ℃ 5 min。
采用Excel 2010进行实验数据分析, P< 0.05被认为是差异显著, 作图采用Excel 2010 与PowerPoint 2010。
将消毒好的菊苣种子均匀播种在1/2 MS培养基上黑暗培养5~7 d至2片子叶张开(图2A), 挑选饱满健壮的子叶从下胚轴处剪下, 并用解剖刀将其中分为2份, 加入准备好的农杆菌菌液进行遗传转化(图2B), 将转化好的外植体均匀放置于共培养基上, 光下培养2~3 d(图2C), 将共培养组织转移到愈伤诱导培养基上, 每星期更换一次培养基, 直到长成黄绿色绿色愈伤组织, 并将其转移到分化培养基上培养2~3周, 每周将愈伤转移到新鲜培养基直到长出绿色芽点(图2D), 将再生芽切下转移生根培养基(图2E), 待植物长出不定根后将培养瓶打开炼苗3~5 d(图2F), 将转基因材料移栽到花钵(图2G), 通过PCR等分子手段对转基因植株进行鉴定, 将阳性植株转移到大田进行加代繁殖(图2H)。
本实验分别采用子叶与真叶两种不同的外植体对菊苣进行遗传转化, 其外植体制备的详细过程参照材料与方法1.3。在未经预培养直接进行农杆菌侵染条件下, 子叶外植体的出愈伤比例能达95.79%(表2), 而真叶直接侵染存活率只有0.86%(表2)。将外植体进行一个短暂的预培养(2 d), 以真叶为外植体的出愈伤的比例显著提高达到93.31%(表2), 与子叶的效果相当。经过2 d预培养的子叶外植体进行农杆菌转化时, 愈伤诱导率与处理1相比略有下降, 但差异不显著(表2)。从愈伤诱导效果、实验时间成本和经济成本综合考虑, 处理1以3~5 d子叶外植体直接进行农杆菌侵染的转化方法最好。
| 表2 不同外植体来源和处理方式对愈伤形成率的影响 Table 2 Different callus induction rates of two explants of cotyledons and true leaves |
在诱导愈伤以及再生苗分化过程中我们发现组培过程中再生组织玻璃化程度与细胞分裂素的强度密切相关, 以子叶为外植体, 在共培养阶段采用强细胞分裂素0.01 mg/L TDZ+1.0 mg/L IAA快速诱导细胞分裂, 在诱导愈伤以及分化过程分别采用不同强度的细胞分裂素进行诱导, 包括0.01 mg/L TDZ+1.0 mg/L IAA, 2.0 mg/L 6-BA+1.0 mg/L IAA, 1.0 mg/L 6-BA+1.0 mg/L IAA 3种不同(浓度)的激素组合。其中, 在愈伤和再生苗诱导过程中, 采用低分化强度的细胞分裂素6-BA诱导能显著减低玻璃化比例, 最适宜的愈伤诱导激素组合为2.0 mg/L 6-BA+1.0 mg/L IAA, 最适宜的再生苗诱导激素组合为1.0 mg/L 6-BA+1.0 mg/L IAA(表3)。
| 表3 不同激素组合对愈伤及再生苗玻璃化的情况 Table 3 Different vitrification rates of callus and regeneration seedlings resulted from different phytohormones |
采用检测抗性标记的方法PCR扩增140个转基因菊苣抗性标记NPT基因。并进行电泳分离, 结果显示132个单株(94.3%)能够扩增出目的条带, 大小与阳性对照(以pBI121质粒为模板)相同, 而阴性对照(以非转基因菊苣为模板)则无扩增, 表明转化材料中已经含有外源基因DNA片段(图4A), 随机挑选22株阳性转基因植株, 与阳性对照(pBI121-AtmiR156)和阴性对照(非转基因植株)一起, 利用35S+AtmiR156R进行检测扩增, 所有挑选的植株都能扩增出目标条带(图4B)。
转基因作物具有高产、稳产等特点, 是解决粮食短缺、环境破坏等世界性难题的主要手段之一, 农作物转基因研究是未来农业研究的一个热点与重点领域[22]。以棉花(Gossypium hirsutum)、油菜(Brassica campestris)、玉米(Zea mays)以及木瓜(Chaenomeles sinensis)为代表的农作物的转基因育种及推广工作已经取得了巨大的突破, 通过转基因技术已经在农作物产量、抗逆性、抗病虫以及抗杂草等方面对传统品种实现定向改良[12, 23]。然而, 牧草类作物开展相关研究相对较少, 在苜蓿(Medicago sativa)、饲用玉米等应用较广的牧草品种已经有成功报到, 通过过量表达野生大豆(Glycine soja) WRKY20能够增强紫花苜蓿对干旱和盐胁迫的抵抗力[24]。过量表达CBF基因能够显著提高饲用玉米对低温的抵抗力[25]。然而对于应用相对较少的牧草开展基因工程研究相对滞后, 制约转基因研究的技术瓶颈就是高效率的遗传转化体系的建立。
菊苣是一种优质的菊科牧草, 在西南喀斯特地区, 酸性土壤及高温干旱气候限制了紫花苜蓿应用推广, 菊苣重要性更加突出。前人对菊苣组织培养和遗传转化早已展开, 并建立多个以不同营养器官为外植体来源的组培再生体系, 然而只有有限的转基因研究被报道, 主要原因之一是遗传转化效率不高, 在赵龙等[4]的研究中, 普那菊苣(Cichorium intybus cv. Puna)阳性转化率只有10%, 将军菊苣(Cichorium intybus cv. Cmmadrhne)只有13%, 不能满足高通量遗传转化的需要。与已建立的方法相比, 本研究的方法在遗传转化的多个环节都有技术革新[26]。在外植体准备方面, 我们采用暗培养的子叶组织作为外植体, 前人多用4周大的真叶叶片或叶柄等作为外植体, 比较脆弱, 承受不了酒精和84消毒液(对植物伤口损伤较大, 对人危害较小)的毒害而只能用剧毒的升汞(对植物伤口损伤较小, 对人危害较大)来灭菌。本发明采用的子叶外植体可以由消毒的种子萌发而来, 而子叶由于有种皮保护, 可以采用酒精和84消毒液灭菌方法, 保护实验操作者和环境免受升汞的危害。此外, 本研究的方法简化了实验步骤、缩短了实验时间、减少了实验成本。以真叶为外植体的研究中, 外植体准备需要4周, 制备的外植体需要预培养2~3 d才能用于遗传转化[20], 本研究以子叶为外植体只要萌发3~5 d, 即可直接用于遗传转化。由于子叶细胞贮存了丰富的营养物质, 具有良好的分生能力。在黑暗条件下, 子叶细胞分裂受到抑制, 在恢复光照条件后能利用自身的营养物质迅速分裂[21]。因此, 不需要对外植体预培养可直接用于遗传转化, 极大地减少了人力、物力与时间成本。
细胞分裂素的种类和浓度对组培再生苗具有重要影响[11]。在共培养时, 希望能够迅速诱导细胞分裂完成遗传转化, 采用强细胞分裂素诱导细胞分化。在后续的愈伤诱导、植株分化以及生根培养等环节我们采用强度和浓度递减的细胞分裂素进行培养, 有效地降低了再生苗的玻璃化比例(图5)。本研究建立的遗传转化方法成功率高, 操作简单, 可以进行高通量操作。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [4] |
|
| [5] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [26] |
|