作者简介:贾辉(1981-),男,甘肃古浪人,在读博士.E-mail:jiah66@163.com
为了从东祁连山高寒草甸土壤中分离筛选纤维素分解细菌,本研究根据在羧甲基纤维素钠培养基和滤纸平板培养基上的生长情况,初步筛选出3株具有较强纤维素分解能力的细菌,并对其生长条件进行了初步研究,结果表明,3株菌的最适生长温度范围为25~30℃;最适生长pH因菌种不同位于5~8之间;最适生长盐浓度位于4%~5%.菌株X1-2具有较好降解特性,根据形态观察,革兰氏染色及16S rRNA系统发育比较,鉴定该菌为芽孢杆菌( Bacillus sp.),是一株十分具有开发生产纤维素酶能力的菌株.
Eight bacterial strains were isolated from soil in the east Qilian Mountains. Of these, four strains had a higher capacity for degradation of plant cellulose when cultured on a CMC-Na plate medium. The growth characteristics of the four strains were studied, and the optimum temperature range of the 4 active strains was 25-30℃, the optimum pH for growth was 5-8, and the optimum sodium concentration was 4% to 5%. A strain designated X1-2 possessed the highest cellulose degradation ability. Based on morphology, gram stain reaction, and 16S rRNA phylogenetic comparison, this strain was identified as a member of the genus Bacillus ( Bacillus sp.). It is a bacterium with strong plant cellulose degradation ability.
纤维素是葡萄糖残基以β -1, 4-糖苷键连接而形成的线性葡聚糖, 是一种广泛存在于植物中的骨架多糖[1, 2].纤维素丰富的糖源可以用于许多原料加工工业.遗憾的是许多纤维素废弃物通常被燃烧处理掉, 这是一个普遍存在于发展中国家甚至是全球的浪费现象[3, 4], 由此形成的环境污染问题和资源浪费都已经相当严重.因此, 研发大规模, 工业化和经济节约的天然纤维素资源化转化技术是摆在当今世界的一大课题.利用微生物分解转化纤维素类物质可以将其变为饲料, 栽培基质, 有机肥料, 化工原料等[5, 6, 7].纤维素酶是纤维素降解过程中的重要酶类物质, 包括3类可溶性细胞外的酶:1, 4-β -内切葡聚糖酶, 1, 4-β -外切葡聚糖酶和β -葡糖苷酶.许多微生物包括许多细菌, 真菌和放线菌都有产纤维素酶的能力.自然界中具有纤维素分解能力的菌株很多, 例如:梭状芽孢杆菌, 球毛壳菌, 木霉, 青霉属, 曲霉, 担子菌, 虫拟蜡菌, 木腐菌和青霉菌等[8, 9, 10].但目前获得的菌株其纤维素酶活力普遍较低[11, 12, 13], 即使酶活力很高的菌株继代培养后表现出退化或不稳定, 这些因素一直是阻碍纤维素酶大规模生产应用的瓶颈问题[14, 15, 16, 17].筛选高效纤维素酶活力的菌株仍然是人们努力的目标[18, 19].东祁连山高寒草甸金枪河流域, 植物群落多样性复杂, 微生物资源丰富, 本研究拟从该地区土壤中筛选高产纤维素分解细菌, 通过对其纤维素降解能力和生物学特性测定, 旨在获得能够高效, 快速降解纤维素的优良菌种.
2013年5月土样采集自祁连山高寒草甸甘肃省天祝县金枪河地区.主要供试培养基有以下几种:羧甲基纤维素钠(CMC-Na)平板培养基:NaNO3 2 g, K2HPO4 1 g, KCl 0.5 g, MgSO4 0.5 g, FeSO4 0.01 g, CMC-Na 10 g, 琼脂10 g, 蒸馏水1000 mL.滤纸平板培养基:NaNO3 2.5 g, KH2PO4 1 g, CaCl2· 6H2O 0.1 g, MgSO4 0.3 g, NaCl 0.1 g, FeCl3 0.01 g, 滤纸条10 g, 蒸馏水1000 mL, 无菌滤纸, pH自然.牛肉膏蛋白胨(NA)培养基:牛肉膏3 g, 蛋白胨5 g, 琼脂8 g.NB培养基:牛肉膏3 g, 蛋白胨5 g, 葡萄糖2.5 g.
1.2.1 具有降解纤维素能力的细菌分离 称取各样10 g加入90 mL无菌水, 将样品振荡10~15 min, 使土壤颗粒均匀分散成为悬液, 静置数分钟, 吸取1 mL土悬液到9 mL稀释液中, 依次按10倍法稀释, 通常稀释到10-4成一系列稀释液.取1 mL土悬液接种于羧甲基纤维素钠平板培养基上, 用玻璃刮刀使其均匀涂抹于培养基表面, 每稀释度设3个重复, 在28~30℃ 温箱中培养, 待菌落长成后, 按菌落特征归类和编号, 然后将菌落特征不同的细菌转入NA斜面培养基培养, 纯化后保存备用.
1.2.2 供试细菌分解纤维素能力的测定 对CMC-Na分解能力的测定:挑取分离的细菌菌落接到CMC-Na平板培养基上, 于25℃ 避光培养7 d, 采用刚果红染色, 记录各菌株的透明圈大小.
对滤纸分解能力的测定:将分离得到的具有纤维素分解能力的菌株, 接入NB培养基中20℃ 摇床培养5 d后制成菌悬液, 于盛有50 mL液体培养基的150 mL三角瓶中放入2.6 cm× 6.2 cm的滤纸条, 接入1 mL菌液100 r/mim进行恒温振荡培养8 d, 以滤纸条的断裂程度评价降解效果.
对中华羊茅(Festuca sinensis)凋落物分解能力的测定:称取5 g中华羊茅凋落物, 放入盛有100 mL液体培养基的250 mL三角瓶中, 然后接入1 mL菌液, 100 r/mim进行恒温振荡培养15 d后取出, 烘干称重, 按下列公式计算中华羊茅的减重百分比, 确定菌种分解中华羊茅凋落物的能力.
W=(S-S1)/S× 100%
式中, W代表中华羊茅凋落物分解百分比, S代表中华羊茅凋落物的原始干重, S1为中华羊茅凋落物溶解后的烘干量.
1.2.3 纤维素降解菌的生长条件测定 最佳生长温度的测定:将复选出的菌种接于细菌液体培养基, 分别置于5, 10, 15, 20, 25, 30, 35, 40, 45℃ 等9个温度下悬浮培养, 每处理3 次重复, 3 d后测定菌液的OD600值, 并根据OD600值的大小判断不同温度条件下菌体的生长状况, 确定其最适生长温度.
最佳生长酸碱度的测定:pH值分别用4.0, 4.5, 5.0, 5.5, 6.0, 6.5, 7.0, 7.5, 8.0, 8.5, 9.0磷酸缓冲液配制成11个浓度, 置于上述所测最适温度下培养, 每处理3 次重复.3 d后测定菌液的OD600值, 并根据OD600值的大小判断不同pH条件下菌体的生长状况, 确定其生长的最适pH值.
耐盐能力的测定:在28℃ 条件下, 将NA培养液中NaCl含量分别调到0.5%, 1.0%, 1.5%, 2.0%, 2.5%, 3.0%, 3.5%, 4.0%, 5.0%, 6.0%, 7.0%, 8.0%和9.0%, 然后接入菌体.48~72 h后取出用分光光度计进行测定, 记录OD600数值.
1.2.4 菌株的分子生物学鉴定 引物设计:根据16S rDNA两端的保守序列, 设计1对细菌的通用引物.引物1序列:5'-CCGGATCCAGAGTTTGATCATGGCTCAGCA-3'; 引物2序列:5'-CGGGATCCTACGGCTACCTTGTTACGACTT-3', 由上海生物工程技术有限公司合成.
菌株DNA 的提取和纯化:采用Ezup柱式细菌基因组DNA抽提试剂盒, 16S rRNA基因的扩增按文献[9]进行.
系统发育分析:将纯化PCR产物送至上海Sangon生物技术公司测序, 并将获得的序列与NCBI数据库中已报道的与该序列相似性较高的典型菌株的序列进行同源性比较.采用Clustal 1.8软件进行多序列比对, 再用 MEGA 4.1中的Neighbor-joining (NJ)方法构建系统发育树, 用Bootstrap对系统树进行统计检验, 确定菌株的系统发育学地位.
所得数据用SPSS 17.0软件进行处理和分析, 并用Excel软件作图.
将初次分离的8株细菌接在NA培养基上培养3 d后, 对菌落形态特征进行描述(表1).
| 表1 菌落培养特征描述 Table 1 Cultural features of bacteria |
2.2.1 菌种分解CMC-Na能力测定 将8株分离获得的具有纤维素分解能力的细菌, 根据水解圈直径(D2)与菌落直径(D1)的比值可以看出, 菌株X1-2分解纤维素的能力最强, X1-1和X2次之, X5的纤维素分解能力最弱(表2).
| 表2 纤维素分解菌株的CMC-Na分解能力测定 Table 2 Diameter ratio between cellulose decomposing circle and bacterial colony on flat of CMC-Na |
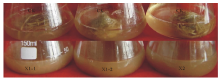
2.2.2 滤纸崩解试验 对获得的8株纤维素分解细菌进行摇瓶滤纸崩解试验, 探究其纤维素分解能力, 在15 d的滤纸崩解试验中, 有3株细菌表现出明显的滤纸降解效果(图1), 其菌株X1-1, X1-2和X2中滤纸基本完全崩解, 摇瓶中的液体处于半清状, 表明该3株细菌对滤纸具有明显的分解能力.
2.2.3 中华羊茅分解定量测定 根据获得的菌株在CMC-Na平板上的生长情况和水解结果, 以及滤纸的崩解试验结果, 选择3株细菌X1-1, X1-2和X2进一步研究它们对中华羊茅纤维素的分解效果.对3株细菌分别培养5, 10, 15 d后的中华羊茅重量变化情况进行了测定, 结果见图2和表3.
| 表3 纤维素分解菌株对中华羊茅纤维素分解能力测定 Table 3 Changes of quality of F. sinensis after being degraded for 15 days by 3 strains |
培养5 d后, 3株细菌对中华羊茅纤维素都有所分解, 但差异性不显著, 其中中华羊茅的分解率分别为9.8%, 13.9%和11.3%.培养10 d后3株菌株对中华羊茅的分解率都有了显著的增加, 分别为22.8%, 35.0%和26.3%, 尤其是菌株X1-2降解中华羊茅纤维素的能力最高, 继续培养至15 d后菌株X1-2使得中华羊茅的分解率达到了55.4%, 分解效果明显.
2.3.1 温度对菌体生长的影响 试验结果表明, 接菌培养3 d后, 3种菌在15~45℃ 均能够生长.X1-1最适生长温度为25℃ , 在30和35℃ 均生长良好, 与25℃ 相比差异显著(P< 0.05), 低于25℃ , 在15, 10和5℃ 时菌体生长明显受阻, 与25℃ 相比差异显著(P< 0.05); X1-2最适生长温度为25℃ , 低于20℃ 或高于30℃ 对菌体生长均产生明显的差异(P< 0.05); X2在15~45℃ 之间生长差异不显著(P> 0.05), 且随着温度的上升, 生长有增强趋势, 属高温菌(表4).
| 表4 温度对菌株生长的影响 Table 4 Effect of temperature on growth of the strains |
2.3.2 pH对菌体生长的影响 试验结果表明, 3株细菌在pH为4.5~8.5之间均能生长, 但最适生长的pH值存在较大差异.X1-1偏酸性, 最适pH值为5.5, 与pH为5.0差异不显著(P> 0.05), 大于5.5或小于5.0均存在显著性差异(P< 0.05); X1-2生长的酸度范围较广; X2的最适pH均为8.5, 大于或小于8.5存在显著差异(P< 0.05).总体可见偏酸环境(pH< 4.5)对3种菌均有不同程度的抑制作用, 与对照无明显差异(P> 0.05)(表5).
| 表5 pH对菌株生长的影响 Table 5 Effect of pH on growth of the strains |
2.3.3 盐浓度对菌体生长的影响 试验表明, 每种菌体的最适盐浓度不同, X1-1最适盐浓度为6.0%, 与5.0%差异不显著(P> 0.05), 大于6.0%或小于5.0%均存在显著差异(P< 0.05); X1-2最适盐浓度为3.0%, 与1.0%, 1.5%, 2.0%和2.5%差异不显著(P> 0.05), 说明X1-2耐盐性较差; X2在0.5%~8.0%的盐度范围内生长差异不显著(P> 0.05), 即X2对盐度具有广泛的适应性, 有一定的耐盐能力; 总体上3个菌株的盐浓度承受值X2> X1-1> X1-2(表6).
| 表6 盐度对菌株生长的影响 Table 6 Effect of NaCl on growth of the strains |
综合评价几株细菌的CMC-Na水解圈试验, 滤纸崩解试验以及中华羊茅分解试验, 菌株X1-2对纤维的分解能力最强, 生长速度快, 易培养, 具有进一步研究开发的潜力, 因此, 本试验通过形态学和分子生物学技术, 对该细菌进行了分析鉴定(图3和图4).
 | 图3 菌株X1-2菌落和菌体形态A:NA培养基中菌落照片NA medium colony photos; B:革兰氏染色显微照片Gram staining micrograph.Fig.3 Micrograph of strain X1-2 with colonies on a NA plate and its morphology |
菌株X1-2为好氧, 杆状, 周生鞭毛, 能运动, 菌落乳白色, 表面无光泽且较粗糙, 边缘不整(图3A).在NA培养基上, 易培养, 生长较快, 革兰氏阳性菌(图3B).
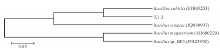
由测序结果可知, 菌株X1-2的16S rRNA 序列全长为1443 bp.通过与GenBank中序列比对, 调取与之基因序列最为相近的菌种使用MEGA 5.0进行Clustal X多序列匹配比对, 构建系统进化树(图4).结果表明, 菌株X1-2与芽孢杆菌系统发育关系密切.结合形态特征, 初步确定菌株X1-2属于芽孢杆菌属中的枯草芽孢杆菌(Bacillus subtilis).
滤纸属纤维素类物质, 能够在滤纸上生长的菌种, 说明可以利用滤纸作为碳源, 滤纸片液体培养基中滤纸片的溃烂程度可以证明供试菌种具有纤维素分解能力.在本研究中首先以供试菌种在CMC-Na培养基的生长情况和透明圈大小作为指标, 筛选出具有纤维素分解能力的细菌, 然后结合滤纸平板上的生长情况, 滤纸片液体培养基中的生长情况, 选用多个指标进行初步筛选, 避免了单一筛选方法的不足, 多指标筛选体系的建立可防止试验误差可能出现的漏选菌种.
细菌分解纤维素时, 首先是细菌黏附在纤维素上, 在多种酶的协同作用或多纤维素酶的作用下, 在接触点纤维素被溶解, 细菌从纤维素的表面向内增生, 逐渐分解纤维素.由于天然分解菌活性低, 降解速度慢, 而纤维素的降解需要多种酶协同作用, 所以充分利用自然界多种微生物的协同关系, 人工筛选构建能够产生多种纤维素酶的高效稳定菌系, 引起了人们的高度重视.
稳定性试验过程中发现, 当外界条件(如温度, pH值, 盐浓度)几乎相同时, 3个菌种一直很稳定.采用CMC-Na培养基和刚果红染色相结合的方法进行筛选, 淘汰了纤维素分解能力不稳定的菌株, 保证了具有稳定遗传特性的菌株基因资源, 将菌株的稳定性作为一个指标进行筛选, 目标性更强, 并且具有实际的意义.
研究供试菌种的培养条件对菌体生长的影响, 对了解菌体的生物学以及生理学特性具有重要的意义, 尤其是对一些新的微生物资源的认识和开发利用更具有不可估测的作用.本研究通过温度, pH值, 盐浓度3个培养条件对菌体生长进行了初步研究.
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|