作者简介:邵麟惠(1981-),女,甘肃合水人,在读博士。E-mail:shaolinhui@126.com
泛素化在植物生长和发育过程中起重要作用,E3泛素连接酶负责对靶蛋白特异性识别,其中U-box结构的E3泛素连接酶具有调控植物生长发育和免疫反应等功能,并在抗逆性方面发挥作用。目前,关于蒺藜苜蓿U-box家族基因的研究尚未见报道。本研究从蒺藜苜蓿中克隆得到U-box ( MtPUB4)基因,该基因cDNA全长2448 bp,编码815个氨基酸,包括1个U-box结构(C-X2-H-X7-C-X7-C-X2-C-H-X2-H)和5个ARM结构域,属于U-box/ARM类型E3泛素连接酶。构建原核表达载体pET- MtPUB4,通过聚丙烯酰胺凝胶电泳(SDS-PAGE)表明在大肠杆菌中表达了MtPUB4蛋白。荧光定量PCR分析表明 MtPUB4基因在蒺藜苜蓿花中的表达量最高,在根中表达量最低。 MtPUB4基因受到NaCl、聚乙二醇、脱落酸诱导,随着诱导时间增加,表达量呈现出增长趋势。这些结果表明, MtPUB4基因在蒺藜苜蓿生长发育和抗逆性中可能起到重要调节作用,但在低温胁迫中表达量稍微下降,变化不明显。本研究成功构建了pBI121- MtPUB4植物表达载体,为进一步转化拟南芥突变体 Atpub4奠定了基础。
The E3 ubiquitin ligase is essential for the specific recognition of target proteins of ubiquitin, and therefore, it plays an important role in plant growth and development. The U-box family of E3 ubiquitin ligases function in regulating plant immune responses and stress resistance. To the best of our knowledge, there have been no reports on U-box family genes in Medicago truncatula. In this study, a U-box gene ( MtPUB4), consisting of a 2448-bp cDNA encoding a putative protein of 815 amino acids, was cloned from M. truncatula. A sequence alignment analysis revealed that the MtPUB4 protein contains a U-box domain (C-X2-H-X7-C-X7-C-X2-C-H-X2-H) and two ARM (Armadillo) regions. Therefore, it was classified as a U-box/ARM E3 ubiquitin-ligase. We constructed a prokaryotic expression vector (pET- MtPUB4), and an SDS-PAGE analysis confirmed that the MtPUB4 protein was successfully expressed in prokaryotic cells. Real-time polymerase chain reaction analyses showed that the transcript levels of MtPUB4 were higher in flowers and lower in roots. Abiotic stresses such as NaCl, polyethylene glycol, and abscisic acid resulted in increased transcript levels of MtPUB4, with higher transcript levels after longer induction times. The transcript levels of MtPUB4 decreased slightly under low-temperature stress. These results indicated that MtPUB4 may be involved in regulating growth, development, and stress resistance in M. truncatula. The construction of the pBI121- MtPUB4 vector has laid the foundation for transformation of Arabidopsis in future studies.
泛素化是真核生物细胞中重要的蛋白质翻译后修饰的过程, 对生物体生长发育和生物体对周围环境适应性起调控作用, 其中泛素分子是由76个高度保守的氨基酸组成的多肽[1]。该过程首先是靶蛋白被泛素分子标记, 然后被蛋白酶体识别后降解[2]。标记靶蛋白的过程由E1泛素活化酶、E2泛素结合酶和E3泛素连接酶共同介导催化完成[1]。E1泛素活化酶依靠ATP提供能量催化泛素分子与底物蛋白结合, 同时激活泛素分子转移至E2泛素结合酶, 最后通过E3泛素连接酶与赖氨酸残基结合标记靶蛋白[3, 4, 5]。E3泛素连接酶在靶蛋白特异性识别中起关键作用, 依据共价键结合方式, 可分为HECT (homologous to the E6-AP carboxyl terminus)结构域和RING/U-box结构域[6]。近年来研究表明, E3泛素连接酶参与了各种抗病信号反应途径的调控, 其中U-box蛋白也在抗非生物胁迫和抗病过程中发挥作用[7, 8]。
U-box/ARM蛋白是植物中特有的一类蛋白, 由70多个氨基酸残基构成, 功能域最初在酵母UFD2蛋白中发现, 在多种真核生物中高度保守[9]。植物U-box蛋白的数量多于其他生物, 目前在拟南芥(Arabidopsis thaliana)中已经鉴定出64个U-box蛋白[10], 水稻(Oryza sativa)中鉴定出77个U-box蛋白[11], 蒺藜苜蓿(Medicago truncatula)中鉴定出41个U-box蛋白[12]。研究表明, 拟南芥pub4基因影响花粉绒毡层细胞生长发育, 在花粉发育的第8~9期开始出现差异变化, 其突变体在22 ℃时花粉绒毡层细胞过度生长膨胀或延迟退化、减小了花粉囊腔空间, 使花粉粒被挤压粘连、无法释放传粉而造成雄性不育, 却在16 ℃的低温时可恢复部分育性, 说明该基因表达方式对温度敏感[3]。因此, 推测利用此类基因特性可创制出温敏型雄性不育材料。此外, 近年研究人员发现, U-box类基因也参与植物非生物胁迫应答反应, 拟南芥AtPUB22和AtPUB23响应干旱胁迫[7], AtPUB18和AtPUB19基因受NaCl诱导表达[13], 辣椒(Capsicum annuum)基因CaPUB1在拟南芥中超表达可以增强植物的耐盐性[14]。
蒺藜苜蓿是豆科苜蓿属草本[15]。二倍体(2n=2x=16), 具有生育期短(80~100 d)、基因组小(454~526 Mb)、自花授粉、易于转化、再生时间较短等特点, 被作为豆科模式植物进行研究, 目前已完成全基因组测序[12]。紫花苜蓿(Medicago sativa)与蒺藜苜蓿同属于苜蓿属植物, 具有相似的遗传特点, 从蒺藜苜蓿中获得的信息对研究其他豆科植物特别是紫花苜蓿具有重要参考价值。目前, 有关蒺藜苜蓿U-box基因家族的研究尚未见报道[12]。因此, 本试验以蒺藜苜蓿为研究材料, 利用植物U-box基因序列高度保守的特点, 采用RT-PCR方法对蒺藜苜蓿U-box基因编码区序列进行克隆研究, 以期为蒺藜苜蓿U-box基因在花粉发育过程中所起的调控作用和该类基因抗逆特性进行初步探索, 为今后通过基因工程手段选育新种质奠定理论基础。
选取蒺藜苜蓿A17基因型, 蒺藜苜蓿种子由本实验室保存。
RNA提取使用TransZol Up Plus RNA Kit(ER501)试剂盒, cDNA反转录使用TransScript II One-Step gDNA Removal and cDNA Synthesis Supermix(AH311)试剂盒, PCR扩增使用TransStartFastPfu Fly DNA Polymerase酶, 实时荧光定量使用TransStart Top Green qPCR SuperMix试剂盒, 购于北京全式金生物有限公司。DNA maker DL5000、限制性内切酶BamHI、T4 DNA Ligase连接酶, 购于Takara公司; 克隆载体使用pEASY-Uni Seamless Cloning and Assembly Kit(CU101)试剂盒、质粒抽提使用EasyPure Plasmid MiniPrep Kit试剂盒, 原核表达载体使用pEASY-Blunt Simple cloning Kit试剂盒, 胶回收使用 Gel Extraction Kit试剂盒, 分别购于北京全式金生物有限公司和北京康为世纪生物有限公司。大肠杆菌(Escherichia coli)DH5α 购于天根生化科技(北京)有限公司; 根癌农杆菌 (Agrobacterium tumefaciens) AGL1由本实验室保存; pMD18R-T vector载体购于Takara公司。其他试剂为国产分析纯级。
1.2.1 材料处理
将蒺藜苜蓿种子用酒精消毒后播种于铺有滤纸的培养皿中, 在光照培养箱(温度24 ℃, 光照12 h/d)培养至种子发芽, 将发芽种子用海绵条包裹种植移至盛有MS营养液的水培盘继续培养。20 d左右对幼苗开始处理, 胁迫处理时将水培溶液换成0.1 mol/L NaCl溶液、20%聚乙二醇(PEG)溶液和 1× 10-4 mol/L ABA溶液, 低温处理的水培溶液换成蒸馏水置于4 ℃冰箱, 分别处理0, 2, 6, 12, 24 h, 各时间点选取叶片组织置于2 mL离心管, 液氮速冻后贮于-80 ℃, 提取总RNA, 用于 Real-time PCR分析。组织特异性分析选取正常栽培条件下结荚期蒺藜苜蓿根、茎、叶、花、荚果。基因克隆选取开花期16 ℃放置48 h的蒺藜苜蓿叶片。
1.2.2 RNA提取及反转录
取蒺藜苜蓿叶片组织100 mg, 按照北京全式金TransZol Plus RNA Kit(ER501)试剂盒说明步骤提取总RNA[16]。利用紫外分光光度计测定RNA含量, 经琼脂糖凝胶电泳检验, 将质量合格的RNA在-80 ℃条件保存备用。cDNA第一链合成方法, 反应体系为:RNA 1 μ L, 5× TransScript All-in-One SuperMix for qPCR 4 μ L, gDNA Removal 1 μ L, RNase-free Water 14 μ L, 反转录反应体系总体积为20 μ L, 反应条件为:25 ℃ 10 min, 50 ℃ 30 min, 85 ℃ 5 min, 冰浴5 min, -20 ℃条件保存备用。
1.2.3 MtPUB4基因全长克隆及生物信息学分析
从Genbank中下载MtPUB4基因(登录号:XP_013460388.1)序列, 用Primer Premier 5.0和oligo 5.0软件设计并合成扩增引物F1/R1(表1), 以反转录cDNA第一链为模板, 进行PCR扩增。反应体系50 μ L, Template 1 μ L, Primer 各1 μ L, 5× TransStart Buffer 10 μ L, dNTPs 5 μ L; DNA Polymerase 1 μ L, ddH2O 31 μ L; 反应条件:预变性 95 ℃ 5 min; 95 ℃ 20 s, 55 ℃ 20 s, 72 ℃ 90 s, 35个循环; 延伸72 ℃ 10 min。将PCR扩增产物经凝胶电泳检测合格后胶回收。将胶回收纯化PCR产物, 用pMDR18-T载体4 ℃条件下连接过夜; 将连接产物转化至DH5α 感受态细胞, 冰浴30 min后, 42 ℃热激30 s, 加入LB培养基于37 ℃恒温摇床振荡培养过夜后, 置于含Amp+ 抗性的LB平板中进行筛选, 对所获得的单菌落培养后提取质粒、PCR扩增、用BamHI单酶切鉴定, 重复24次。对菌液进行PCR检测, 选择阳性菌液送北京英俊公司进行DNA测序。测定序列用DNAstar软件进行拼接分析, 得到正确的U-box基因核苷酸序列, 并进行氨基酸序列预测。
利用NCBI网站(http://ncbi.nlm.nih.gov/)ORF Finder和Conservd Domains程序分析核酸和氨基酸序列; 利用在Expasy网站查询(http://www.expasy.org/tools/)预测蛋白功能; 利用Genebank筛选下载其他植物的12种U-box蛋白同源序列, 在MEGA 5.0软件中选择邻近结合法(neighbor-joining)构建进化树, 分析MtPUB4编码的氨基酸序列物种进化关系[16]。
1.2.4 实时荧光定量PCR检测MtPUB4基因表达量
提取总RNA, 进行反转录合成cDNA第一链, 方法同1.2.2。使用Bio-Rad CFX96 实时定量PCR仪, 采用两步法进行Real-time PCR扩增。基因特异性引物F3/R3(表1), 内参基因选择蒺藜苜蓿ACTIN1, 引物F2/R2(表1)。反应条件:第一步 94 ℃预变性30 s; 第二步 94 ℃ 30 s, 58 ℃ 15 s, 72 ℃ 10 s, 共40个循环。每个样品3次重复。根据实验所得Ct值, 利用Livak等[17]报道的fold change=2-Δ Δ CT法, 计算蒺藜苜蓿MtPUB4基因在根、茎、叶、花、荚果中的表达量。把根的表达量设为对照, 茎、叶、花、荚果设为4个处理; 不同胁迫处理中, 把0 h表达量设为对照, 2, 6, 12, 24 h设为4个处理, 利用公式进行计算:
Δ Δ CT=(CT-gene-CT-actin)胁迫处理-(CT-gene-CT-actin)对照式中, CT表示循环阈值, CT-gene表示目标基因达到设定阈值的循环数, CT-actin表示Actin基因达到设定阈值的循环数, (CT-gene-CT-actin)胁迫处理表示处理样品中目标基因经Actin基因校正的循环次数; (CT-gene-CT-actin)对照表示对照样品中目标基因经Actin基因校正的循环次数; Δ Δ CT表示处理样品中目标基因和对照样品中目标基因循环次数的差值。然后再计算出2-Δ Δ CT的相对表达量, 根据计算所得结果绘制柱形图。
1.2.5 蛋白原核表达与鉴定
以蒺藜苜蓿cDNA为模板, 利用引物F4/R4(表1), 进行PCR扩增。取PCR胶回收产物和表达载体pEASY-Blunt Simple进行连接, 将连接产物全部转化Trans1-T1感受态细胞中, 接种SOC(super optimal broth)培养基培养, 涂于LB培养基(含50 μ g/mL Amp+)37 ℃过夜培养。次日挑取单菌落, 以引物F5/R5(表1)进行菌液PCR验证, 将合格菌液加入1 mL含Amp+抗生素的LB培养基37 ℃培养过夜, 提取合格质粒送公司测序。以构建好的亚克隆载体为模板, 进行PCR扩增目的片段, 引物使用F6/R6(表1), 胶回收PCR产物, 连接pEASY-Blunt E1载体, 转化Trans1-T1感受态细胞, 通过筛选阳性菌液、提取质粒、送交测序, 得到插入目的基因重组子pEASY-MtPUB4。
将阳性克隆菌液20 μ L接种至2 mL LB(含50 μ g/mL的Kan+和Amp+)培养基中37 ℃过夜培养。取30 μ L过夜培养菌液, 加入至3 mL LB培养基中, 37 ℃震荡培养至OD600约0.6; 取部分液体作为未诱导对照组, 余下的分别加入0.1, 0.2, 0.5, 1.0 mmol/L的 IPTG诱导剂作为实验组, 在37 ℃震荡培养。在诱导5 h时取菌体1 mL, 离心10000 r/min× 30 s 收获沉淀, 用100 μ L 1% 磷酸盐缓冲液PBS (phosphate buffer saline) 重悬, 混匀, 100 ℃ 10 min。10000 r/min离心10 min, 取上清进行SDS-PAGE分析。
1.2.6 植物表达载体构建
以克隆测序后的质粒为模板, 使用TransStartKD Plus DNA Polymerase聚合酶, 通过PCR扩增目的片段, 以酶切鉴定引物F7/R7(表1), 用内切限制酶BamHI, 对克隆载体pMD18-T::Mtpub4进行单酶切。酶切体系共200 μ L, 质粒120 μ L, 限制性内切酶4 μ L, 10× CutSmart Buffer 20 μ L, ddH2O补足至200 μ L。提取单酶切表达载体质粒, 取纯化目的基因PCR产物和pBI121载体, 用pEASY-Uni Seamless Cloning and Assembly Kit (CU101)连接酶连接, 将连接体系置于25 ℃连接2 h; 连接体系共10 μ L, 其中载体3.75 μ L, 目的片段1.25 μ L, 2× Assembly Mix 5 μ L。对于酶切后的表达载体质粒, 取纯化目的产物, 用T4 DNA Ligase连接酶与pBI121载体连接, 将连接体系置于25 ℃连接2 h; 连接体系10 μ L, 其中载体3.0 μ L, 目的片段4 μ L, T4 DNA Ligase 1 μ L, 5× T4 DNA Ligase Buffer 2 μ L。将质粒连接产物转化至DH5α 感受态细胞, 冰浴30 min后, 42 ℃ 热激30 s, 加入400 μ L LB于37 ℃恒温摇床振荡培养, 涂于含Kan+ 抗性的LB平板上, 37 ℃过夜培养; 次日挑取单克隆, 进行菌落PCR鉴定; 取鉴定合格菌液, 加2 mL至含Kan+抗性的LB培养基中, 37 ℃, 200 r/min转速摇菌过夜, 使用EasyPure Plasmid Mini Prep Kit试剂盒提取质粒; 将质粒进行酶切鉴定, 反应条件为25 ℃ 1 h, 37 ℃ 1 h。取鉴定合格菌液, 送北京英骏公司测序。
| 表1 引物信息 Table 1 Primers information |
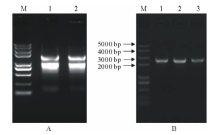
取蒺藜苜蓿叶片提取总RNA, 凝胶电泳检测显示有28S、18S两个条带, 说明RNA较完整。用紫外分光光度计检测, A260/A280值为1.877; A260/A230值为2.054, 说明RNA质量较好(图1A)。将提取RNA反转录合成cDNA第一链; 以cDNA第一链为模板, 以基因特异性引物进行PCR扩增目的片段(图1B), 利用DNAMAN拼接后的全长cDNA为2448 bp。将该基因命名为MtPUB4, NCBI登录号为XP_013460388.1。
2.2.1 保守结构域
运用Expasy网站SMART程序对MtPUB4基因编码的蛋白结构域分析, 结果显示MtPUB4蛋白215~278位氨基酸具有U-box/AEM家族所具备的典型U-box结构, 515~764位氨基酸具有典型的ARM重复结构, 该基因属于U-box家族的一员, 其编码的U-box保守氨基酸序列为FCCPLSLELMTDPVIVASGQTYERAFIKNWIDLGLT VCPKTHQTLAHTNLIPNYTVKALIANW。运用NCBI保守域在线分析, 该蛋白氨基酸序列C端存在U-box结构域, 修饰RING锌指结构, 没有Zn2+结合配体, 蛋白N端存在ARM重复结构, 最末端是谷氨酰胺, 可能参与E3泛素化。与其他物种U-box蛋白序列多重比对结果表明, U-box/ARM结构区域保守性较强, 有127个氨基酸完全一致(图2)。
 | 图2 MtPUB4与其他植物U-box蛋白氨基酸保守区序列多重对比分析Cicer arietinum:鹰嘴豆; Glycine soja:野大豆; Glycine max:大豆; Phaseolus vulgaris:菜豆; Theobroma cacao:可可; Gossypium arboreum:木本棉; Cucumis sativus:黄瓜; Nicotiana tabacum:烟草; Brassica oleracea:甘蓝; Arabidopsis thaliana:拟南芥; Oryza sativa:水稻。Consensus 表示序列一致性, 黑色表示100%相同, 粉色表示75%相同, 蓝色表示50%相同。Consensus indicates same sequences and are listed below; Black indicates 100% identity; Pink indicates 75% identity; Blue indicates 50% identity.Fig.2 Multiple alignment analysis of MtPUB4 conserved domain with its homologous in other plants |
 | 图2 MtPUB4与其他植物U-box蛋白氨基酸保守区序列多重对比分析Cicer arietinum:鹰嘴豆; Glycine soja:野大豆; Glycine max:大豆; Phaseolus vulgaris:菜豆; Theobroma cacao:可可; Gossypium arboreum:木本棉; Cucumis sativus:黄瓜; Nicotiana tabacum:烟草; Brassica oleracea:甘蓝; Arabidopsis thaliana:拟南芥; Oryza sativa:水稻。Consensus 表示序列一致性, 黑色表示100%相同, 粉色表示75%相同, 蓝色表示50%相同。Consensus indicates same sequences and are listed below; Black indicates 100% identity; Pink indicates 75% identity; Blue indicates 50% identity.Fig.2 Multiple alignment analysis of MtPUB4 conserved domain with its homologous in other plants |
2.2.2 系统进化
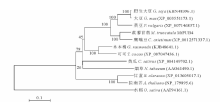
将克隆序列提交NCBI网站BLAST程序进行比对, 选取同源性较高不同物种序列下载, 利用MEGA 5.0软件邻近法程序构建系统进化树[12]。根据图3显示结果, 克隆序列蒺藜苜蓿MtPUB4与鹰嘴豆(C. arietinum)(XP_0012571337.1)同源性最高, 为89%; 与野生大豆(G. soja)(KHN48396.1)和大豆(G. max)(XP_003551173.1)、菜豆(P. vulgaris)(XP_007146857.1)同源性次之, 都是81%; 与其他科属植物可可(T. cacao)(XP_007047436.1)、木本棉(G. raimondii)(KJB48641.1)、黄瓜(C. sativus)(XP_004149702.1)、烟草(N. tabacum)(AAO61490.1)、甘蓝(B. oleracea)(XP_013605017.1)、拟南芥(A. thaliana)(NP_179895.6)和水稻(O. sativa)(AAT94161.1)等植物同源性较低, 分别是71%, 69%, 65%, 58%, 56%, 56%和54%。
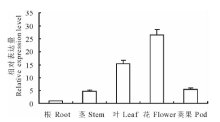
蒺藜苜蓿MtPUB4基因在不同组织中的相对表达量见图4。结果表明, MtPUB4在花中表达量最多, 其次是叶, 根中表达量最少。以蒺藜苜蓿根中MtPUB4基因表达量为对照, 花中表达量是根中表达量的26.68倍, 叶中表达量是根中15.45倍, 荚果中表达量是根中的5.60倍, 茎中表达量是根中的4.82倍。
蒺藜苜蓿MtPUB4基因分别受到NaCl、PEG、ABA和低温诱导0, 2, 6, 12, 24 h的相对表达量见图5。结果显示, MtPUB4基因在NaCl胁迫诱导下, 6 h时迅速上升, 是2 h时表达量的3倍, 12 h时达到峰值, 24 h下降(图5A)。在PEG胁迫诱导下2 h以内变化较小, 6 h表达量增到2 h的4倍, 达到峰值, 与NaCl胁迫下变化近似, 但是12 h时开始下降, 24 h时表达量低于0 h时表达量(图5B)。在低温处理后, 2 h时表达量稍微有所下降, 6 h时表达量与2 h表达量接近, 12 h时持续下降, 24 h时恢复至6 h水平(图5C)。在ABA诱导12 h后, 表达量稍有降低, 随后迅速上升, 24 h时表达量接近0 h的5倍(图5D)。除了低温胁迫MtPUB4基因表达量变化稍有降低, 表达量变化不明显外, 其余3种处理方式表达量都出现数倍上升, 这说明MtPUB4基因对盐、干旱和ABA胁迫响应, 可能参与这些逆境的信号调控。
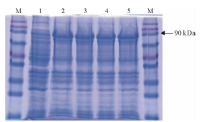
将目的片段连接pEASY-Blunt Simple载体, 转化至大肠杆菌BL21(DE3), 经测序验证序列正确, 表明蛋白表达载体构建成功。将含有阳性质粒的大肠杆菌表达菌BL21(DE3)pLysS Chemically Competent Cell株系, 用不同浓度的IPTG诱导表达, 上样浓度为0.1, 0.2, 0.5和1.0 mmol/L。结果显示, 含有MtPUB4片段的表达载体菌体在诱导后出现特异性条带, 各个浓度对蛋白表达影响不明显。该蛋白在90 kDa条带处, 与预期结果88.36 kDa相符(图6)。说明该蛋白在大肠杆菌中成功诱导, 可用于进一步蛋白表达研究。
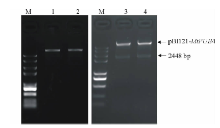
将植物表达载体pBI121和克隆载体分别酶切, 回收相应片段纯化连接、转化、挑取单菌落、提取质粒, 构建MtPUB4基因植物表达载体。经过BamHI酶切鉴定, 得到与预期大小一致的目的片段(图7)。鉴定为阳性的质粒送公司测序后拼接, 与基因序列一致, 说明成功构建植物表达pBI121-MtPUB4。
U-box E3泛素连接酶基因在植物生长发育和抗逆过程中起着重要作用。目前E3 泛素连接酶U-box的研究主要集中在拟南芥、水稻、烟草等模式植物中。本研究得到的蒺藜苜蓿MtPUB4基因的氨基酸序列中(图3), 在C端存在Ring super family U-box结构域, 有Zn指结构40个残基结合2个Zn原子, 由半胱氨酸和组氨酸组成, 可能参与蛋白质与蛋白质之间的相互反应, Hatakeyama等[8]认为这类蛋白与序列复制、信号传导和发育有关; 在N端有连续5个ARM重复结构, 末端是谷氨酰胺, 推测参与E3泛素化。有学者认为ARM结构域蛋白质在植物生长发育和激素应答等方面起重要作用[9, 18]。在某些植物U-box蛋白中, 如拟南芥中ARC1(Arm Repeat Containing 1), 其C端含有一个6~7个ARM重复结构功能域, 中间含有一个U-box功能域, 是SRK激酶下游信号的传递因子, 能在柱头乳突细胞中特异性表达, 能促进花粉水合、萌发和花粉管生长的雌性亲和因子[19]。在水稻中发现的SPL11[20, 21, 22]、烟草中的ACER276[23]、拟南芥中的AtPUB17等U-box基因都与植物抗病性有关[24]; 马铃薯(Solanum tuberosum)中发现的U-box基因PHOR1(photoperiod-responsive1)参与GA信号转导, 是GA信号转导途径中的正调控因子[25]; 烟草中的NtPUB4参与了植物发育和细胞分裂素信号转导[26]; 拟南芥AtPUB4的U-box/ARM功能域缺失能使绒毡层结构肥大最终导致植物雄性不育[3]; 蒺藜苜蓿中未见报道。通过构建系统进化树结果表明, 它们与同科属植物同源性很高, 和其他科属的植物同源性较低, 这与其他学者在其他物种间同源性分析结论基本一致[16, 27], 说明同源关系较近的植物中基因保守性更强。依据属内同源性较高的理论, 说明U-box/ARM蛋白家族基因进化上也比较保守, 其氨基酸序列相似度可在一定程度上说明了不同物种亲缘关系远近, 本研究中的蒺藜苜蓿MtPUB4基因与拟南芥AtPUB4基因、烟草NtPUB4的同源性较低, 但是在同一类型进化枝上, 这可能与拟南芥与烟草基因组较小有关系。
前人研究表明U-box E3连接酶可调控植物多个生理代谢途径, Samuel等[28]研究发现, 拟南芥中的U-box/ARM蛋白家族与拟南芥SD1受体蛋白激酶亚家族相互结合, 通过酵母双杂交实验表明, 两个受体结合可使U-box/ARM蛋白的ARM功能域磷酸化, 从而参与调控植物生理过程。Kim等[26]研究认为, 烟草的NtPUB4参与CHRK1介导的植物发育及细胞分裂素信号转导过程。据报道, CHRK1是烟草内的一种新型类受体激酶, 参与调控发育信号转导及内源细胞分裂素平衡, 且NtPUB4在烟草的花器官大量表达, 在苗、根、茎、叶中少量表达。本研究中, 蒺藜苜蓿Mtpub4基因也在花中大量表达, 与NtPUB4、ARC1有相似的结构域, 因此推测它们具有相似的功能。而CHRK1与SRK类受体激酶聚类在一起, 推测NtPUB4与ARC1功能相似[26]。Samuel等[28]在拟南芥中研究发现, 一些U-box/ARM基因受到NaCl胁迫诱导表达, 基因表达量会上调。以上结果表明U-box基因在抗性方面也可能发挥作用。本实验增加了干旱、低温和ABA诱导方面的研究, 通过模拟各种胁迫条件, MtPUB4基因在受到NaCl、PEG和ABA胁迫诱导后, 基因表达量都数倍提高, 此基因在NaCl、PEG和ABA胁迫反应中也可能参与调控反应, 但在低温胁迫中, 表达量稍微下降, 变化不明显。
雄性不育与一些基因突变有关, 产生这些基因突变的主要原因包括光周期、光强度、湿度和温度等环境因素的改变。目前, 利用这种现象人工筛选突变体, 通过两系配套法培育不育系已在杂交作物的生产上成功应用[29]。在拟南芥中, 突变体Atpub4在16 ℃中可恢复部分育性, 主要是花粉囊中的花粉粒可成功授粉。目前尚无蒺藜苜蓿U-box E3泛素连接酶蛋白的相关研究[30], 我们通过全基因组U-box结构域分析得出, 蒺藜苜蓿MtPUB32可能与ARK2共同调控植株侧根发育, MtPUB26可能与干旱胁迫相关[12]。通过对克隆蒺藜苜蓿MtPUB4序列分析, 得出它与拟南芥AtPUB4蛋白间有共同保守域结构, 利用生物信息学相关软件分析基因序列特征、功能蛋白结构、基因进化关系, 发现克隆基因属于植物U-box家族成员, 具备1个U-box结构域和5个ARM重复结构。本研究为进一步了解U-box基因如何调控蒺藜苜蓿的生长发育, 以及如何参与逆境胁迫信号转导, 揭示植物生长发育过程中的一些机制提供理论基础。
本实验通过RT-PCR技术, 克隆了蒺藜苜蓿U-box E3泛素连接酶基因, 对其核苷酸、氨基酸序列对比分析, 检测相对表达量变化规律, 进行原核表达并提取了MtPUB4蛋白, 同时成功构建植物表达载体。为后期筛选蒺藜苜蓿雄性不育基因、将其转化至拟南芥Atpub4雄性不育突变体材料进行遗传互补提供了候选基因。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [2] |
|
| [5] |
|
| [10] |
|
| [12] |
|
| [15] |
|
| [16] |
|
| [27] |
|