作者简介:谢开云(1984-),男,甘肃武威人,副教授,博士。E-mail: xkycah@163.com
混播草地中豆科牧草与禾本科牧草(简称豆/禾牧草)之间的氮转移在草地农业系统氮循环中具有重要作用。在豆科/禾本科牧草混播系统和豆科/禾谷类作物间作系统存在一种氮素共享的通道,即在间(混)作中,豆科植物固定大气中的氮在满足自身生长需求前提下,还通过各种途径为伴生的禾本科植物提供氮源。在混播草地中氮素转移途径主要分地上和地下两种。地上途径主要是豆科牧草的地上部分经放牧家畜采食后粪便归还土壤,后又被禾本科牧草吸收利用或者地上凋落物在土壤中经微生物分解矿化释放出有效氮被另一种植物吸收利用(反之亦成立)。地下途径相对复杂,可能有以下3种:1)通过植物根际沉积氮转移。2)通过菌根真菌的菌丝传递。3)通过植物根系分泌物中含氮化合物来转移。目前的研究虽然明确了有可能转移的途径,但哪一种途径是主要的方式?在氮素转移的过程中,某一途径会部分的发生,还是好几种途径同时发生,每一个途径的贡献为多少?这仍缺少关键的证据。本研究针对国内外关于豆/禾混播草地中豆科牧草生物固氮、豆/禾牧草间氮转移的研究现状,重点对混播草地中豆/禾牧草之间的氮素转移数量、转移途径及影响因素等方面进行了分析与总结,并对可能存在的氮素转移机理进行了综述,对今后的研究方向进行了展望,以期为下一步通过将豆科植物引入我国农牧业种植结构来实现农牧业可持续发展模式的研究提供理论资料。
Nitrogen transfer between legumes and grasses in mixed grass-legume swards plays an important role in the nitrogen cycle of grassland agricultural systems. There is a nitrogen-sharing pathway in legume-cereal intercropping systems and in grass-legume mixed swards whereby the legume plant not only meets its own nitrogen requirements for growth by way of fixed nitrogen from the atmosphere, but also provides nitrogen for the associated grasses through various pathways. The pathways of nitrogen transfer in mixed grass-legume swards can be categorized as above-ground or below-ground. The above-ground pathway occurs when herbage of legume plants is eaten by grazing animals and returned to the soil via excreta, then absorbed by other plants (including grasses), or when herbage litter falls to the ground and is decomposed and mineralized by microorganisms in soil to release plant-available nitrogen. The below-ground pathway is relatively complex and involves three routes: 1) Decomposition: decomposition of legume root tissues followed by uptake of released N by neighboring plants. 2) Mycorrhizae: transfer of N mediated by plant-associated mycorrhizae. 3) Root exudation: the exudation of soluble N compounds by donors and uptake by receivers. Although the current study identifies the possible routes of nitrogen transfer, many questions remain. Which is the main transfer route? What is the contribution of each route? To what extent can particular transfer routes operate concurrently? Such questions still lack key evidence. This paper briefly describes the current research status of biological nitrogen fixation of legume forages and of legume-grass nitrogen transfer in mixed grass-legume swards. A number of possible nitrogen transfer routes are reviewed, and directions for future research are identified. Better understanding of these questions will pave the way to achieve sustainable development of agriculture and animal husbandry in China, through realization of the potential benefits offered by legumes.
在农业(草地)生态系统中, 氮肥是维持生产力的必要条件, 在农业生产中被大量的应用, 但过量施用却造成严重的环境污染[1, 2]。从目前形势来看, 农业面源污染已成为我国粮食高产稳产的重要制约因素, 造成农业生产潜力下降, 严重影响到我国农业生产可持续性、农产品质量安全和国家生态环境安全, 成为我国社会经济可持续发展的重大障碍[3]。陈文新院士在第十一届全国土壤微生物学术讨论会上指出, 要解决目前我国农业面临的两个重大难题:一是化肥的大量施用引发了严重的农田面源污染, 导致作物增产对化肥的依赖性增强; 二是在现有种植体系下, 作物连作重茬引起的病虫害严重, 却只能大量使用化学农药来防治, 使得农业生产进入了恶性的循环, 唯一有效的途径就是调整产业结构, 将豆科植物纳入到间(套、轮、混)作体系中, 充分发挥豆科植物共生固氮的作用。与化学合成的氮肥相比, 豆科植物的生物固氮途径是一种绿色、可持续的氮源, 在陆地生态系统氮循环中扮演着重要角色, 也是未来实现农业可持续发展的重要资源。目前已有研究证明[4, 5, 6]:在豆科/禾本科牧草混播系统和豆科/禾谷类作物间作系统存在一种氮素共享的通道, 即在间(混)作中, 豆科植物固定大气中的氮在满足自身生长需求的前提下, 还通过各种途径为伴生的禾本科植物提供氮源; 在轮作中豆科植物通过特殊的氮素残留方式补充土壤氮库为后茬作物提供一定数量的氮[7, 8]。这种氮素共享的方式有效地避免了因为土壤有效氮供应和植物氮素需求之间在时间和空间上的不匹配所造成的氮损失[9]。
构建豆科植物参与的间(套、混、轮)作种植体系, 充分发挥豆科植物的生物固氮作用, 对于减少化学肥料的投入, 减轻农业生产对环境的负面影响, 保障粮食安全和农业可持续发展具有重要意义。当前该研究方向已成为世界范围内农业科学家、生态学家、政府部门关注的焦点。2016年中央一号文件明确提出了“ 探索实行耕地轮作休耕制度试点” 。2017年欧盟启动了一项由法国农业科学研究院(French National Institute for Agricultural Research, INRA)牵头组织13个欧盟国家参与的“ 基于间套混作重新设计欧洲的农作系统” 的研究与应用项目(https://www.remix-intercrops.eu)。这些都说明我国以及国外发达国家已经充分认识到间(套、混、轮)作在农业可持续发展中的重要性。这就迫切需要我们全面理解间(混、套、轮)作系统中豆科植物的生物固氮, 以及与禾本科植物(其他科)之间氮素转移机理以及相关研究进展。在此背景下, 本研究以豆/禾混播草地为切入点, 对豆科/禾本科牧草氮素转移机理及影响因素的研究进行了系统的总结和归纳, 并指出了在混播草地中豆科牧草和禾本科牧草之间氮素转移研究中存在的不足及未来研究方向, 以期为草地生态系统中氮循环领域的相关研究提供参考。
豆科植物与根瘤菌之间是一种互惠互利的“ 交易” 关系, 即根瘤菌将空气中的氮气转化成氨为豆科植物生长提供氮素, 而豆科植物则通过光合作用为根瘤菌提供碳水化合物。根瘤菌固定的氮素有94%供给它的寄主植物(豆科植物), 仅有6%供自己利用。这种独特的共生关系的建立首先始于由宿主植物在根际分泌类黄酮, 被具兼容性的根瘤菌识别, 并诱导根瘤菌产生的特异性的多糖信号分子脂壳寡糖(或称结瘤因子)[10], 根瘤菌进入根毛细胞并形成侵染线, 侵染线增长并伸入根的皮层, 与此同时皮层细胞进行有丝分裂, 产生根瘤原基, 侵染线继续增长和分枝, 伸入各原基细胞, 根瘤菌从侵染线中释放出来, 根瘤原基发育为根瘤。根瘤的形成不仅受生物因素的影响, 如根瘤菌和豆科植物的种类, 豆科植物光合作用强度和病原体的发生等[11], 也受到各种非生物因素影响, 如土壤湿度, 养分(有机质含量), pH值等。在豆科植物根系上形成的根瘤中, 并非所有的根瘤菌都可以固氮, 有效根瘤菌在利用豆科植物的碳水化合物的同时也为豆科植物提供氮素, 但无效根瘤菌并没有真正地固氮作用, 它占据了豆科植物中根瘤的位置, 利用了豆科植物的碳水化合物却不能为其提供氮素。豆科植物根系上形成根瘤的形状与豆科植物种类有关。如紫花苜蓿(Medicago sativa)形成细长的圆柱形或扇形根瘤[12]。根瘤的活性可通过其颜色来判断。一般幼小、活性较小的根瘤横切面呈白色, 活性较强的呈粉红色, 濒死或衰老的根瘤是绿色的, 无活性的根瘤呈棕色。
据报道, 豆科植物每年的固氮量为100~380 kg N· hm-2, 也有报道固氮量可达到500 kg N· h
大多数植物均依靠吸收土壤氮来满足生长需要, 但某些进化物种(最具代表性的是豆科植物)能够通过与根瘤菌的共生关系来获得氮源(即生物固氮)。豆科植物的生物固氮不仅可以满足自己生长需要, 而且还可以为伴生/后茬作物提供氮素, 这一现象广泛存在于豆科/禾本科混播草地[20]和豆科-禾谷类作物间作系统[21, 22]。大量的研究表明[4, 5, 6], 在豆科/禾本科混播系统中存在一种氮素共享的通道, 即豆科植物固定大气中的氮不仅可以满足自身的生长需求, 还可以通过各种途径为伴生的禾本科植物提供氮源; 在间作中, 固定的氮素被转移给伴生的作物; 在轮作中豆科植物通过直接的氮素残留方式或者增加土壤矿质氮库的氮量为后茬作物提供一定数量的氮[7, 8]。另外, 豆/禾植物间(混和轮)作系统中的氮素是双向迁移的, 既能从豆科植物到禾本科植物[23, 24], 也能从禾本科植物到豆科植物[25], 但是氮净转移倾向于从含氮较高(即豆类和其他固氮植物)的植物流向具有较高氮需求的植物(非固氮植物)[6]。
Vallis等[26]最先利用15N同位素标记技术证明了豆科与禾本科混播系统中发生了豆科牧草[矮柱花草(Stylosanthes humilis)]固定的氮向禾本科牧草[非洲虎尾草(Chloris gayana)]的转移。随后大量的研究者针对不同的研究对象利用不同的方法对于豆/禾牧草之间氮素转移量所占比例给出一个非常大的范围(0~80%)[27, 28, 29, 30]。如Stern[31]用15N同位素标记试验证实不同的间作系统中氮素转移量的大致范围每年为25~155 kg N· hm-2。有研究[32]评估了白三叶(Trifolium repens)和多年生黑麦草(Lolium perenne)混播草地氮素转移的量每年为11~113 kg N· hm-2, 平均值为70 kg N· hm-2。与根瘤菌固定的氮相比, 植物会优先吸收土壤中的无机态氮, 尤其是硝态氮, 因为从土壤中吸收氮的过程中消耗的能量较低[33]。前期室内的研究结果表明紫花苜蓿通过根瘤菌固定的氮素约占80%, 转移给禾本科牧草的氮素比例却低于30%, 这可能与土壤中无机氮含量高有关[18]。
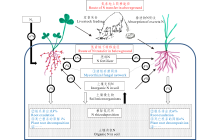
豆/禾混播草地中氮素转移主要分地上途径和地下途径(图1)。地上途径主要是豆科牧草的地上部分经放牧家畜采食后粪便归还土壤, 后又被禾本科牧草吸收利用或者地上凋落物在土壤中经微生物分解矿化释放出有效氮被另一种植物吸收利用(反之亦成立)。相比而言, 地下的氮素转移途径相对复杂。综合现有文献, 关于豆/禾混播草地中地下氮素转移的途径可能有以下3种(图1):
1)根际沉积氮(N rhizodeposition)。通过根、根瘤、根冠、根边缘细胞、脱落的细胞、表皮及凋落物在土壤中降解[4, 5, 34, 35]。根际沉积是指植物根系在生长过程中不断地向土壤中释放的有机与无机化合物。根际沉积在陆地生态系统作用的研究已有大量报道, 特别是根际沉积碳, 已经在沉积数量、方法、释放机制、影响因素等方面做了大量的研究[36, 37]。根际释放的有机物质通过影响植物的根际环境和根际微生物的利用转化, 影响植物-土壤间的氮循环过程。另外, 根际沉积氮是土壤微生物重要的营养元素来源, 也是联系植物-土壤-微生物的桥梁, 更是一种重要的植物与土壤间氮交换的界面过程。在有机农业或可持续种植的豆/禾混(间、套、轮)作系统中, 植物根际沉积氮被认为是系统氮高效利用的关键因素之一, 深入理解和认识根际沉积氮的流量和方向对于增加牧草产量及建立根际环境中氮的合理分配模式, 促进草地的可持续管理具有重要意义。
近年来在根际沉积氮方面的研究逐渐受到重视, 目前的研究表明植物根系释放了大量的氮, 占到了作物地下氮的绝大部分, 显著影响了农作系统氮素平衡。但关于根际沉积氮的数量和组成以及运转过程的研究依然十分有限, 尤其是在干旱区中低产田和低投入地区, 根际沉积氮的研究仍存在很多不足[38], 仅见少量研究[39, 40, 41, 42, 43]均集中在豆科作物, 比如豌豆(Pisum sativum), 禾本科作物, 如小麦(Triticum aestivum)和大麦(Hordeum vulgare)等[44, 45]。特别是从植物根系释放到土壤的机理依然没有可靠的依据。另外, 作物与牧草有本质的不同:a.豆科作物一般为一年生的, 多以收获籽实为目的, 而豆科牧草为多年生的, 一年可以收获多次, 多以收获营养体为目的。因此, 豆科牧草和豆科作物生长对氮素的需求量不同, 导致其在生长过程中根际沉积氮的数量和方式也不同。b. 作物间作时株距较大, 根系延伸的范围有限, 而豆科牧草与禾本科牧草混播时, 株距较小, 根系解除面积较大, 因此在混播中发生氮素转移的机理可能也不同。
2)菌丝传递。丛枝菌根真菌(arbuscular mycorrhizal fungi, AMF)在自然界中广泛存在, 能与绝大多数(70%~90%)的陆地高等植物形成共生体系[46], 是迄今发现的与植物关系最为密切的土壤微生物之一。目前人们对AMF从土壤吸收磷的分子基础和基因调控已经有了较为深刻的理解[47]。氮显然也是AMF通过侵染从土壤吸收后向植物根部输送的重要元素[48]。有研究报道在自然界丛枝菌根真菌可以定居在植物根系上并形成菌丝, 而AMF的根外菌丝(extraradical mycelium, ERM)可以从周围的环境中吸收利用硝态氮、铵态氮和氨基酸等, 并将不同来源的氮素运转至宿主植物[49]。
豆禾植物之间可以通过丛枝菌根真菌的菌丝相连并直接吸收和转移氮素[31, 50]。丛枝菌根真菌的存在可以促进豆科植物固定的氮转移到非豆科植物, 如白三叶草到多年生黑麦草[51], 埃及三叶草(Trifolium alexandrinum)到玉米(Zea mays)[52], 豌豆到大麦[50], 大豆(Glycine max)到玉米[53]和绿豆(Vigna radiate)到水稻(Oryza sativa)[54]。也有研究认为豆/禾牧草之间通过菌根真菌直接转移的氮非常有限[55]。从机制上讲, AMF促进植物间氮转移, 或者是通过在豆科植物和禾本科植物之间建立直接的菌丝连接[56, 57], 或者通过增加禾本科植物根系表面积进而增加吸收豆科植物释放氮的能力[56, 58]。AMF通过菌丝网络将氮从一植物转移至另一植物, 明显地提高了寄主植物利用不同来源氮的机会[59]。AMF可以直接吸收${NH_{4}}^{+}$、${NO_{3}}^{-}$和有机氮[60], 并且能从土壤有机物分解中获得大量的氮[61, 62]。另外AMF可以帮助植物有效拦截土壤中的氮[63, 64], 减少土壤中的氮损失[65, 66], 这表明在豆科/非豆科植物混合种植系统中, 豆科植物释放的氮可以被菌根有效地保持, 并随后转移到邻近的非豆科植物。通过菌根网络途径在豆科植物/非豆科植物混播系统中的氮转移是双向的[60, 67], 但大多数通过菌根真菌途径的氮转移是从固氮豆科植物到非固氮植物(达到80%), 也可以从非固氮植物转移到豆科植物(不到10%)[67], 这是因为在豆/禾植物之间通过菌根介导的氮转移主要通过源-库关系来驱动, 即氮净转移倾向于从含氮较高的豆类和其他固氮植物流向具有较高氮需求的非固氮植物[6]。
3)根系分泌物。第3种可能途径是通过含氮较丰富的豆科植物根系的渗出液间接的转移[68, 69, 70]。根系释放到根际周围土壤中的化合物被称为根系分泌物[71]。根系分泌物可以是低分子量化合物(如氨基酸, 有机酸, 糖, 酚类和各种其他次级代谢物)或高分子量化合物(如蛋白质)[71, 72, 73]。豆科植物根系渗出液中氨基盐和氨基酸是含氮化合物的主要组成成分[74], 这些化合物从植物根系向外渗透的过程是一个基于根系与土壤之间浓度梯度的被动扩散的过程[68]。根系分泌物被认为是豆禾混播草地中建植初期或早期氮素转移的主要方式[75]。如在建植不久的豆禾混播草地中, 黑麦草通过吸收白三叶根系渗出液被认为是主要的氮素转移方式[76], 剩余部分可经土壤微生物矿化后被临近植物吸收利用[77]。另外, 有研究[78]证明植物可以直接吸收有机氮(如氨基酸, 肽和蛋白质), 因此部分根系分泌物可被非豆科植物直接吸收。
在混播草地中从豆科牧草到非豆科牧草的氮转移在草地农业系统中发挥着非常重要作用。Trannin等[35]和Sierra等[79]认为与根系分泌物或菌根介导的N转移相比, 根瘤分解和根系分解转移途径更加重要。据估计, 豆科植物根系和根瘤分解转移氮素3~102 kg N· hm-2, 相当于生物固氮的2%~26%[32]。尽管不同植物通过3种途径转移氮素的贡献不同, 但与根分泌物和菌根介导的N转移途径相比, 根系和根瘤分解转移途径是一个缓慢的过程, 涉及较复杂有机化合物的分解和矿化。在时间尺度上, 第一种转移方式是长周期的, 主要是通过豆科植物死亡的根系和根瘤在土壤中经微生物作用后发生分解; 后两种转移方式是短周期的, 主要通过含氮的根分泌物和菌根网络连接后发生。从转移的途径来看, 第1种转移方式是间接的转移, 即氮从供体植物转移到接收植物要经过微生物矿化; 第2种转移方式是直接的转移, 即氮从供体植物转移到接收植物而不经过矿化; 第3种转移方式是直接途径还是间接途径, 主要取决于根系渗出物是被相邻植物直接吸收[80], 还是经过土壤微生物矿化后吸收[78]。
豆科牧草的生物固氮不仅受到生物因素的影响, 如牧草种类、品种基因型、生物量, 利用强度等, 还要受到非生物因素的影响, 如土壤pH值, 土壤湿度、土壤温度、土壤养分(特别是有效氮)、生长年限、农药、管理措施等[33]。其中最为主要的因素是土壤中有效氮的含量、水分和施用的农药。在混播草地中豆禾牧草发生氮素转移的前提是豆科植物通过生物固氮途径获得了大量的氮。因此氮转移除了受到以上因素的影响以外, 还要受植物根系的分布(特别是根系接触距离和面积), 植物生长密度, 生长阶段, 生长年限等因素的影响。
不同豆科牧草的物种特异性差异是影响生物固氮量及氮素转移差异的重要因素。Pirhofer-Walzl等[81]发现, 与红三叶(Trifolium pratense)(22 kg N· hm-2)或紫花苜蓿(11 kg N· hm-2)相比, 白三叶向邻近的植物转移了更多的氮(48 kg N· hm-2)。Frankow-Lindberg等[82]观察到白三叶(147 kg N· hm-2)比苜蓿(59 kg N· hm-2)转移了更多的氮。Louarn等[83]的试验也验证了相同的规律。与百脉根(Lotus corniculatus)和红三叶相比, 从白三叶向高羊茅(Festuca elata)转移了更多数量的氮[84]。在豆禾混播中不同的豆科牧草向邻近禾本科牧草转移氮素的差异可能是由于豆科牧草生长习性, 根系分布, 共生的根瘤菌种类, 根系分泌物强度, 死亡根系的分解速率以及菌根真菌的存在等因素。基于文献分析发现, 就白三叶和紫花苜蓿相比而言, 同等条件下白三叶向邻近禾草氮转移数量最大, 紫花苜蓿氮转移数量最小。可能的原因是:1)白三叶无性繁殖(匍匐茎)能力较强, 在生长中减少了根系内氮储存的需要, 将更多的氮用于向外转移[85]。2)白三叶主根短, 侧根和须根系发达, 细根低的C: N和低的木质素含量有利于在土壤中凋亡的根系分解、转化并释放出氮素[83]。相比之下, 苜蓿在其主根系中存储大量的氮以确保被刈割或放牧后的再生[83]。此外, 苜蓿主根发达而次生根系较小[81, 82, 83], 这进一步限制了在混播中与非豆科植物根系的密切接触面积。另外, 苜蓿具有较大的主根系, 根系C: N(> 20)和木质素含量较高, 限制了凋亡根系更新分解速率。以上因素都是造成苜蓿在混播中向邻近植物氮素转移量较小的原因。
从豆科牧草到禾本科牧草的氮转移也受到豆科牧草品种基因型的影响。Elgersma等[86]发现, 小叶型红三叶品种(87 kg N· hm-2)比大叶型白三叶品种(115 kg N· hm-2)转移更多氮。Thilakarathna[87]也报道了6个不同基因型红三叶品种与草地早熟禾(Poa pratensis)之间氮素转移也存在差异。Laidlaw等[88]基于4年的大田实验中观察到3种不同基因型白三叶品种与多年生黑麦草混播, 其中大叶型白三叶品种(15%)比小叶型白三叶品种(34%)转移的氮要少。并归纳了造成这种差异的主要原因为:1)大叶红三叶品种根和匍匐茎的腐烂、分解速率缓慢; 2)在混播中大叶红三叶品种与禾草对有效N的竞争激烈; 3)大叶和小叶红三叶品种在根系和根瘤形态上存在差异[89]; 4)与小叶品种相比, 大叶品种具有高的茎叶/根, 导致更多的N(可用于转移的直接N源)从根部转移到茎叶中[90]。混播草地中的非豆科成分也是影响氮转移的重要因素。如Marty等[91]研究报道了在混播草地中两种不同的禾本科牧草分别从三叶草接受的氮存在显著差异。同样, Sincik等[92]发现从白三叶转移到多年生黑麦草(73%), 草地早熟禾(50%)和匍匐剪股颖(Agrostis stolonifera)(48%)的氮存在着差异。禾本科植物的根系类型和分布在捕获来自豆科植物转移的氮素中具有重要作用, 一般来说与具有直根系的双子叶植物相比, 具有须根系的禾本科植物在捕获有效氮方面更有效[82]。除根系结构外, 禾本科植物的生物量大小、生长速率和与菌根相关性也可能是造成禾本科植物在吸收来自豆科植物转移氮素的差异的重要原因。
草地的利用强度(刈割和放牧)对豆禾混播草地的氮转移也具有重要影响。Tarui等[93]研究发现与混播草地中没有刈割处理相比(8 kg N· hm-2), 刈割处理下的多毛箭筈豌豆(Vicia villosa)(27 kg N· hm-2)转移到燕麦(Avena sativa)的氮增加了237%。草食动物对豆科牧草的选择性采食促进了向邻近非豆科植物的N转移, 这可能与被采食植物根系渗出液有关系。如Ayres等[94]和Dromph等[95]研究发现土壤动物对白三叶根系的采食直接增加了植物向土壤中含氮化合物的渗出, 进而增加了白三叶的氮素向邻近多年生黑麦草的转移。关于草食动物采食与植物根系渗出物之间的关系的研究大部分主要集中在植物根际碳沉积[96, 97], 并指出草食动物对植物的采食是通过增加了植物根际碳沉积提高了微生物的活性[98], 而增加了植物根际土壤有效氮[97, 99]。但也有研究认为草食动物对植物的采食可以直接影响植物根际氮的沉积, 进而提高了土壤氮的有效性。如Saj等[100]通过模拟昆虫采食研究混播草地中豆科牧草去叶处理对其氮素转移的影响, 结果表明去叶处理直接影响了豆科牧草向伴生禾草的氮转移, 而不是通过改变土壤有机碳来影响氮转移。
干旱是直接影响豆科牧草根系结瘤以及土壤中根瘤菌的存活率和固氮酶活性的重要的环境因素[101]。干旱胁迫降低豆科牧草的生物量和营养价值, 显著地降低了土壤中根瘤菌存活率以及豆科植物根系结瘤数[102], 进而严重削弱了豆科牧草的生物固氮能力[103], 导致豆科牧草增加了对土壤无机氮的吸收。重度干旱严重地损害了固氮酶活性, 可能的机制:1)在干旱条件下, 植物光合系统受损, 减弱或停止了向根瘤菌输送碳水化合物, 打破了原有的共生关系。2)缺少了豆科植物根瘤中豆血红蛋白(存在于豆类植物根瘤中在结构及功能上类似血红蛋白, 能与氧可逆地结合, 是豆科植物共生固氮所必需的含血红素蛋白质), 导致其固氮酶活性丧失[104]。另外, Marino等[105]研究证明豆科植物生物固氮对干旱胁迫的响应是局部的而非整株植物。干旱对植物和土壤中的氮素动态循环具有重要影响, 因此也成为氮转移的重要决定因素。在干旱条件下, 植物根细胞壁通透性通常会增加, 从而改变释放到土壤中的含氮化合物的数量和组成[74], 此外, 植物根系和根瘤衰老加剧[106], 导致土壤中有机氮含量增加。但是干旱的土壤环境也不利于土壤微生物的矿化作用[107]。另外, 干旱的土壤环境也不利于氮的运移, 限制邻近植物对氮的潜在吸收。
土壤有效氮的含量是影响豆科植物固氮及豆禾牧草之间氮素转移的重要因素。在豆科作物生产中发现大豆的固氮量与土壤有效氮呈显著的负相关关系[108]。在豆科牧草的草地中, 同样也发现土壤中高的无机氮含量显著降低了豆科牧草的固氮量[24, 109]。在混播中豆科植物的固氮量对土壤有效氮的响应是通过植物之间的竞争来实现的[110], 导致了在混播中豆科牧草的固氮效率比单一种植具有更高的固氮效率[18, 111]。但在豆/禾牧草混播草地中土壤有效氮对氮转移的影响仍存在着分歧。有研究认为[24, 87], 施入氮肥或较高的土壤无机氮含量有效地促进了混播草地中禾本科牧草的生长, 尤其是地上生物量的分布, 进而会促进豆禾牧草之间氮素的转移。也有研究认为[18], 较高的土壤有效氮抑制了豆科植物的生物固氮, 进而也会抑制豆禾牧草之间的氮素转移。总之, 在混播草地中可以通过土壤无机氮水平高低来调控豆/禾牧草的竞争, 即施入氮肥(土壤中高的有效氮)有利于禾本科牧草竞争力的提升, 进而抑制豆科牧草的生长及生物固氮[110](因为高的土壤有效氮不利于豆科牧草生物固氮, 但豆科牧草对土壤氮素的竞争要比禾本科牧草弱); 随着生育期的推进, 土壤中有效氮含量逐渐降低, 禾本科牧草失去了竞争优势, 而此时也有利于豆科牧草的生物固氮, 在混播草地中豆科牧草的竞争力提升。此外, 禾本科牧草的氮素需求部分也要依赖于豆科牧草氮素的转移, 这种依赖性的强弱也受到土壤中存在的有效氮的影响。
混播草地中的物种组成和密度也影响着豆科牧草向非豆科牧草的氮转移效率[21, 22, 24, 112]。通常, 在豆/禾混播草地中当豆科牧草所占比例大于禾本科牧草时, 氮素转移量相对较高, 如在不同的豆禾牧草混播草地中都观察到此现象, 包括苜蓿-百脉根-虉草(Phalaris arundinacea)[113], 白三叶-红三叶-百脉根-高羊茅[84]混播草地。在豆/禾作物间作系统中也发现同样的现象, 如大麦和豌豆以1: 1混播(转移氮占11%)要比2: 1混播(转移氮占4%)转移更多的氮素[21]。不同的豆/禾混播比例不仅影响了混播草地的牧草产量与品质, 群落结构和功能, 草地土壤中碳和氮的积累[114], 也影响了豆科牧草的生物固氮效率[115, 116], 以及氮素转移[81, 82]。当混播草地中豆科牧草所占比例较高时, 可以通过多种途径向土壤中输送有效氮, 更有利于邻近伴生禾本科牧草的吸收利用。相比而言, 在混播中豆科牧草/禾本科牧草比例越大, 越有利于豆/禾牧草间根系的接触, 菌根的连接, 根际沉积氮积累[117], 以及氮移动距离的缩短。豆科牧草和伴生禾本科牧草以1: 1混播种植时, 土壤全氮和土壤有效氮均显著提高[118]。因此, 在混播草地中可以通过增加豆科植物播种量或安排更窄的混播行间距等措施优化混播草地中豆科牧草与和禾本科草牧草的比例, 以提高混播中豆禾牧草之间的氮素转移。
在混播草地中豆禾牧草之间存在着对水分、养分、空间、光照等资源的竞争, 最终都通过牧草生物量以及草地物种的组成变化等指标表现出来。在混播草地中豆科植物和禾本科植物两个功能群之间的竞争关系也会影响豆科牧草的生物固氮及其氮素转移。其中, 豆科牧草的生物固氮受到伴生植物竞争的影响。豆科植物的生物固氮对提高混播草地中氮产量具有重要作用[115], 而非豆科牧草成分也起着关键作用, 因为它迅速耗尽了土壤中的有效氮, 间接地促进了伴生豆科牧草的生物固氮[18]。如Jorgensen等[119]报道在白三叶与多年生黑麦草混播中, 来自生物固氮的氮的比例为85%~97%, 而在白三叶草单播中固氮比例为75%~94%。Soon等[120]观察到, 经过4周杂草竞争的豌豆从大气中获得了81%的氮素, 而受到1周杂草竞争的豌豆只获得为51%的氮素。Wedin等[19]阐明相对于单播的豆科牧草, 豆/禾混播草地中豆科牧草较大的生物固氮量归因于来自非固氮植物对土壤氮的更大竞争。另外, 在混播草地中禾本科牧草的生长模式也会影响氮转移速率, 其中早熟和生长速率较大的牧草在吸收来自豆科牧草释放的氮时更有竞争力[121]。
豆科植物/非豆科植物根系的空间分布对于氮转移也具有重要影响。在混播中当豆禾牧草之间的根系越接近时, 氮素转移率趋于越高[57, 122, 123]。其机理在于:1)豆科植物和非豆科植物的根系紧密接触减少了含氮化合物在土壤中移动的距离。2)豆科植物的根际氮浓度在横向分布上越接近根际越高[124, 125]。在纵向分布上随着土壤深度增加而降低, 而大部分根际氮(95%)分布于表层土壤(0~15 cm)[126, 127]。另外, 豆科植物的根系结构也影响氮转移。如与其他饲用豆科植物相比(特别白三叶), 苜蓿具有较高的固氮能力, 但相关氮转移量却较低[81], 这可能与苜蓿深的主根和较少的次生根, 及相对较少的侧根限制了与邻近植物的密切接触有关[12]。
豆科牧草的生产年限(特别是多年生牧草)也显著影响其生物固氮以及氮转移。如Jorgensen等[119]发现在豆/禾混播草地系统中从白三叶到黑麦草的氮素转移在建植当年可以忽略不计, 但在建植第2和3年分别增加到19和28 kg N· hm-2。其他学者在白三叶和多年生黑麦草[24, 84, 87], 苜蓿和高羊茅[83]混播草地上研究证明了与建植当年或建植后第1年相比, 在建植后第2年以后的豆科牧草的氮转移量普遍较高。另外, Chapagain等[21]发现在豆禾作物间作系统中, 与第1年相比(氮素转移率6%), 第2年的豌豆到大麦的氮转移量增加(氮素转移率16%)。Chapagain等[22]在小麦-菜豆(Phaseolus vulgaris)间作(第2年和第1年分别为6%和3%), 小麦-蚕豆(Vicia faba)间作(第2年和第1年分别为13%和11%)系统中研究发现, 从豆科到禾本科的氮素转移在第2年与第1年略有提高。总的来说, 造成这种差异的原因可能是随着生长年限增加, 一方面豆科植物的生物量和固氮量增加, 另一方面, 豆科植物根系和根瘤组织的分解和矿化以及禾草对矿化氮的吸收增加[128]。另外, 在同一生长季内, 随着生育期的推进, 豆科牧草的生物固氮量和豆/禾牧草之间氮素转移也会增加。如Mallarino等[84]观察到随着生育期的推进, 豆科牧草到禾本科牧草氮素转移量从20%增加到60%。Dahlin等[129]观察到红三叶转移到多年生黑麦草的氮比例从第1次收获的10.1%增加到第3次收获的22.7%。同样, Thilakarathnar等[20]观察到在白三叶转移到草地早熟禾的氮比例从第1次收获时的7%增加到第3次收获时的26%。Zang等[130]对绿豆(Vigna radiata)-燕麦(Avena sativa)间作系统的研究也发现, 从绿豆到燕麦的N转移从荚果期(7.6%)到成熟期(9.7%)略有增加。
随着全球人们对有机农牧业(农牧场)兴趣提高, 环境友好的农牧业发展模式愈来愈受到重视, 而未来生物固氮以及氮素转移将成为大家持续关注和研究的热点。施肥或引入豆科植物均能提高多年生禾草草地生产力, 由于施用氮肥成本较高, 对环境也有风险。因此, 相比较而言引入具有固氮能力的豆科牧草是一种更为理想的方式。但是在实际的生产中, 往往受到各种因素的影响和制约, 使得豆科植物的生物固氮未发挥最大的效率, 氮素利用效率也相对较低。因此, 如何使豆科牧草保持较高的生物固氮效率, 调控和高效利用系统中的有效氮, 将有限的氮素尽可能多的转化为家畜能够利用的蛋白, 并在生产实践中提出有效措施来提高氮素利用效率对于实现农业的可持续发展具有重要意义。现有的研究已经阐明了间(混或轮)作的豆科植物和禾本科植物之间具有竞争和促进作用(氮转移), 但仍有很多研究空白需要填补。
1)豆科牧草生物固氮和豆禾之间转移氮素的数量和时间直接影响着混播中氮素效益, 也是氮素能否被高效利用的关键。现有的文献研究了豆科植物在单播或者混播中的固氮量, 氮素转移量以及影响因素, 但是豆科牧草的生物固氮发生的时间以及与禾本科牧草氮素转移的时间和数量到目前为止仍然不清楚。
2)在现有的研究中发现豆科植物生物固氮量较大而氮素转移量却十分有限, 目前的研究虽然明确了有可能的转移的途径, 但是哪一种途径是主要的方式?在转移氮素的过程中, 某一过程会部分的发生, 还是好几种情况同时发生, 每一个过程的贡献为多少?这需要进一步的研究明确。
3)作为“ 牧草之王” 的紫花苜蓿生物固氮时具有更大的能量需求, 同化作用和呼吸作用强烈, 根际沉积量也更大。其对土壤无机氮库的贡献有多大?在与禾本科牧草混播时氮素转移发生的机制是否同作物一致?这需要进一步研究。
4)当豆科牧草与不同禾本科牧草混播生长时, 倾向于固定不同量的氮素。因此, 可以通过研究豆/禾牧草之间氮素转移来识别兼容的豆/禾类物种, 为混播草地建植中选择更友好的物种类型提供理论依据。
5)在中国北方紫花苜蓿生产中, 生产者为了提高产量, 都存在不同程度的施氮肥的现象(在新疆干旱区尤为严重), 产量虽然提高了, 但固氮能力却被完全抑制了, 不仅增加了生产成本, 而且造成了严重的环境污染。作为紫花苜蓿主产区的北方是典型的半干旱、干旱区, 牧草生产必须依靠灌溉, 因此, 如何在满足紫花苜蓿正常生长发育的情况下, 有效提高植物养分的利用效率, 充分利用和发挥紫花苜蓿生物固氮的特性, 尽可能减少农业经济成本, 对干旱半干旱地区节约用水和农牧业可持续发展至关重要。大多数的研究都集中在如何提高紫花苜蓿的水分利用效率, 而如何在提高紫花苜蓿水分利用效率的同时提高其养分利用效率以及生产利率方面还未开始关注。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|
| [79] |
|
| [80] |
|
| [81] |
|
| [82] |
|
| [83] |
|
| [84] |
|
| [85] |
|
| [86] |
|
| [87] |
|
| [88] |
|
| [89] |
|
| [90] |
|
| [91] |
|
| [92] |
|
| [93] |
|
| [94] |
|
| [95] |
|
| [96] |
|
| [97] |
|
| [98] |
|
| [99] |
|
| [100] |
|
| [101] |
|
| [102] |
|
| [103] |
|
| [104] |
|
| [105] |
|
| [106] |
|
| [107] |
|
| [108] |
|
| [109] |
|
| [110] |
|
| [111] |
|
| [112] |
|
| [113] |
|
| [114] |
|
| [115] |
|
| [116] |
|
| [117] |
|
| [118] |
|
| [119] |
|
| [120] |
|
| [121] |
|
| [122] |
|
| [123] |
|
| [124] |
|
| [125] |
|
| [126] |
|
| [127] |
|
| [128] |
|
| [129] |
|
| [130] |
|