作者简介:王琼(1994-),女,甘肃民勤人,在读硕士。E-mail: qwang17@lzu.edu.cn
箭筈豌豆炭疽病是一类重要的真菌性病害。采用形态学特征观察结合基于内转录间隔区( ITS)、肌动蛋白( ACT)、几丁质酶( CHS1)和3 -磷酸甘油醛脱氢酶( GADPH) 4个基因序列的多基因系统发育分析方法来鉴定甘肃夏河箭筈豌豆炭疽病的病原菌。结果表明,菌株WQ在马铃薯葡萄糖琼脂(PDA)培养基上的菌落平坦,正面为深灰色-橄榄色至橄榄色-黑色,边缘菌丝白色,背面灰色-橄榄色至铁灰色。分生孢子单胞透明,大小为(17.5~25.0) μm×(3.75~5.00) μm,略呈镰刀形。菌株WQ与编号为CBS 128.57的菌株同源性最高,在70%水平上聚为一支。病原菌可以通过伤口侵染箭筈豌豆叶片。确定箭筈豌豆炭疽病病原菌为菠菜炭疽菌,这是箭筈豌豆菠菜炭疽菌在中国的首次报道。寄主范围测定结果表明,病原菌对红豆草和燕麦均具有强致病性,对4个品种的箭筈豌豆具有中等致病性,对苜蓿和三叶草的致病性最低,而对黑麦草无致病性。
Anthracnose in Vicia sativa is an important fungal disease affecting leaves and stems. This research combined morphological and multiple gene phylogenetic analyses, using gene sequences of an internal transcribed spacer region, actin, chitin synthase 1 and glyceraldehyde-3-phosphate dehydrogenase to identify an anthracnose pathogen (WQ) isolated from leaves and stems of vetch plants (cv. Lanjian No.2) in Xiahe County, Gansu Province. Koch’s postulates were applied to identify pathogenicity of the strains. It was found that colonies of the fungus on potato dextrose agar (PDA) were flat, with surface dark gray-olivaceous to olivaceous-black, white margin, covered by short floccose whitish aerial mycelium, reverse gray-olivaceous to iron-gray. Conidia were hyaline, unicellular, (17.5-25.0) μm×(3.75-5.00) μm, and slightly falcate. Multiple-gene phylogenetic analysis indicated that the isolate WQ and a strain of CBS 128.57 were clustered into one clade, with a confidence level of 70%. The strains (WQ) could infect V. sativa leaves through wounds. It was confirmed that the pathogen was Colletotrichum spinaciae. This is the first report of C. spinaciae on V. sativa in China. A host range test showed that C. spinaciae exhibited high pathogenicity to Onobrychis viciifolia and Avena sativa, and moderate pathogenicity to four V. sativa cultivars, and low pathogenicity to Medicago sativa and Trifolium repens. However, Colletotrichum spinaciae had no pathogenicity to Lolium multiflorum.
箭筈豌豆(Vicia sativa)为豆科野豌豆属一年生重要栽培品种[1, 2], 因其适应性广而广泛分布于世界五大洲温暖地区[3]。我国于20世纪40年代引进, 用于根茬肥地, 地上部青饲或晒制干草, 或留种子加工饲用或食用[4]。箭筈豌豆固氮能力强[5], 蛋白质含量高[6, 7], 适口性好[8], 也能改善土壤理化性状[9], 对后续作物具有增产作用[10, 11], 是我国草地农业系统中重要的豆科牧草及绿肥作物。2011-2015年, 兰州大学南志标院士团队针对我国高山草原地区缺少优良豆科牧草, 造成家畜生产力低下、死亡, 选育了兰箭1号, 兰箭2号和兰箭3号3个新品种, 可在海拔3000~4000 m的地区生长, 生产种子[12]。
在实际生产中, 箭筈豌豆的生长受到许多生物和非生物因素的胁迫, 其中病害一直是限制其优质高产的重要因素之一[13]。炭疽病是箭筈豌豆生产中一种普遍发生的真菌性病害[14]。箭筈豌豆炭疽病仅在美国和中国报道记载。美国学者Dearness[15]于1926年首次报道了由野豌豆刺盘孢(Colletotrichum viciae)引起的箭筈豌豆炭疽病。Horn[16]和Weimer[17]分别于1945和1952年报道了发生于美国由冬箭筈豌豆刺盘孢(Colletotrichum villosum)和苕子炭疽病菌(Colletotrichum sativum)引起的炭疽病。1959年, Sawada[18]记录了台湾发生的箭筈豌豆炭疽病, 病原为救荒野豌豆炭疽菌(Colletotrichum viciae-sativae)。我国学者对箭筈豌豆炭疽病的研究始于1984年, 刘若等[19]于吉林省发现了由野豌豆刺盘孢引起的箭筈豌豆炭疽病。2015年, Xu等[20]报道了发生于甘肃庆阳的箭筈豌豆炭疽病, 病原为小扁豆刺盘孢(Colletotrichum lentis), 植株发病率为100%, 30%的植株死亡, 造成箭筈豌豆品质的下降和损失[21]。
本研究于2018年7月在甘肃省夏河县山塘村兰箭2号上发现炭疽病, 主要危害植株叶部、茎部和荚果, 严重时造成叶片枯死进而植株死亡。因此, 为明确夏河箭筈豌豆炭疽病病原菌的分类地位, 采集了病株进行常规分离, 并对病原菌形态、致病性、分子生物学及寄主范围等进行了研究, 为病害综合防控提供理论依据。
2018年开展甘肃夏河箭筈豌豆炭疽病调查工作, 调查面积为667 m2以上的样地, 每田人为划分为面积相等的3块, 每块调查5个点, 每点调查10株。统计发生主要病害的株数及叶片数, 以此计算植株发病率和病情指数[22]。采集具有典型症状的茎、叶进行症状描述。分离病原菌的方法为组织分离法:将叶片和茎秆的病健交界处切成5 mm× 5 mm的小块, 先放在75%酒精中30 s, 然后5%次氯酸钠消毒2 min, 再用无菌水冲洗5次。置于马铃薯葡萄糖琼脂(potato dextrose agar, PDA)培养基上25 ℃黑暗培养, 长出菌丝后进行纯化[23]。根据箭筈豌豆叶片病斑占叶面积的百分比对箭筈豌豆叶片进行病害分级, 标准如下[21]:代表值0(1级):无病斑; 代表值1(2级):病斑占叶面积1%~10%; 代表值2(3级):病斑占叶面积11%~25%; 代表值3(4级):病斑占叶面积26%~50%; 代表值4(5级):病斑占叶面积51%~75%; 代表值5(6级):病斑占叶面积76%~100%。
发病率=(病株数/调查总株数)× 100%
致病性测定试验在兰州大学草地农业科技学院智能温室进行。选取健康饱满的箭筈豌豆(兰箭2号)种子200粒, 分别经75%酒精处理3 min, 1%次氯酸钠消毒10 min, 再用无菌水冲洗5次后均匀摆放于铺有灭菌滤纸的无菌培养皿(直径90 mm)中, 滴加5 mL无菌水, 每天注意加水保湿。在恒温培养箱里黑暗培养72 h后, 挑选无污染的幼苗用于试验。盆栽用土先过筛(孔径2 mm)剔除杂物, 平铺在瓷盘上约3 cm厚, 将瓷盘放置在烘箱中, 169 ℃下灭菌2 h, 降温后装在塑料大桶中, 盖上桶盖备用。每次称取灭菌土壤1000 g, 装在15 cm(上口径)× 11 cm(下口径)× 14 cm(高)、底部铺两层滤纸的塑料花盆中用以种植植物。将箭筈豌豆幼苗移栽于花盆中, 每盆8株。采用涂抹刺伤法(TS)、涂抹非刺伤法(TF)、喷雾刺伤法(PS)和喷雾非刺伤法(PF)4种接种方法, 将配制好的1× 106个· mL-1孢子悬浮液接种到12盆箭筈豌豆植株上, 每盆接种量为200 mL, 并用接无菌水作为对照[21], 共16盆。黑暗保湿48 h。接种3、7和14 d后调查植株的发病情况。调查方法如1.1。
1.3.1 形态学鉴定 培养25 d后, 观察菌落的正、反面颜色及边缘形状。记录分生孢子特征并拍照, 同时测定50个分生孢子的大小。
1.3.2 分子生物学鉴定 病原菌在25 ℃下PDA培养基黑暗培养25 d后, 刮取菌丝体置于研钵中, 采用真菌DNA提取试剂盒(上海生物工程有限公司)提取病原菌DNA, 再利用内转录间隔区序列(ITS)、肌动蛋白(ACT)、几丁质酶(CHS1)和3-磷酸甘油醛脱氢酶(GADPH)引物进行PCR扩增[24, 25](表1)。PCR扩增为25.0 μ L体系:1.5 μ L模板DNA, 上下游引物各1.0 μ L, 12.5 μ L Eco taq mixture, 9.0 μ L dd H2O。反应条件为:94 ℃ 5 min; 94 ℃ 30 s, 55 ℃ 30 s, 72 ℃ 1 min, 35个循环; 72 ℃ 10 min[21]。将测序后的各基因序列提交至GenBank数据库获得序列号, 并下载模式炭疽菌的相应基因序列[26](表2)。按ITS-ACT-CHS1-GAPDH的连接顺序将所有供试菌株各基因首尾相连。使用MEGA 6.0软件构建系统发育树。
| 表1 扩增箭筈豌豆炭疽病菌不同序列所用的引物 Table 1 Primer sets and corresponding amplification targets |
| 表2 GenBank供试基因序列 Table 2 Test gene sequence in GenBank |
供试寄主植物为兰箭1号(V. sativa cv. Lanjian No.1)、兰箭2号(V. sativa cv. Lanjian No.2)、兰箭3号(V. sativa cv. Lanjian No.3)、333/4(V. sativa cv. 333/A)、苜蓿(Medicago sativa)、红豆草(Onobrychis viciifolia)、三叶草(Trifolium repens)、燕麦(Avena sativa)和黑麦草(Lolium multiflorum)。每种植物种植8盆, 每盆种植5株, 分为接菠菜炭疽菌(P+)和不接菌(P-)处理, 4次重复。采用致病性测定试验中效果较好的方法进行接种。接种14 d后测定植株发病率、病情指数、株高、根长和生物量(地上鲜重、干重; 地下鲜重、干重)等指标。采用直尺直接测量法测定株高、根长。采用电子天平测量(BSA224S-CW)测定生物量。
采用Excel 2007处理数据, 利用 SPSS 20.0软件进行方差分析, 用最小显著差法(LSD)进行显著性检验, 并利用GraphPad Prism 5.01软件绘图。
箭筈豌豆炭疽病于7月中旬开始发生, 病情指数为8.45; 8月中旬达到高峰期, 发病率为56.3%, 病情指数为15.88。主要危害箭筈豌豆叶片和茎秆, 发病初期, 在叶片和茎秆上出现圆形、椭圆形的黑褐色小斑点, 后期扩展为黑褐色圆形病斑, 病斑中央则由黑褐色变为灰白色。病斑上产生轮纹状的小黑点, 病斑可形成穿孔, 病叶易脱落。发病严重时大量植株变黄最后枯死(图1)。
将分离得到的代表菌株(编号为WQ)作为供试菌株进行致病性测定试验。采用涂抹刺伤法(TS)、涂抹非刺伤法(TF)、喷雾刺伤法(PS)和喷雾非刺伤法(PF)4种方法接种, 试验结果表明, 4种方法接种后均可发病, 发病率为16.7%~79.2%, 对照未发病。其中接种效果最好的方法是喷雾刺伤法, 发病率为29.2%~79.2%(图2a), 病情指数为8.0~34.3(图2b)。接种14 d后, 采用喷雾刺伤法的发病率为79.2%, 相比涂抹刺伤法, 涂抹非刺伤法和喷雾非刺伤法分别提高了15.8%, 10.6%和15.8%; 其病情指数为34.3, 相比其他3种方法分别提高了40.8%, 42.6%和8.8%。接种3 d后观察到叶片上出现小黑点, 严重时黑点遍布整个叶片, 然后小点不断扩展成黑色圆形或椭圆形病斑, 中间为灰白色(图3)。发病症状与田间症状相似, 从病叶上重新分离出与接种菌种形态特征一致的病原菌。
2.3.1 形态学鉴定 PDA培养基上的菌落平坦, 正面为深灰色-橄榄色至橄榄色-黑色, 边缘菌丝白色, 由短的絮状白色气生菌丝体覆盖, 黏附水珠, 背面灰色-橄榄色至铁灰色(图4a, b)。菌落生长速度慢, PDA培养基上25 ℃黑暗培养10 d, 直径为26.45 mm。分生孢子透明, 单细胞, 大小为(17.5~25.0) μ m× (3.75~5.00) μ m, 略呈镰刀形(图4c, d)。与Damm等[26]、Kurt等[27]和杨佳文等[28]对菠菜炭疽菌形态特征的描述相似。
 | 图4 箭筈豌豆炭疽病菌在PDA培养基上的形态学特征 a, b: 在PDA上的菌落特征; c, d: 分生孢子特征。Fig.4 Morphological features of pathogen on PDA a, b: Upper colony morphology on PDA; c, d: Conidia. |
2.3.2 分子生物学鉴定 将菌株WQ的ITS、ACT、CHS1和GAPDH基因序列上传至GenBank数据库, 得到的登录号为MK402144、MK387713、MK387714和MK387715。BLAST后发现菌株CHS1和GAPDH基因序列与登录号为GU228337.1和GU228239.1的菠菜炭疽菌相似性达100%, ITS基因序列与登录号为GU227847.1菠菜炭疽菌的相似性达99%, ACT基因序列与登录号为GU227945.1菠菜炭疽菌的相似性达98%。系统发育树分析结果表明, 菌株WQ与编号为CBS 128.57菠菜炭疽菌同源性最高, 在70%水平上聚为一支(图5)。结合箭筈豌豆炭疽病病原菌形态特征, 根据多基因序列分析结果, 将箭筈豌豆炭疽病病原菌确定为菠菜炭疽菌。
2.4.1 发病率、病情指数及致病性 采用喷雾刺伤法对6种供试植物接种试验, 14 d后调查发现菠菜炭疽菌可侵染箭筈豌豆(兰箭1号、兰箭2号、兰箭3号和333/A)、苜蓿、红豆草、三叶草和燕麦, 不能侵染黑麦草。除了黑麦草之外所有植株叶片均出现了不同程度的炭疽病症状。发病率最高的为燕麦, 达87.5%, 其次是红豆草。苜蓿的发病率最低, 为18.6%。箭筈豌豆的发病率为40.6%~53.1%。菠菜炭疽菌对红豆草和燕麦均具有强致病性, 对4个品种的箭筈豌豆具有中等致病性, 对苜蓿和三叶草的致病性最低, 而对黑麦草无致病性。病原菌侵染4个品种箭筈豌豆的病情指数分别为10.8、10.0、7.2和11.0, 三叶草的病情指数较低, 为3.0, 而苜蓿的病情指数最低, 为1.5(表3)。
| 表3 菠菜炭疽菌的寄主范围测定 Table 3 Host range of C. spinaciae |
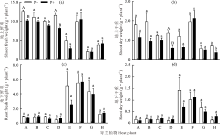
2.4.2 生长指标 试验结果表明, 接种菠菜炭疽菌(P+)后, 兰箭1号、兰箭2号、兰箭3号、红豆草和燕麦的株高均显著低于未接菌处理(P-)植株(P< 0.05)。接菌处理下, 333/A的株高较对照降低了17.2%(P< 0.01), 而苜蓿和三叶草的株高在接菌和不接菌下无显著差异(P> 0.05)(图6a)。兰箭1号和燕麦的根长在接菌和不接菌下存在显著性差异(P< 0.05), 接菌后分别降低了27.2%和42.5%。兰箭2号和兰箭3号植株受到菠菜炭疽菌侵染后, 其根长均极显著降低(P< 0.01), 而其他寄主植物的根长并未受显著影响(P> 0.05)(图6b)。
2.4.3 生物量 菠菜炭疽菌影响了供试寄主植物的地上鲜重和地上干重, 而对地下鲜重和地下干重没有影响(图7)。其中, 兰箭1号和333/A的地上鲜重在菠菜炭疽菌侵染和对照两种处理下存在极显著差异(P< 0.01), 接菌后分别降低了19.5%和29.7%; 菠菜炭疽菌侵染兰箭3号后, 其地上鲜重显著低于健康植株, 而其他植物在接菌和不接菌处理下的地上鲜重均无显著差异(P> 0.05)(图7a)。 接种菠菜炭疽菌后燕麦和333/A地上干重分别降低了55.3%(P< 0.05)和56.3%(P< 0.01)(图7b)。综合可知菠菜炭疽菌在很大程度上影响了333/A的地上生物量。
本研究通过形态学鉴定、多基因联合分析及致病性测定, 将分离自甘肃夏河县箭筈豌豆的炭疽菌鉴定为菠菜炭疽菌。这是箭筈豌豆菠菜炭疽菌在中国的首次报道。炭疽菌属(Colletotrichum)真菌主要分布在热带和亚热带地区, 可引起多种草本植物和木本植物的炭疽病, 寄主范围十分广泛[29]。引起箭筈豌豆炭疽病的病原有野豌豆刺盘孢[15]、苕子炭疽病菌[16]、冬箭筈豌豆刺盘孢[17]、救荒野豌豆炭疽菌[18]、野豌豆刺盘孢[19]和小扁豆刺盘孢[20, 21]。其中我国报道的箭筈豌豆炭疽病病原菌有救荒野豌豆炭疽菌、野豌豆刺盘孢和小扁豆刺盘孢, 小扁豆刺盘孢是侵染兰箭3号的病原菌。菠菜炭疽菌被认为是黑线炭疽菌的小变种, 与葱刺盘孢(Colletotrichum circinans)的亲缘关系最近[26]。该病原菌多侵染菠菜(Spinacia oleracea)和甜菜(Beta vulgaris), 分别造成其产量50%和20%的损失[30, 31]。加拿大[32]、澳大利亚[33]、意大利、荷兰、英国[26]和土耳其[27]等国家的学者报道了由菠菜炭疽菌引致的菠菜炭疽病。
Xu等[21]发现甘肃庆阳市的箭筈豌豆炭疽病可危害植物叶片、茎和荚, 发病初期, 在新叶上形成圆形褐色斑点。在个别小叶上可能存在一个或多个病斑, 一半甚至整个小叶都受到侵染。病害发生严重时, 叶片变黄, 有许多浅棕色至棕褐色坏死斑点, 边缘较暗。茎和叶柄上的病变最初是黑色线性的, 后来逐渐扩大并且经常与相邻病斑聚结, 直到侵染大部分茎秆。
本研究发现接种效果最好的方法是喷雾刺伤法。张金萍[34]在对杨树(Populus spp.)叶纹斑病病原菌分离鉴定的过程中, 发现相比无伤接种, 刺伤接种能显著提高病害的发病率。引起奉新猕猴桃(Actinidia chinensis)烂果的6种病原菌都能从猕猴桃果实伤口侵入而导致发病[35]。欧美杨(Populus euramericana)细菌性溃疡病菌主要通过有伤接种引起植株发病, 这说明病原菌进入植株的途径主要是通过枝条上的伤口[36]。这能从一定程度上说明伤口是病原菌侵入植株进而造成损害的一种途径。箭筈豌豆炭疽病病原菌具有从叶片表面直接侵入而导致发病的能力。
Damm等[26]和Kurt等[27]描述了菠菜炭疽菌的形态特征, 分生孢子大小分别为(15~20) μ m× (2~4) μ m和(17~28) μ m× (2.5~6.0) μ m, 几乎没有弯曲, 两侧逐渐变细; 炭疽菌属真菌种类多、分布广, 为箭筈豌豆炭疽病的主要病原菌, 对箭筈豌豆具有极大危害性。在早期炭疽病病原菌的研究中, 多采用传统形态学结合致病性的鉴定方法[37], 依靠病原菌的纯培养物、分生孢子及附着胞等形态特征进行分类[38]。但由于炭疽属真菌近缘物种颇多, 种间关系复杂, 不同种间的培养性状较为相似且同种间的培养性状不稳定, 易受环境影响, 给分类造成了很大难度[39]。随着分子生物学技术的发展, 可结合形态学特征和多基因序列分析更为准确地鉴定炭疽菌。Xu等[21]利用ITS、ACT、TUB2、GAPDH和HIS3进行多基因联合建树, 将甘肃庆阳箭筈豌豆炭疽病的病原菌鉴定为小扁豆刺盘孢; 有研究表明, 扩增ITS、ACT、TUB2、CHS1、GAPDH和HIS3等引物的序列可用来鉴定菠菜炭疽菌[26]。本研究基于ITS、ACT、CHS 1和GAPDH基因序列构建了多基因系统发育树, 结合形态学鉴定结果, 将甘肃夏河箭筈豌豆炭疽病的病原鉴定为菠菜炭疽菌。
目前已报道的菠菜炭疽菌寄主包括菠菜、甜菜、藜(Chenopodium album)、马齿苋(Portulacae herba)、荷兰芹(Petroselinum crispum)和三叶草[29]。本研究只选用了4种豆科和2种禾本科植物, 进行了箭筈豌豆炭疽病病原菌的寄主范围测定, 结果表明, 菠菜炭疽菌除了寄生箭筈豌豆外, 苜蓿、红豆草、三叶草和燕麦也是其潜在的寄主, 而菠菜炭疽菌不能侵染黑麦草。菠菜炭疽菌的寄主范围究竟是否涉及其他科, 还有待进一步探究。此研究为炭疽病发生田块的合理轮作倒茬提供了科学参考, 应重视不同寄主间的交叉感染, 防止病害的流行。在生产上应引起高度重视, 制定合理的防治措施, 在田间操作时应尽量避免将箭筈豌豆与苜蓿、红豆草、三叶草等植物进行间作或轮作[40], 并制定合适的栽培制度。
1) 经过形态学特征观察结合基于内转录间隔区(ITS)、肌动蛋白(ACT)、几丁质酶(CHS1)和3-磷酸甘油醛脱氢酶(GADPH) 4个基因序列的多基因系统发育分析, 并进行致病性测定, 将甘肃夏河箭筈豌豆炭疽病的病原菌鉴定为菠菜炭疽菌, 这是箭筈豌豆菠菜炭疽菌在中国的首次报道。
2) 菠菜炭疽菌对红豆草和燕麦均具有强致病性, 对兰箭1号、兰箭2号、兰箭3号及333/A 4个品种的箭筈豌豆具有中等致病性, 对苜蓿和三叶草的致病性最低, 而对黑麦草无致病性。
3) 供试6种寄主植物受到菠菜炭疽菌侵染后, 其株高、根长和地上生物量均有不同程度的降低。其中对箭筈豌豆、红豆草和燕麦的影响较大, 说明这3种植物是菠菜炭疽菌的优势寄主。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|