作者简介:王泳超(1987-),男,黑龙江齐齐哈尔人,讲师,博士。E-mail: wangyongchao723@163.com
为明确干旱胁迫下γ-氨基丁酸(GABA)保护玉米幼苗光合系统的生理响应,以郑单958为试验材料,依据玉米幼苗生长数据,选择1 mmol·L-1为γ-氨基丁酸(GABA)供试浓度,设置空白对照(CK)、1 mmol·L-1 GABA(G)、20%聚乙二醇(PEG-6000)模拟干旱胁迫(D)、20%聚乙二醇(PEG-6000)模拟干旱胁迫和1 mmol·L-1 GABA(DG)4个处理开展玉米水培试验。结果表明:不同浓度GABA能缓解干旱胁迫的抑制作用,使玉米幼苗恢复生长,其中1 mmol·L-1 GABA效果最好。干旱胁迫下,外源施用1 mmol·L-1 GABA能显著提高叶片超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性,减少丙二醛(MDA)、超氧阴离子($O_{2}^{-}$)和过氧化氢(H2O2)积累,降低叶片相对电导率。此外,外源GABA能显著提高干旱胁迫下叶片内可溶性蛋白、可溶性糖和脯氨酸含量,从而提高细胞保水能力。外源施用GABA能显著降低叶片干旱胁迫下初始荧光( F0),提高暗适应下最大可变荧光( Fv)、最大荧光( Fm)和最大光量子效率( Fv/ Fm),从而降低叶片光化学损伤。在干旱胁迫第5天,与D处理相比,DG处理SPAD数值、净光合速率( Pn)、蒸腾速率( Tr)和气孔导度( Gs)分别提高8.25%、7.69%、9.13%和7.38%,胞间CO2浓度( Ci)降低2.93%。因此,外源GABA能通过降低叶片的氧化损伤和提高细胞保水能力来改善叶片对干旱胁迫的适应能力,从而保护玉米幼苗光合系统。
This research aimed to clarify the physiological role of γ-aminobutyric acid (GABA) in the protection of the photosynthetic system of maize seedlings under drought stress. The maize variety studied was Zheng Dan 958, and the exogenous application of GABA at a concentration of 1 mmol·L-1 was used tested in a hydroponic culture experiment where drought stress was simulated by adding PEG-6000. The experiment comprised four treatments: Blank control (CK), 1 mmol·L-1 GABA treatment (G), 20% PEG (PEG-6000) simulated drought stress (D), 20% PEG (PEG-6000) simulated drought stress and 1 mmol·L-1 GABA treatment (DG). It was found that: Application of 1 mmol·L-1 exogenous GABA significantly improved the activities of superoxide dismutase, peroxidase and catalase and decreased the malondialdehyde, superoxide anion and hydrogen peroxide concentrations of leaf tissue. Leaf relative conductivity was also reduced. Furthermore, exogenous GABA significantly increased the content of soluble protein, soluble sugar and proline in leaves under drought stress, thereby improving the water retention capacity of cells. Exogenous application of GABA significantly reduced the chlorophyll fluorescence F0 value; and improved the Fv, Fm and Fv/ Fm values, thereby reducing photochemical damage in leaves. Compared with the D treatment, SPAD, Pn, Tr and Gs of the DG treatment were increased by 8.25%, 7.69%, 9.13% and 7.38%, respectively in 5th day after stress. In addition, Ci was decreased by 2.93%. In summary, exogenous GABA improved the drought resistance in leaves by reducing oxidative damage and increasing the capacity for cell water retention, thereby protecting the photosynthetic system in maize seedlings.
水资源短缺是当前全球农业发展和粮食安全所面临的一个严峻生态问题, 尤其是进入21世纪以来, 在全球气候变暖、极端气候事件趋多增强的背景下, 干旱的强度和频率都呈现明显增加的趋势, 成为限制农作物产量的主要因素[1]。目前中国受干旱影响的地区较多, 给农作物生产带来的影响也日渐严重[2]。玉米(Zea mays)是我国重要的粮食、经济和饲料作物, 其在生育期间需水量较大, 对干旱胁迫较为敏感, 其中苗期干旱灾害已成为制约玉米增产的重要因素[1]。因此研究干旱胁迫下玉米的适应及保护机制, 对玉米生产具有重要的理论意义和实际价值。
光合作用作为植物最基本的生命活动, 对干旱胁迫非常敏感。干旱胁迫下, 气孔和非气孔限制共同导致光合作用下降, 而植物对干旱胁迫的首要响应就是关闭气孔[3], 这会造成CO2吸收减少, 引起CO2同化量降低, 净光合速率下降, 从而导致光系统Ⅱ (PSⅡ )光能过剩, 进而引起活性氧代谢障碍, 丙二醛(malondialdehyde, MDA)等有害物质在膜系统的积累, 损害叶片光合机构。植物会通过减少光能的捕获、提高体内抗氧化酶活性、积累渗透调节物质等途径来减少氧化损伤, 从而维持细胞膜正常生理功能, 并以此来提高植物对干旱胁迫的抵抗能力[4, 5]。但植物通过改变自身生理生化代谢来适应干旱胁迫的能力是有限的, 仅在干旱初期阶段具有显著效果, 而随着干旱时间和程度的增加, 植物自身代谢出现紊乱, 最终影响生长, 甚至死亡[6]。
目前, 在农业生产中可以通过多种栽培耕作措施和调控手段来减少干旱胁迫对作物生长的危害, 其中外源施用化学调控物质具有效率高、成本低等特点而被广泛应用。γ -氨基丁酸(γ -aminobutyric acid, GABA)是一种以自由态存在于各种生物中的四碳非蛋白质氨基酸, 在作物的非生物胁迫中[7], GABA具有能维持作物体内C/N平衡、作为信号传导物质、改善抗氧化酶系统活性、提高渗透调节物质含量等功能, 因此其与作物的抗逆境调控密切相关[8]。近年来, 关于外源GABA调控作物生理功能来提高作物抗逆性的研究已取得一定进展, Harsh等[9]的研究表明, 1 mmol· L-1的GABA处理高温胁迫的水稻(Oryza sativa)幼苗, 会缓解高温胁迫对幼苗光合特性的损伤, 使叶绿素含量、最大光量子效率(maximum opticon efficiency, Fv/Fm)得到恢复, 减小高温胁迫对光合作用的损害。外源GABA处理显著提高了超氧化物歧化酶(superoxide dismutase, SOD)、过氧化物酶(peroxidase, POD)等活性, 分别比NaCl处理提高7.62%和37.55%, 而对过氧化氢酶(catalase, CAT)活性无显著影响[10]。此外, 外源施用GABA能明显地降低番茄(Solanum lycopersicum)幼苗叶片活性氧产生速率、过氧化氢(hydrogen peroxide, H2O2)和丙二醛含量, 增加可溶性蛋白、可溶性糖等渗透调节物质的积累, 降低脯氨酸含量, 从而缓解干旱胁迫对番茄幼苗生长的抑制作用[11]。因此, 本研究以郑单958为试验材料, 采用向营养液中加入聚乙二醇(PEG-6000)模拟干旱胁迫的方法, 通过叶片喷施GABA, 研究干旱胁迫下GABA保护玉米幼苗光合系统的生理响应, 以期为GABA缓解干旱胁迫的研究提供理论依据, 为玉米的抗旱生产提供新的技术手段。
试验所用品种为郑单958(河南农业科学院提供), 供试调控剂为γ -氨基丁酸(购自Sigma公司), 干旱模拟剂为聚乙二醇(PEG-6000)(购自Sigma公司)。
本试验于2018年在河南农业大学农学院人工气候光照培养箱进行, 播种前种子用10%(V/V)的次氯酸钠(NaClO)消毒10 min, 蒸馏水冲洗3次, 浸种8 h后在(26± 1) ℃的恒温培养箱中黑暗催芽48 h, 之后将出芽的种子播种于50 cm× 30 cm的塑料托盘中, 以沙子为基质。待玉米幼苗生长到二叶一心时, 选择长势一致的幼苗定植于装有2.5 L的1/2 Hoagland营养液[pH为(6.5± 0.1)]的水槽中培养, 幼苗生长环境为:光周期为12 h/12 h(昼/夜), 昼/夜温度为(28± 1) ℃/(25± 1) ℃, 光照强度约为400 μ mol· m-2· s-1, 培养箱内相对湿度为60%~70%, 每3 d更换一次营养液, 待幼苗生长到三叶一心时进行处理。1)对照(CK), 正常施加营养液, 叶片喷施清水; 2)GABA处理(G), 正常施加营养液, 叶面喷施不同浓度的GABA(0.25、0.5、1、2、5、10 mmol· L-1), 每天喷施一次, 连续喷施2 d; 3)干旱处理(D), 施用含有浓度为20%(M/V)PEG-6000的Hoagland营养液, 叶面喷施清水; 4)干旱+GABA处理(DG), 施用含有浓度为20%(M/V)PEG-6000的Hoagland营养液, 叶面喷施不同浓度的GABA(0.25、0.5、1、2、5、10 mmol· L-1)。干旱处理在喷施GABA结束后进行, 处理期间每天进行pH的测定和调整, 于干旱胁迫的1、3和5 d分别取完全展开的倒2叶进行指标测定。每个处理3次生物学重复。
1.3.1 幼苗生长指标的测定 于胁迫后5 d每个处理选取3株幼苗, 用最小刻度为1 mm的米尺测量株高, 用CI-203型叶面积仪(美国CID公司, 产地:美国)测定单株叶面积。将用清水冲洗干净的幼苗表面水分吸干, 于烘箱内105 ℃杀青30 min, 之后80 ℃烘干至恒重, 测定整株干鲜重, 单位为g· 株-1。于胁迫第5天取植株根系进行根系扫描。
1.3.2 抗氧化酶活性测定 超氧化物歧化酶(SOD)活性采用氮蓝四唑(nitro-blue tetrazolium, NBT)还原法测定[12], 过氧化物酶(POD)活性采用愈创木酚法测定[13], 过氧化氢酶(CAT)采用高俊凤[14]的方法测定。
1.3.3 氧化损伤指标测定 丙二醛(MDA)含量采用硫代巴比妥酸法测定[15], 超氧阴离子含量(
1.3.4 渗透调节物质测定 脯氨酸(proline, Pro)含量采用磺基水杨酸法测定[18]。可溶性糖含量参照薄晓培等[19]的测定方法。可溶性蛋白含量采用G-250方法测定[20]。
1.3.5 叶片相对电导率和叶片相对含水量测定 为取各植株相同部位叶片, 首先测定植物叶片的鲜重M1, 后将叶片浸入蒸馏水中5~6 h, 使叶片吸水达到饱和状态, 取出擦干叶片至表面无水分残留, 再称重, 得植物叶片的饱和鲜重M2, 最后将植物叶片放进烘箱, 105 ℃杀青30 min, 再于80 ℃环境下烘至恒重, 得叶片干重M3。叶片相对含水量按公式计算:(M1-M3)/(M2-M3)× 100%。参照郝再彬等[21]的方法测定叶片相对电导率。以相对电导率的大小表示质膜相对透性即质膜受害程度:质膜相对透性=L1/L2× 100%, L1表示组织杀死前外渗液电导值, L2表示组织杀死后外渗液电导值。
1.3.6 光合指标测定 使用FMS-2脉冲调制式叶绿素荧光仪(Hansatech, UK)测定F0:初始荧光、Fv:暗适应下最大可变荧光、Fm:最大荧光等荧光参数, 通过这些参数可计算出PSⅡ 的Fv/Fm:最大光量子效率、Fv/F0:PSⅡ 潜在活性等值。测定前叶片暗适应时间为20 min, 光化学强度为400 μ mol· m-2· s-1, 饱和闪光强度为8000 μ mol· m-2· s-1。叶绿素含量采用CCM-200+手持叶绿素测定仪(澳作生态仪器有限公司, 产地:北京)进行测定, 以SPAD数值代表叶绿素相对含量(chlorophyll relative content)。使用LI-6400便携式光合仪(LI-COR公司, 产地:美国)测定Ci(胞间CO2浓度)、Tr(蒸腾速率)、Gs(气孔导度)和Pn(净光合速率)。
试验数据取平均值, 每个处理3次生物学重复。采用SPSS 17.0进行方差分析, 采用LSD最小显著性差异法进行多重比较, 植株生长数据采用胁迫后5 d数据, 采用Microsoft Excel 2010 作图。
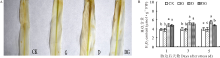
图1所示, 与正常处理(CK)相比, 干旱胁迫明显抑制幼苗生长, 外源施用GABA可以缓解干旱胁迫带来的抑制作用。外源施用GABA能提高干旱胁迫下玉米幼苗株高、叶面积、全株干重, 降低根冠比(表1); 但不同浓度的GABA缓解抑制作用的能力不同, 其浓度为1 mmol· L-1时效果最好。与D处理相比, 喷施1 mmol· L-1 GABA的幼苗株高、叶面积、茎叶干重和根系干重分别增加20.45%、37.41%、31.92%和49.41%, 根冠比降低13.34%, 且差异显著(表1)。表2表明, 在干旱胁迫条件下, 1 mmol· L-1的GABA缓解干旱胁迫的效果最好, 与D处理相比, 1 mmol· L-1的GABA浓度下根长、根表面积、根体积和根尖数分别增加了37.92%、52.50%、85.42%和37.40%, 且差异显著。因此, 选取1 mmol· L-1的GABA进行后续试验。
| 表1 干旱胁迫下不同浓度GABA对玉米幼苗生长的影响 Table 1 Effect of different concentrations of GABA on maize seedling growth under drought stress |
| 表2 干旱胁迫下不同浓度GABA对玉米幼苗根系的影响 Table 2 Effect of different concentrations of GABA on maize seedling roots under drought stress |
超氧化物歧化酶(SOD)能歧化两个
H2O2对细胞会产生毒害作用, 过氧化物酶(POD)被认为是活性氧清除系统中主要的H2O2清除酶。随着胁迫天数增加, 对照、G和DG处理呈先升后降的趋势, D处理呈下降趋势(图2B)。与对照相比, G处理叶片POD活性提高, 但差异不显著。在干旱胁迫后1 d, 叶片POD活性显著升高, 第3和5天显著降低(图2B)。外源施用GABA会显著提高干旱胁迫下叶片内POD活性, 与D处理相比, DG处理在胁迫后的1、3和5 d分别升高13.33%、52.14%和53.69%(图2B)。
过氧化氢酶(CAT)能将H2O2分解成为H2O和O2, 从而降低H2O2含量。随着胁迫天数的增加, 对照和G处理呈先升后降的趋势, D和DG处理呈下降趋势(图2C)。正常条件下, 外源施用GABA能促进叶片的CAT活性升高, 但差异不显著(图2C)。干旱胁迫下, CAT活性在3和5 d低于对照, 分别下降4.14%和11.61%(图2C)。外源施用GABA可缓解干旱胁迫对叶片的伤害, 显著提高CAT活性, 与D处理相比, DG处理的叶片CAT活性在胁迫后的1、3和5 d分别升高8.01%、15.95%和37.71%, 差异显著(图2C)。
丙二醛(MDA)是膜脂过氧化的产物, 过量积累对细胞膜具有损害作用。随着胁迫天数的增加, 叶片MDA含量逐渐升高。正常条件下, 外源施用GABA对MDA含量没有显著影响(图3)。干旱胁迫导致叶片内MDA含量显著升高, 与对照及G处理相比差异显著。施用外源GABA会显著降低干旱胁迫下叶片内MDA含量, 在胁迫后的1、3和5 d, DG处理的MDA含量分别是D处理的0.82、0.63和0.60倍(图3)。
氧气在植物体内产生氧自由基时第一个产生的就是超氧阴离子, 其本身具有毒性, 进行一系列的反应后会产生其他的氧自由基, 对细胞有毒害作用。对叶片中的
H2O2对细胞会产生毒害作用, 对叶片中的H2O2进行显色反应, 其中褐色斑点越深, 表明叶片H2O2含量越高。由图5A可知, 干旱胁迫会增加叶片中H2O2含量, 而DG处理H2O2含量明显降低。由图5B可知, 随着处理时间的增加, CK和G处理的叶片中H2O2含量并没有明显变化, D处理和DG处理呈现逐渐升高的趋势。在正常生长条件下, 外源施加GABA对叶片内H2O2含量没有显著影响, 而在干旱胁迫下, 外源施加GABA可以降低叶片内H2O2的含量, 特别在处理第5天, 与D处理相比, DG处理的叶片内H2O2含量降低14.58%, 差异显著。
可溶性蛋白是重要的渗透调节物质和营养物质, 其增加和积累能提高细胞的保水能力, 对细胞的生命物质及生物膜起到保护作用。图6A显示, 随着胁迫天数的增加, 叶片内可溶性蛋白含量逐渐升高。正常生长条件下, 外源GABA对叶片可溶性蛋白含量没有显著影响, 而在干旱胁迫下可溶性蛋白含量显著升高。与对照相比, 胁迫后1、3和5 d的D处理可溶性蛋白含量分别升高72.55%、62.52%和68.67%。干旱胁迫下, 外源施用GABA能提高叶片内可溶性蛋白含量, 提高叶片保水能力。与D处理相比, DG处理在胁迫后的1、3和5 d可溶性蛋白含量分别升高16.43%、53.93%和74.39%, 且胁迫3和5 d时差异显著。
 | 图6 干旱胁迫下GABA对玉米幼苗渗透调节物质的影响Fig.6 Effect of GABA on osmotic regulators in maize seedlings under drought stress |
可溶性糖作为植物的营养成分, 其含量变化可以反映植物的生长状态。图6B显示, 与对照相比, G处理可溶性糖含量没有显著变化。在干旱胁迫条件下, 随着处理时间的增加, D处理的可溶性糖含量逐渐增加, 而外源喷施GABA使叶片可溶性糖含量进一步增加, 与D处理相比, DG处理在胁迫后的1、3、5 d叶片可溶性糖含量分别增加11.72%、3.45%和19.08%。
脯氨酸含量可以反映植物遭受干旱胁迫的情况。由图6C可知, 在正常生长情况下, 外源施加GABA对叶片内脯氨酸含量没有显著影响。干旱胁迫会明显提高叶片脯氨酸含量, 尤其是在干旱胁迫第5天, 脯氨酸含量明显增加。外源施加GABA可以提高干旱胁迫下叶片的脯氨酸含量, 与D处理相比, 干旱胁迫的第1、3、5天, DG处理叶片内脯氨酸含量分别提高26.19%、23.63%和29.81%。
叶片相对含水量多少可代表抗干旱能力的大小, 因此是判断抗旱性的重要指标。图7A显示, 随着胁迫天数增加, 对照和G处理叶片相对含水量呈上升趋势, 而D和DG处理呈下降趋势。正常生长条件下外源施用GABA对叶片相对含水量没有显著影响。干旱胁迫会显著降低叶片相对含水量, 胁迫后第5天, D处理相对含水量比对照降低24.31%, 差异显著。外源施用GABA能显著提高干旱胁迫下叶片相对含水量, 提高叶片持水能力。与D处理相比, DG处理在胁迫后第5天叶片相对含水量提高10.63%, 差异显著。
 | 图7 干旱胁迫下GABA对玉米叶片相对含水量及相对电导率的影响Fig.7 Effect of GABA on relative water content and relative electric conductivity of maize leaves under drought stress |
叶片的相对电导率可以判断细胞膜受伤害的程度。由图7B可知, 随着处理时间的增加, 叶片的相对电导率呈现逐渐增加的趋势, 但是G处理和CK相比差异不显著。干旱胁迫下, 叶片的相对电导率显著增加, 外源喷施GABA可以降低叶片的相对电导率, 在处理的第1、3、5天, 与D处理相比, DG处理的叶片相对电导率分别降低14.95%、29.49%和32.21%, 差异显著。
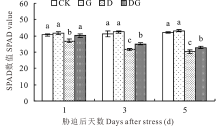
叶绿素是光合作用的物质基础, 负责光能的捕获、传递、分配和转化等过程, 其含量变化能够反映光合作用的强弱, 而SPAD数值的大小能直接反映出叶绿素含量的多少。如图8所示, 随着胁迫天数增加, 对照和G处理的SPAD值呈小幅上升的趋势, D和DG处理呈现逐渐下降的趋势。G处理SPAD数值与对照相比在所有取样天数差异不显著, 这表明正常生长条件下施用外源GABA对叶绿素含量无明显影响。干旱胁迫会导致SPAD数值显著降低, 外源施用GABA能显著提高叶片SPAD数值, 与D处理相比, DG处理在胁迫后1、3和5 d叶片SPAD数值分别升高8.97%、10.73%和8.25%。
F0代表最小荧光强度, 是已经暗适应的光合机构全部PSⅡ 中心都开放时的荧光强度。图9A显示, 随着胁迫天数增加, F0呈逐渐上升的趋势。与对照相比, G处理的F0下降, 但只有胁迫后第5天差异显著。干旱胁迫下, F0显著升高, 与对照相比, D处理F0在胁迫后1、3和5 d分别升高9.01%、11.38%和15.43%。外源施用GABA能显著降低干旱胁迫下的F0, 与D处理相比, DG处理F0在胁迫后1、3和5 d分别下降5.44%、6.34%和7.53%。
 | 图9 干旱胁迫下GABA对玉米幼苗叶绿素荧光参数的影响Fig.9 Effect of GABA on chlorophyll fluorescence parameters of maize seedlings under drought stress |
Fv代表黑暗中最大可变荧光强度, 图9B所示, 随着胁迫天数的增加, 对照和G处理的Fv呈上升趋势, D和DG处理呈下降趋势。正常生长条件下, 外源施用GABA对Fv没有显著影响, 而干旱胁迫会显著降低Fv, 且与对照相比差异显著。干旱胁迫下施用外源GABA能提高Fv, 与D处理相比, DG处理的Fv在胁迫后1、3和5 d分别升高6.95%、8.76%和15.04%, 且差异显著。
Fm代表黑暗中最大荧光, 是已经暗适应的光合机构全部PSⅡ 中心都关闭时的荧光强度。由图9C可知, 正常生长条件下, 外源GABA对Fm没有显著影响, 而干旱胁迫下Fm显著降低, 与对照相比差异显著。外源施用GABA会显著升高干旱胁迫下的Fm, 与D处理相比, DG处理的Fm在胁迫后1、3和5 d分别升高3.46%、4.27%和7.79%。
Fv/Fm代表没有遭受环境胁迫并充分暗适应的叶片PSⅡ 最大的或潜在的量子效率。图9D所示, 对照和G处理随着胁迫天数的增加Fv/Fm无明显变化, 而D和DG处理的Fv/Fm有小幅下降。正常条件下, 外源施用GABA会提高Fv/Fm, 但与对照相比差异不显著。干旱胁迫下Fv/Fm下降, 但差异不显著。外源施用GABA能提高干旱胁迫下的Fv/Fm, 但差异不显著。
净光合速率(Pn)可以直接反映植物光合作用的强弱。由图10A可知, 非胁迫条件下, 外源施用GABA会提高叶片净光合速率, 但差异不显著。干旱胁迫下, 叶片净光合速率显著降低, 外源喷施GABA可以缓解干旱胁迫导致的损伤, 净光合速率上升。与D处理相比, 处理的第1、3和5天, DG处理净光合速率分别提高了9.42%, 6.85%和9.13%。
 | 图10 干旱胁迫下GABA对玉米幼苗光合参数的影响Fig.10 Effect of GABA on photosynthetic parameters of maize seedlings under drought stress |
蒸腾速率(Tr)可以反映植物对矿物质吸收和运输能力的高低。由图10B可知, 随着处理时间的增加, CK和G处理的叶片蒸腾速率都呈现出先下降后上升的趋势, 外源施加GABA会提高叶片的蒸腾速率。干旱胁迫会导致蒸腾速率降低, 处理的第1、3和5天, D处理的蒸腾速率分别降低了17.05%、16.9%和54.3%。DG处理可以显著提高干旱胁迫下幼苗的蒸腾速率, 处理的第1、3和5天, DG处理叶片的蒸腾速率分别提高了6.75%、1.79%和7.69%。
气孔导度(Gs)可以反映二氧化碳和水汽通过气孔的难易程度。由图10C可知, 随着处理时间的增加, CK和G处理的气孔导度逐渐增加。在干旱胁迫条件下, D处理的叶片气孔导度逐渐降低, 与D处理相比, DG处理的第1、3和5天叶片的气孔导度分别提高了6.89%、5.28%和7.38%。
胞间CO2浓度(Ci)可以间接反映光合作用强弱。由图10D可知, 随着处理时间的增加, CK和G处理的叶片胞间CO2浓度逐渐降低, D和DG处理的逐渐增加。与CK相比, G处理的叶片胞间CO2浓度在培养的第1、3和5天分别降低了7.06%、11.63%和8.43%。在干旱胁迫条件下, 与D处理相比, DG处理的叶片胞间CO2浓度在培养的第1、3和5天分别升高了9.97%、8.73%和2.93%。
干旱是影响玉米生长和发育最常见的环境胁迫, 当玉米遭受干旱胁迫时, 其在形态和生理上会产生抗旱应对策略, 如干物质以及根冠比的调整等[22]。本研究中, 在干旱胁迫下, 玉米幼苗的株高、叶面积和幼苗干重都出现明显下降, 而根冠比出现明显升高, 表明干旱胁迫对地上部分干物质积累的抑制作用要大于地下部分, 与李丽杰等[23]采用外源亚精胺处理干旱胁迫幼苗的结论相似。在轻度和重度干旱胁迫中, 外源施用GABA能明显提高甜瓜(Cucumis melo)幼苗的株高、茎粗、叶面积和整株干鲜重, 缓解干旱胁迫给生长造成的抑制作用[24]。本研究中, 干旱胁迫下外源施用GABA能显著的恢复玉米幼苗的生长, 缓解干旱胁迫的抑制作用, 且GABA浓度在1 mmol· L-1时效果最佳。根冠比的显著下降也表明GABA对干旱胁迫下地上部分的促进作用大于地下部分。
植物适应环境的变化需要植物细胞体内多种途径之间的协调平衡来实现, 非生物胁迫下, 这种平衡被破坏, 特别是当植物暴露于水势急剧下降时, 体内活性氧(reactive oxygen species, ROS)等物质大量积累, 从而对蛋白质、DNA和脂质等造成损伤[25]。膜质损伤会造成MDA、
当植物遭遇干旱胁迫, 植物自身抗氧化酶系统活性会出现明显升高, 以便于清除活性氧, 减少膜质过氧化物的积累, 保证细胞膜的完整性和正常的功能[26]。本研究发现, 在干旱胁迫下, SOD、POD和CAT活性在胁迫1 d时高于对照, 之后出现显著下降, 且明显低于对照。这表明干旱胁迫初期玉米植株能通过自身的保护系统清除体内有害物质, 而随着胁迫时间的延长其生理功能受到严重影响, 自身调控能力减弱, 植株的生长受到抑制。外源施用GABA能显著提高SOD、POD和CAT的活性, 有效缓解干旱胁迫对玉米叶片的损伤, 与杨丽文等[11]在番茄幼苗上的研究有相似的结论, 即外源施加GABA不仅能提高SOD、POD、CAT的活性, 且升高幅度也逐渐增加, 进而有效缓解胁迫带来的损伤。
当植株遭受干旱胁迫, 玉米叶片内脯氨酸、可溶性糖、可溶性蛋白等渗透调节物质含量会明显升高, 以便于维持细胞膨压, 保持细胞正常生理功能, 提高玉米幼苗的渗透调节能力, 进而缓解干旱胁迫带来的氧化损伤。GABA是一种四碳非蛋白质氨基酸, 由于其特殊结构使其在逆境胁迫中具有同脯氨酸类似的功能。Liu等[27]研究水分胁迫对烟草(Nicotiana tabacum)叶片中GABA和脯氨酸含量的影响中发现, GABA作为一种渗透调节物质其维持细胞膨压, 降低活性氧含量的作用明显高于脯氨酸。本研究发现, 干旱胁迫下, 外源施用GABA除能起到渗透调节作用外还能提高叶片内脯氨酸、可溶性糖和可溶性蛋白含量, 证明其不仅能作为一种渗透调节物质, 也能促进其他渗透调节物质的积累。同时, 在干旱胁迫下, 外源喷施GABA可以显著增加叶片的相对含水量, 降低叶片相对电导率, 从而改善叶片生理状态, 维持植株的正常生长。
玉米幼苗有机物质的积累与叶片光合特性密切相关, 其中叶绿素在光合作用中发挥着重要作用, 其参与对光的吸收、传递以及原初光化学反应等重要过程[28]。研究表明, 干旱胁迫下玉米叶肉细胞中的叶绿素含量显著减少, 而维管束鞘细胞的叶绿素减少并不显著[29]。在对水稻幼苗的研究中发现, 干旱胁迫能抑制叶绿素合成途径中关键酶基因的表达, 从而使酶活性降低, 进而造成叶绿素合成受阻[30]。但Kaewsuksaeng[31]的研究却认为干旱胁迫下叶绿素含量降低主要是由于色素加速降解导致。本研究中, 干旱胁迫降低了叶片SPAD数值, 并且随着胁迫天数的增加, SPAD数值下降速度加快, 与对照相比差异显著。Esmaeil等[32]在黑孜然(Nigella sativa)上的研究结果表明, 外源施用不同浓度的GABA都能明显提高不同干旱程度下叶绿素a和叶绿素b含量, 改善光合作用。这种更好的持绿性可能是因为外源GABA对某些酶的激活作用, 从而启动了光合保护机制, 以及其干旱胁迫期间对代谢的调节作用[33]。本研究中虽未对叶绿素a和叶绿素b单独测定, 但SPAD数值能准确反映出叶片中叶绿素含量。外源施用GABA能显著的提高干旱胁迫下叶片SPAD数值, 缓解干旱胁迫下叶绿素分解速率或提高其合成速率, 从而改善光合能力。
维持光合器官的稳定和较高的光化学效率是植物响应抗旱的主要机制, 也是探究植物在干旱胁迫下光合机构是否受到损伤的主要依据[34]。较多的研究已证实, 干旱胁迫对植物的PSⅡ 反应中心造成很大程度的损伤, 促使电子传递速率下降和光化学效率受到抑制, 而PSⅡ 的受损导致过量激发能产生, 与氧气反应产生大量活性氧, 加速叶绿素降解和加剧PSⅡ 结构中复合蛋白变性失活程度, 导致光抑制的加剧, 造成植物的光能转化效率显著降低[35]。本研究中, 干旱胁迫下, 玉米叶片F0显著升高, Fv和Fm显著下降, 与对照相比, 干旱处理的Fv/Fm虽没有明显变化, 但干旱处理降低了Fv/Fm, 这表明叶片PSⅡ 反应中心受到胁迫伤害, 从而降低了电子传递速率和光化学效率。王日明等[36]研究表明, 高温胁迫下, 外源施用5 mmol· L-1的GABA能明显地提高Fv/Fm、ETR(电子传递速率, electron transport rate)、qP(荧光猝灭)等荧光参数, 有效地改善了PSⅡ 的功能。而本研究中, 干旱胁迫下, 外源施用GABA能显著地降低F0, 提高Fv和Fm, 但Fv/Fm没有显著变化, 这可能是由于GABA对不同的逆境胁迫的调控机制不同导致的。
光合作用是影响作物生产力的重要因素。干旱导致作物产量降低主要是由于光合速率下降、降低了同化产物合成, 抑制了作物生长。干旱胁迫下, 植物的光合作用受到抑制, 光合作用的抑制作用主要是多种因素共同作用的结果, 如果胞间CO2浓度和气孔导度均减少, 则净光合速率主要受气孔限制作用, 如果气孔导度减少, 但胞间CO2浓度不变或增加, 则净光合速率减少可归因于非气孔限制因素[37]。本试验研究发现, 干旱胁迫下叶片的净光合速率、蒸腾速率、气孔导度降低, 胞间CO2浓度升高, 这表明光合作用受到气孔和非气孔限制因素的共同限制。外源施加GABA能显著缓解干旱胁迫带来的损伤[38], 增加叶片的净光合速率、蒸腾速率、气孔导度, 使叶片的胞间CO2浓度降低, 有效缓解干旱胁迫对玉米幼苗叶片光合作用的气孔和非气孔限制作用, 提高干旱胁迫下玉米幼苗的光合能力。
干旱胁迫下, 外源施用GABA能显著提高玉米叶片SOD、POD和CAT活性, 减少MDA的积累, 从而缓解干旱胁迫对细胞膜的损害, 使叶片的相对电导率下降。此外, 渗透调节物质含量的升高, 可以提高细胞吸水、保水能力, 维持细胞的正常形态。同时, 外源施用GABA能显著降低叶片F0, 提高Fv、Fm和Fv/Fm, 从而有效地减少叶片光化学损伤, 缓解干旱胁迫对叶绿素及光合作用的负面效应, 使玉米幼苗恢复生长。外源施加GABA还可以提高叶片的蒸腾速率、净光合速率、气孔导度, 缓解干旱胁迫对幼苗光合作用的影响, 提高植株在干旱胁迫下的适应能力。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|