作者简介:谢德金(1988-),男,河南洛阳人,在读博士。E-mail:1246353702@qq.com
研究3种不同光质[白光(WL)、红光(RL)和蓝光(BL)]对草珊瑚幼苗的生长状态和相关生理生化指标的影响。选取不同光质处理下的草珊瑚幼苗,测定生长状态(株高、地径、总鲜重、总干重、根系形态指标、根冠比)和相关生理生化指标[叶绿素含量、可溶性蛋白含量、可溶性糖含量、还原糖含量、淀粉含量、丙二醛(MDA)含量、过氧化物酶(POD)活性、超氧化物歧化酶(SOD)活性、净光合速率( Pn)、最大光能利用率(LUEmax)、最大水分利用率(WUEmax)和最大光合效率( Fv/ Fm)],并结合方差统计方法进行分析比较。在不同光质处理下,大部分试验指标均有显著差异,与白光和蓝光处理相比,红光除了能促进幼苗株高及WUEmax增加外,其他相关指标都显著减少;与白光相比,蓝光的根系各形态指标、根冠比、可溶性蛋白含量、MDA含量、POD活性、SOD活性、WUEmax等相关指标显著增加,其他指标都相应减小。红光处理能够促进草珊瑚幼苗的株高和WUEmax增加,但导致其他指标显著降低。蓝光处理不仅显著增加幼苗根系的各形态指标,而且提高了其最大水分利用率,结果可为利用LED光质调控技术提高草珊瑚幼苗的培育技术提供一定的理论基础。
This research aimed to explore in detail the effects of three light regimes [white light (WL), red light (RL), and blue light (BL)] on growth status and physiological and biochemical traits of Sarcandra glaba seedlings. Measures of plant growth status conducted were: plant height, stem diameter, total fresh weight (roots and shoots), total dry weight (roots and shoots), root morphology indexes, and root∶shoot ratio. Physiological and biochemical traits measured included chlorophyll, solution protein, solution sugar, reducing sugar, and malondialdehyde (MDA) concentrations of leaf tissues; peroxidase (POD) and superoxide dismutase (SOD) activities, net photosynthetic rate ( Pn), maximum light use efficiency (LUEmax), maximum water use efficiency (WUEmax) and maximum photosynthetic efficiency ( Fv/ Fm). Most of the measured traits showed differences between light regimes. Compared with WL and BL groups, the RL treatment resulted in a significant reduction in a majority of the measured traits. Exceptions were plant height and WUEmax which were increased in RL. Compared with the WL treatment, in the BL light regime, root morphology indexes, root∶shoot ratio, protein and MDA concentrations, POD and SOD activities and WUEmax were considerably increased, while other indexes were decreased. In this experiment, the RL treatment resulted in a significant decrease in many traits. Meanwhile, the BL regime not only stimulated root morphology indexes, but also improved WUEmax. This research lays a theoretical foundation for developing light quality guidelines for the cultivation of S. glaba seedlings.
光是植物进行光合作用和光形态建成的直接影响因子, 光质、光照强度和光周期是光的三要素, 且都是重要的环境变量, 通过调节光的三要素, 植物体内的光受体(如:光敏素、隐花素等)能够接收外界的光信号的变化, 从而对植物的生长发育和代谢等方面起到调控作用[1, 2, 3]。从对光质的相关研究可知, 红光和蓝紫光作为叶绿素吸收光谱的最强吸收区, 通过LED技术特定控制最强吸收区中红光、蓝光和紫光等单一光质和以不同比例组合的红蓝复合光以及通过补光的方式对植株进行诱导, 从而获知不同光质对植株的形态特征、生理生化指标、代谢活性成分、光合作用的光响应和叶绿素荧光的影响, 进而筛选出能够满足目标需求的植株已成为热点[4, 5]。梁宗锁等[6]在对丹参(Salvia miltiorrhiza)的研究中发现:不同补光能够显著影响丹参幼苗的生长、有效成分的积累以及相关的酶活性, 增加蓝光能显著降低丹参的株高, 增加红光能促进地下根生物量的增加, 补充蓝光和红光后均大幅度提高丹酚酸B含量, 但对丹参酮Ⅱ A的含量没有明显影响。吴小玉[7]以绞股蓝(Gynostemma pentaphyllum)种子萌发幼苗为研究对象, 探明了红光与蓝光都有利于绞股蓝皂苷的积累, 其中红光比蓝光更有利。李慧敏等[8]发现, 红蓝复合光有利于黄秋葵(Abelmoschus esculentus)幼苗的生长, 并能显著提高叶绿素的含量, 而且气孔发育相对较好。龚洪恩等[9]通过研究发现以1∶ 9组合的红蓝复合光处理油茶(Camellia oleifera)苗, 有利于油茶苗的生长和光合能力的提高。木荷(Schima superba)和杉木(Cunninghamia lanceolata)幼苗叶片在单一的红光和蓝光光质诱导后, 都能显著降低植株的潜在最大光合能力, 同时使幼苗叶片抗氧化酶系统的稳态失衡, 不利于幼苗生长[10]。总之, 光质对植物的生长发育具有重要意义。
草珊瑚(Sarcandra glaba), 为金粟兰科草珊瑚属多年生常绿草本或亚灌木, 具祛风除湿、抗菌消炎、活血止痛、通经接骨及抗肿瘤等功效[11]。在已报道的文献中, 草珊瑚在播种育苗技术、化学成分分析、药理、培育技术、质量控制技术及其分离提取技术等方面的研究较为深入, 而在光质对草珊瑚幼苗的形态特征、生理生化及代谢活性成分等方面的研究较为缺乏[12]。本试验以草珊瑚幼苗为材料, 选择白光、红光和蓝光3种不同光质对其进行诱导, 从而测定并分析光质对植株幼苗的形态指标、生理生化指标、光合作用的光响应参数和叶绿素荧光参数的影响变化, 为育苗技术提供一定的理论依据。
供试材料为2018年11月15日在福建省三明市三元区楼源国有林场采集的完全变红的草珊瑚成熟果实。育苗基质采用PINDSTRUP公司的Pindstrup Seeding型号, 颗粒大小为010 mm, pH 5.5的泥炭藓和珍珠岩按3∶ 1进行混合配制, 盆栽基质则采用Pindstrup Substrate No.5型号, 颗粒大小为1030 mm, pH 5.5的泥炭藓和珍珠岩按3∶ 1进行混合配制。两种不同型号的混合基质在使用前均用一定浓度的多菌灵进行杀菌消毒, 15 d后取出备用。育苗盘大小为34 cm(长)× 25 cm(宽)× 4.5 cm(高), 盆栽花盆为10 cm(长)× 10 cm(宽)× 8.5 cm(高)的黑色方形盒。
采收的成熟果实经搓洗后, 去除果肉并分离出种子。将种子在通风处晾干后, 用湿沙层积的方式(沙和种子的比例3∶ 1)于种子低温低湿储藏柜中进行储藏。2019年3月1日取出适量的草珊瑚种子均匀散播在盛有湿沙的育苗盘中, 在恒温恒湿光照培养箱内进行培养, 培养条件为:温度25 ℃, 湿度50%, 光合有效辐射为30 μ mol· m-2· s-1, 光周期为光照(16 h)和黑暗(8 h)。培养期间每5 d翻动一次, 根据沙子的湿度, 及时喷水保持适宜的含水量。大约培养40 d后, 种子破壳, 待幼根长出1 cm左右时, 将其转移至含有育苗基质的育苗盘中, 在恒温恒湿光照培养箱内进行出苗培养。培养条件为:温度25 ℃, 湿度60%, 光合有效辐射为50 μ mol· m-2· s-1, 光周期为光照(16 h)和黑暗(8 h), 培养期间每10 d根据基质的湿度适量补充水分。培养30 d左右, 待长出第一对真叶并完全伸展开时, 将长势大致一样的幼苗逐一转移至盛有盆栽基质的方形盒中。
2019年5月15日将长势一致的共120株草珊瑚幼苗, 置于人工气候培养室中进行3 种不同LED光质处理, 即WL (普通白光LED, white light, 450 nm)、RL(红光LED, red light, 656 nm)、BL(蓝光LED, blue light, 380760 nm)。3种光质下分别有40株幼苗进行诱导培养, 10株为一个重复, 共4个重复。处理条件:光合有效辐射为80 μ mol· m-2· s-1, 光周期16 h光照/8 h黑暗, 室温为25 ℃, 培养期间每7 d根据基质的湿度适量补充水分。在第30和60天后进行取样, 对相关指标进行测定并记录。
1.2.1 生长状态指标测定 对不同光质处理下的第30和60天的草珊瑚幼苗株高和地径进行测定, 每个重复随机选取5株, 重复4次, 每个处理共20株幼苗(n=20)。在不同光质处理下, 对第60天的总鲜重和各部位组织鲜重进行称重记录。在105 ℃的烘箱中杀青20 min后在80 ℃条件下烘干至恒重, 对总干重和各部位组织干重进行称量。草珊瑚的根系(鲜重条件下)在EPSON扫描仪按实际比例扫描后, 用根系扫描仪软件WinRHIZO对根系的总表面积、体积、根尖数和根长进行测定。
1.2.2 生理生化指标测定 采用丙酮∶ 无水乙醇∶ 蒸馏水(4.5∶ 4.5∶ 1)的混合提取液对不同光质处理下第60天的第2对鲜叶(从顶芽向下数)进行浸提, 用酶标仪微量法测定叶绿体色素提取液在波长OD663、OD645和OD470的吸光度, 后参考高俊凤[13]的方法对总叶绿素、叶绿素a、叶绿素b和类胡萝卜素含量进行计算。参照高俊凤[13]的方法测定叶片可溶性糖、还原糖含量。使用苏州科铭生物技术有限公司生产的试剂盒分别对可溶性蛋白(考马斯亮蓝法)、蔗糖、淀粉、丙二醛(malondialdehyde, MDA)含量及超氧化物歧化酶(superoxidedismutase, SOD, 氮蓝四唑法)和过氧化物酶(peroxidase, POD)活性进行测定。测定时每个重复随机选取第2对鲜叶位置的3个叶片, 重复4次, 每个处理共12个叶片(n=12)。
选取不同光质处理下第60天的第2对鲜叶位置(从顶芽向下数)的任意叶片, 利用LI-6400便携式光合测定仪(Li 6400-XT, 美国)测定光响应曲线, 每个重复选择3个叶片进行测量, 重复4次, 每个处理共12个叶片(n=12)。测定时间为上午9:00-11:30, 在每次测量前, 需要将叶片放置于光合有效辐射(photosynthetically active radiation, PAR)为800 μ mol· m-2· s-1的红蓝光源下诱导20 min, 并且从高到低设置16个不同的光强梯度:1400, 1200, 1000, 800, 600, 400, 300, 200, 100, 80, 70, 60, 50, 40, 20和0 μ mol· m-2· s-1, CO2浓度设定在400 μ mol· mol-1, 在室温为25 ℃的条件下进行光响应曲线测量。测量完毕后, 将不同光照强度下的净光合速率(net photosynthetic rate, Pn)、气孔导度(stomatal conductance, Gs)、胞间二氧化碳浓度(intercellular CO2 concentration, Ci)和蒸腾速率(transpiration rate, Tr)等相关参数进行整理计算, 同时根据Pn和Tr的比值(Pn/Tr)得出不同光质处理下的水分利用率(water use efficiency, WUE)以及根据Pn和PAR的比值(Pn/PAR)计算出光能利用率(light use efficiency, LUE)的值。参考叶子飘等[14]提供的光合计算软件(4. 1. 1版本), 求得与光响应曲线、水分利用率光响应曲线以及与光能利用率光响应曲线有关的参数, 如:α (初始速率, initial rate)、Pnmax(最大净光合速率, maximum net photosynthesis rate)、LUEmax(最大光能利用率)、WUEmax(最大水分利用率)、Isat (光饱和点, light saturation point)、Ic(光补偿点, light compensation point)、Rd(暗呼吸速率, dark respiration rate)以及修正模型公式中的α 、β 、γ 和Rd这4个系数, 在Origin 9.0软件中自定义拟合光响应曲线、水分利用率光响应曲线以及与光能利用率光响应曲线, 相关的拟合方程参考叶子飘等[15]提供的理论模型。
使用IMAGING-PAM系列调制叶绿素荧光成像系统(Walz, Germany)对第60天不同光质处理下的第2对鲜叶(从顶芽向下数)位置的叶片进行叶绿素荧光参数测定, 每个重复选择3个叶片, 重复4次, 每个处理共12个叶片(n=12)。测量前将要测量的植株在黑暗条件下暗处理30 min后将叶片取下, 放置于观察板上, 进行相关叶绿素荧光参数的测量, 测量的参数如下:实时荧光(real-time fluorescence, Ft), 初始荧光(initial fluorescence, Fo), 暗适应后的最大荧光(maximum fluorescence, Fm), 荧光F为打开饱和脉冲后的3 s内Ft值的平均, 光下最大荧光(maximum fluorescence under the light, Fm'), PSⅡ 最大光合效率(maximum photochemical efficiency, Fv/Fm)=(Fm-Fo)/Fm, PSⅡ 实际光合效率[actual photochemical efficiency, Y(II)]=(Fm'-F)/Fm', 调节性能量耗散的量子产额[the quantum yield of non-regulated energy losses, Y(NPQ)], 非调节性能量耗散的量子产额[the quantum yield of non-regulated energy losses, Y(NO)], 非光化学淬灭系数(non-photochemical quenching coefficient, qN)=(Fm-Fm')/(Fm-Fo'), 光化学淬灭系数(photochemical quenching coefficient, qP)=(Fm'-F)/(Fm'-Fo'), 其中Fo'=Fo/(Fv/Fm+Fo/Fm')。
使用Excel进行数据处理, 运用SPSS 20.0对相关的试验数据进行单因素方差分析, 并采用Duncan检验法进行显著性差异检验(P< 0.05)。光响应曲线的试验数据用由叶子飘等[14]提供的光合计算软件4.1.1版本进行计算。使用Origin 9.0对光响应曲线进行拟合, 采用Graphpad prism 7进行图表绘制, 并且图表中的数据均为平均值± 标准差。
2.1.1 光质对株高和地径的影响 经过30 d处理后, 红光株高比白光大约增加了16.20%, 蓝光比白光减少了0.551 cm。3种光质的地径差异显著, 白光最大, 红光最小(图1)。经过60 d处理后, 红光的株高显著高于白光和蓝光, 蓝光与白光之间的高度差异也逐渐增加, 蓝光比白光降低了1.360 cm, 而红光地径指数显著小于蓝光和白光, 且蓝光略大于白光。随着时间的推移, 白光、红光和蓝光之间在株高上的差异逐渐增大, 而在地径方面, 红光与白光和蓝光的差异显著增加, 蓝光处理下幼苗在地径横向增长量上会更有优势。
2.1.2 光质对鲜重和干重的影响 分别对处理60 d的各组织部位的鲜重和干重进行分析比较, 不同光质下各组织部位的鲜重和干重的差异具有相似性, 红光处理的总鲜重比白光和蓝光减少了35.19%~39.26%, 且明显的差异部位主要是叶和根部(图2)。相较于红光, 白光和蓝光处理下总鲜重没有显著差异, 在茎鲜重上, 两者较为接近, 但是在叶和根的鲜重方面两者有显著差异, 白光处理的叶鲜重比蓝光多0.262 g, 而白光根鲜重又比蓝光少0.488 g。所以从各组织部位的鲜重和根冠比的分析可知, 蓝光能够促进根部组织的发育, 而红光能够促进地上部茎的增高, 同时也抑制了根的生长。
2.1.3 光质对根系形态指标的影响 不同光质处理下的根长、根表面积、根体积和根尖数差异显著(图3)。除总根尖数外, 蓝光处理下的总根长、总根表面积、总根体积都显著高于白光和红光, 红光处理下的4个根系形态指标都是最低的。而从径级分类的结果可知, 不同光质处理下的根长、根表面积、根体积都是在0.5~1.0 mm范围内所占的比重最大, 分别占到:66.61%~71.01%, 64.84%~66.64%, 61.60%~68.70%, 而在0~0.5 mm径级范围内, 根尖数占到总数的96.08%~97.22%。以上结果更进一步阐明蓝光处理能够促使根长、根表面积、根体积的生长发育, 从而增加植株的地下鲜重, 使植株的根冠比增加, 壮苗指数提高, 而红光则起到相反的作用。
2.2.1 光质对可溶性蛋白、可溶性糖、蔗糖、还原糖、淀粉、叶绿素和类胡萝卜素含量的影响 可溶性蛋白含量在3种光质处理下差异显著(表1), 蓝光处理最高, 红光最低, 且红光比蓝光和白光减少了10.33%23.67%。红光处理可溶性糖、蔗糖和还原糖含量与其他两个处理具有显著差异, 含量依次减少了28.69%35.92%, 15.80%47.29%, 22.96%23.84%。在蓝光处理下, 蔗糖含量比白光和红光都显著增加。在红光和蓝光处理下, 淀粉含量显著高于白光处理。综上所述:红光不利于体内积累更多的可溶性糖、蔗糖和还原糖, 而淀粉含量相比于白光处理明显增加; 单一蓝光诱导也会造成幼苗叶片中可溶性糖含量的减少, 但有利于蔗糖的合成和淀粉的积累。叶绿素和类胡萝卜素的含量明显受到不同光质的影响(图4), 相较于白光, 蓝光和红光处理的叶绿素a、叶绿素b和类胡萝卜素含量都有不同程度的降低, 但在红光下, 叶绿素和类胡萝卜素含量最低且与白光差异显著, 蓝光除了对叶绿素a含量有显著的减少外, 叶绿素b和类胡萝卜素含量与白光处理的差异不显著。
| 表1 不同光质对草珊瑚幼苗的可溶性蛋白、可溶性糖、蔗糖、还原糖和淀粉含量的影响 Table 1 Effect of different light qualities on the content of solution protein, solution sugar, sucrose, reducing sugar and starch of S. glaba (mg· g-1 FW) (mean± SD, n=12) |
2.2.2 光质对MDA含量、POD和SOD活性的影响
经过红光处理后, MDA含量比白光显著降低了30.57%(表2), 而经过蓝光处理后, MDA含量约为白光的1.123倍。在蓝光处理下, POD和SOD活性均高于红光和白光, 而红光处理下这两个指标均低于白光。
| 表2 不同光质对草珊瑚幼苗的MDA含量、POD和SOD活性的影响 Table 2 Effect of different light qualities on the content of MDA, and the activity of POD and SOD of S. glaba |
2.2.3 不同光质下草珊瑚幼苗光合参数的分析 将表3的光合参数Pn及LUE值代入光响应曲线以及与光能利用率光的响应曲线的理论公式中, 用Origin 9.0软件可以高度拟合出不同光质下草珊瑚幼苗的光响应曲线(图5)和光能利用率的光响应曲线, 白光、红光和蓝光下拟合的3条光响应曲线的决定系数(R2)分别为0.996、0.989和0.998。白光、红光和蓝光下诱导的光饱和点分别为:843.557、542.919和776.584 μ mol· m-2· s-1。叶绿素(a+b)含量越大, 其最大净光合速率(Pnmax)和光饱和点(Isat)也越大, 因此白光处理下的草珊瑚幼苗叶片光合速率显著大于蓝光和红光处理(图4, 表3)。3种不同光质处理下光能利用率的光响应曲线在低光强阶段, 其光能利用率随光强的增加而增加(图5), 在短时间内就达到最大值, 而后随着光强的增加而逐渐减弱。随着光强的增大, 3种光质下草珊瑚幼苗叶片Gs、Ci和Tr的动态变化见图6。3种不同光质处理下的植株水分利用率趋势较为相似, 都是随着光强的增加, 达到最大值, 之后出现短时间的下降, 而后又升高。蓝光和红光的水分利用率始终都高于白光, 而在低光强下(低于40 μ mol· m-2· s-1), 蓝光和红光相同, 但随着光强的增加, 蓝光明显高于红光。3种不同光质处理下, 白光的LUEmax值最高, 为0.037 mol· mol-1, 相应的饱和光强为37.160 μ mol· m-2· s-1(表4); 红光的LUEmax最小, 为0.029 mol· mol-1, 其饱和光强为24.551 μ mol· m-2· s-1; 蓝光下的LUEmax与白光差异不大, 并且白光和蓝光处理光能利用率的光响应曲线也较为相似。蓝光处理下的WUEmax值最高, 为6.503 μ mol· mmol-1, 其饱和光强为374.994 μ mol· m-2· s-1; 其次是红光, 而白光的最低, 为4.517 μ mol· mmol-1, 其饱和光强为509.885 μ mol· m-2· s-1。由相关性分析结果可知(表5), Pn与Gs、Tr之间呈极显著正相关, 与叶绿素(a+b)和WUE呈显著正相关, 与Ci呈极显著负相关。
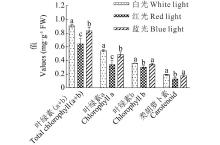 | 图4 不同光质对草珊瑚幼苗的叶绿素和类胡萝卜素含量的影响Fig.4 Effect of different light qualities on the content of chlorophyll and carotenoid |
| 表3 不同光质对草珊瑚幼苗光合参数的影响 Table 3 Effect of different light qualities on the photosynthetic parameters of S. glaba |
 | 图5 不同光质下草珊瑚幼苗的光响应曲线和光能利用率的响应曲线Fig.5 The light response curve and light response curve of light use efficiency of S. glaba under different light qualities |
| 表4 不同光质下最大光能利用率和最大水分利用率及相应的饱和光强 Table 4 The maximum light use efficiency (LUEmax) and water use efficiency (WUEmax) and their saturation irradiance (IL-sat) of S. glaba under different light qualities (mean± SD, n=12) |
| 表5 不同光质下叶绿素含量与部分光合参数的相关性分析 Table 5 Bivariate correlation analysis among chlorophyll (a+b) and other photosynthetic parameters of S. glaba under different light qualities by Spearman’ s rank correlation test |
2.2.4 不同光质下草珊瑚幼苗叶绿素荧光参数的分析 白光处理下草珊瑚幼苗叶片的Fv/Fm值最高, 红光最低, 并且三者的值都低于0.80, 正常生理状态下, 绝大多数C3植物的Fv/Fm为0.800.84, 当Fv/Fm下降时, 表明植物受到了胁迫(表6)。因此, 在光合有效辐射为80 μ mol· m-2· s-1的条件下, 3种光处理的幼苗都受到了光胁迫, 并且最大光合潜能也有所降低, 其中红光处理的Fv/Fm值最低, 其最大光合潜能也最弱。红光处理下的草珊瑚幼苗的实际光合效率较低也能说明其实际光合效率较弱。若调节性能量耗散的量子产额较大, 一方面说明光是过剩的, 另一方面也表明植物有能力通过自身的调节机制耗散掉过剩的光能而自我保护。若非调节性能量耗散的量子产额较大, 一方面说明光化学能量转换和自我保护调节机制比较弱, 另一方面说明植物无法耗散过多的光能。非光化学淬灭系数反映了植物通过热耗散的方式将过剩的光能耗散掉, 红光处理下Y(NPQ)值较白光和蓝光大, 而Y(NO)较白光和蓝光小, qN的值也最大, 说明红光处理下的草珊瑚幼苗有过剩的光能, 并且幼苗通过热耗散的方式耗散掉过剩的光能; 白光和蓝光处理的幼苗也有部分光能过剩, 但植株的自我保护调节机制较弱, 无法耗散过多的光能。光化学淬灭系数反映了天线色素吸收的光能用于光化学电子传递的份额, 在3种光质的处理下, 红光和蓝光的qP值较白光高, 但是叶绿素含量较白光低, 说明单一红光和蓝光处理的草珊瑚幼苗能够在叶绿素降低的情况下, 通过提高光化学电子转化率从而提高光合效率。
| 表6 不同光质下草珊瑚幼苗叶绿素荧光参数 Table 6 The chlorophyll fluorescence characteristics of S. glaba under different light qualities |
有研究表明, 在光的有效辐射范围内, 光质对植株茎的影响与其自身波长呈正相关, 波长越长越有利于茎的伸长[16]。前人研究认为, 在增加红蓝复合光中红光的比例或在白光的基础上补充红光有利于植株根系的生长[6, 17], 也有文献显示, 单一的红光有利于铁皮石斛(Dendrobium officinale)的根系生长[18], 巩彪等[19]在对紫背天葵(Gynura bicolor)的研究中发现与白光相比, 红光处理显著增加了紫背天葵的茎粗, 蓝光处理显著抑制了茎的横向生长。本研究中, 波长较长的红光能够促进草珊瑚幼苗在茎的伸长量上显著高于蓝光和白光处理, 但是红光同时也抑制了地径的横向增长以及地下根部形态的生长发育, 这也导致红光诱导下根冠比和壮苗指数明显小于白光和蓝光。蓝光诱导下的草珊瑚幼苗在前30 d, 地径指数显著小于白光, 培养到60 d时, 地径与白光相比几乎没有差异, 并且蓝光诱导下的根系形态指标显著高于白光和红光, 这说明蓝光更有利于植株根系生长健壮。在本研究中, 红光抑制草珊瑚地径的横向增长和根系的生长发育, 与前人研究得出的红光有利于铁皮石斛根系的生长和促进紫背天葵的茎增粗的结论不一致, 这可能与植株本身有很大关系。在鲜重和干重方面, 巩彪等[19]在对紫背天葵的研究中发现红光能够促进植株干物质的增加, 而且白光加红光的补光试验和增加红蓝复合光下红光的比例同样也可以促进丹参、石蒜(Lycoris radiata)和芹菜(Apium graveolens)的鲜重和干重显著增加[6, 17, 20]。在本研究中, 红光促进草珊瑚幼苗茎伸长的同时抑制茎的横向增长, 而且叶面积相对较小, 根部发育明显弱化, 这些生长特征的变化导致全株的鲜重和干重与白光和蓝光相比都显著降低。在蓝光和白光的诱导下, 两种处理的草珊瑚幼苗总鲜重和总干重上没有差异, 但是通过对地上和地下部组织的比较分析可知, 蓝光处理的根部鲜重和干重都大于白光, 而地上部的总鲜重和总干重都小于白光, 从而使蓝光诱导的根冠比比白光更高。同样, Kara等[21]在研究中也发现蓝光诱导下的胡萝卜(Raphanus sativus)块根、叶片和整株干重都高于红光下生长的植株。红蓝光质对不同植株干重和鲜重的影响不尽相同, 这有可能与试验条件和植物的生长习性有密切联系。
许多研究表明, 增加红光在红蓝复合光中的比例能够促进植株可溶性糖含量的增加, 如黄瓜(Cucumis sativus)、西红柿(Solanum lycopersicum)[22]、石蒜[17]、紫背天葵[19]、矾根(Heuchera spp.)[23]和橄榄型油菜(Brassica napus)[24]等, 蓝光有助于可溶性蛋白的积累但是降低了可溶性糖的含量[1]。孙娜等[25]在对番茄的碳氮代谢研究中发现, 红光能够引起番茄叶片蔗糖含量的减少, 淀粉含量的增加, 而蓝光能够同时降低蔗糖和淀粉的含量。宁宇等[20]的研究表明, 与白光处理相比, 红光处理下芹菜叶片的蔗糖和淀粉含量没有明显波动, 而在蓝光处理下蔗糖含量增加, 而淀粉含量明显降低。在本研究中, 单一的红光引起叶片中可溶性蛋白、可溶性糖、蔗糖和还原糖含量减少, 而淀粉含量相比于白光处理明显增加, 在红光处理下草珊瑚叶片中蔗糖和淀粉的变化趋势与孙娜等[25]的研究相一致。在蓝光处理下叶片中可溶性蛋白、蔗糖、还原糖和淀粉含量明显增加, 但可溶性糖含量显著减少。通过对比孙娜等[25]和宁宇等[20]的研究结果, 从中可知蓝光能够明显降低番茄和芹菜叶片中淀粉的含量, 对蔗糖的影响呈相反趋势, 而叶片在蓝光诱导下淀粉含量显著升高, 这与两者的研究有所不同。在不同处理条件下, 草珊瑚叶片中糖和淀粉的合成、分解和转化与碳代谢的关键酶, 如蔗糖合成酶, 蔗糖磷酸合成酶和转化酶密切相关, 后续需要通过测定这3种关键酶的活性和酶基因的相对表达量来进一步揭示不同光质下叶片中糖和淀粉的合成、分解和转化。
植物在受到环境胁迫时, MDA经常被用来作为膜脂过氧化指标, 从而间接测定膜系统受损程度及抗逆性, POD和SOD这两种抗氧化酶是植物体内重要的保护酶, 其活性的测定可以反映某一时期植物体内代谢和抗逆性的变化, 也可以反映出植物受活性氧毒害的程度[13, 26]。本研究中的草珊瑚幼苗在受到长时间的蓝光诱导后, MDA含量的增加表明, 植株的膜系统受到了一定程度的损伤, POD和SOD活性的增高是植株在蓝光胁迫下的抗逆性反应, 从而能够应对并减缓活性氧对植株的毒害。相反, 在红光诱导下的MDA含量, SOD与POD活性均显著低于蓝光和白光, 说明在红光诱导下草珊瑚幼苗并未受到活性氧毒害的侵袭。
随着光合有效辐射的增加, 叶片的气孔导度和蒸腾速率逐渐增强, 而且对CO2的利用率增强, 胞间二氧化碳浓度也随之逐渐降低, 光合速率增加, 同样植物的净光合速率也会逐渐增大, 到达饱和点后, 由于光抑制现象, 光合速率出现下降, 胞间二氧化碳浓度也相应地略微升高。拟合的光响应曲线能很好地反映植株在不同光质下的光合速率, 并能处理光抑制的光响应问题。LUE和WUE等参数对表征植物的光合效率和水分利用特征具有重要意义[27]。光能利用率能够反映植株叶片对光的利用能力, 值越大, 其利用光能的能力就越强[28, 29, 30]。本试验中白光处理下的草珊瑚幼苗对光的利用能力最强, 而红光最弱, 这与叶片中叶绿素含量的高低有直接联系, 白光处理下的叶绿素含量最高, 相应的光合速率也最大, 对光的利用能力也最强, 红光处理下的叶绿素含量最低, 其利用光能的能力也最弱。WUE能够反映植物叶片对水分的利用率, 其值与净光合速率呈正比, 与蒸腾速率呈反比。本试验中, 蓝光和红光的WUE值均大于白光, 在两者叶绿素含量低于白光的情况下, 蓝光和红光下诱导的草珊瑚植株通过降低蒸腾速率从而提高水分利用率, 这也从侧面反映植物自身的生理调节机制。
正常生理状态下, 绝大多数C3植物的Fv/Fm为0.800.84, 但也有研究将此范围设定为0.760.85[10, 31, 32]。而本研究中, 3种光质处理下的Fv/Fm值都低于0.80, 说明植株在本试验的条件下受到了胁迫。白光的Fv/Fm值最大, 说明白光处理下植物的潜在最大光合能力最强, 而红光处理下植株的Fv/Fm值和Y(II)值在三者中都最低, 这与三者叶绿素含量的多少有密切联系。白光和蓝光的Y(NPQ)值小, 而Y(NO)较大, 表明白光和蓝光处理下草珊瑚幼苗的逆境耐受能力较红光弱, 无法耗散过多的光能而受到损害, 结合对MDA含量、POD和SOD这两种抗氧化酶活性的测定结果分析可知, 红光诱导下植株的MDA含量, 两种酶活性及Y(NO)最低, 而Y(NPQ)最大, 说明红光处理的植株能够通过自身的调节机制耗散掉过多的光能而自我不受损害[33]。
通过3种不同光质对草珊瑚幼苗进行诱导后, 幼苗的生长状态、生理生化指标都发生了显著变化, 红光处理能促进株高增加, 同时抑制了根部结构的发育, 植株的鲜重和干重增加, 而且叶绿素含量及光合速率都显著下降, 不利于植株的生长发育, 但蓝光能促进地下根系统的发育, 使植株的根冠比增高, 植株更加健壮, 在以后的研究和培育中, 可以适当增加蓝光的比例, 有利于草珊瑚幼苗发育。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|






