作者简介:孙小富(1994-),男,贵州盘县人,在读硕士。E-mail:sxfgxk@163.com
为探讨宽叶雀稗在不同供磷水平条件下的形态及生理变化,了解宽叶雀稗对磷胁迫的适应策略,以期为宽叶雀稗的磷养分管理和生理调控提供理论依据。试验采用砂培法,设置极低磷(2 μmol·L-1)、低磷(20 μmol·L-1)、适磷(200 μmol·L-1,对照)、高磷(600 μmol·L-1)、极高磷(1000 μmol·L-1) 5个供磷水平处理,分别在胁迫10、20、30 d后测定幼苗生长状况、根系形态、保护酶活性的变化。结果表明,低磷和极度低磷胁迫显著降低了宽叶雀稗植株高度和地上生物量,同时,叶面积和叶周长均有降低的趋势;根系生物量、总根长、根表面积、根体积、根尖数目、根冠比均高于适磷处理,超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)、酸性磷酸酶(ACP)活性均显著增强( P<0.05),叶片电导率和根部电导率显著提高( P<0.05);主成分分析表明,CAT活性、POD活性和根系磷酸酶活性、根尖数目和根膜透性受磷胁迫的影响较大,供磷水平为600 μmol·L-1时表现较好;偏最小二乘回归分析表明,根表面积、根系磷酸酶活性和叶周长是影响宽叶雀稗产量的重要指标。综合表明,宽叶雀稗可通过降低地上生物量、增加根系数量和根表面积、提高保护酶活性来适应低磷胁迫。
This research explored the morphological and physiological changes of Paspalum wettsteinii under different phosphorus supply levels, to understand the adaptation strategies to low phosphorus stress, and to provide a theoretical foundation for understanding phosphorus nutrient management and physiological regulation in P. wettsteinii. The experiment was carried out using a sand culture method, and treatments comprised 5 levels of phosphorus: 2, 20, 200, 600 and 1000 μmol·L-1, with 200 μmol·L-1 regarded as the control. The changes in seedling growth, root morphology and protective enzyme activity were measured at 10, 20 and 30 days after the imposition of stress. It was found that under low phosphorus supply, the height and aboveground biomass were significantly decreased ( P<0.05), with leaf area and leaf perimeter also showing a decreasing trend. Meanwhile, the root biomass, total root length, root surface area, root volume, number of root tips and root∶shoot ratio were all higher at the low phosphorus supply than in the control. Superoxide dismutase, peroxidase (POD), catalase (CAT) and acid phosphatase (ACP) activities were significantly enhanced ( P<0.05), and leaf lamina and root conductivity were significantly improved ( P<0.05) under low phosphorus supply levels. Principal component analysis showed that CAT activity, POD activity, root acid phosphatase activity, number of root tips and root membrane permeability were significantly affected by phosphorus stress, and better performance when the phosphorus supply level is 600 μmol·L-1 than others. At the phosphorus supply level of 200 μmol·L-1, the multi-trait performance of P. wettsteinii was ranked second, and was exceeded only at the high phosphorus level. Partial least squares regression analysis was used to analyze the relationship between each index parameter and plant biomass under different phosphorus supply levels of P. wettsteinii, and it was concluded that root surface area, root acid phosphatase activity (ACP) and leaf perimeter were crucial indexes affecting the biomass of P. wettsteinii. In summary, these results show that P. wettsteinii adapted to low-phosphorus stress through reducing above-ground biomass, increasing root weight and root surface area, and promoting protective enzyme activity.
磷作为植物生长发育过程中的三大营养元素之一, 是构成核酸、磷脂和高能磷酸化合物等的重要组分, 在能量传递、信息转导、光合作用、酶促反应和物质代谢中扮演着重要角色[1, 2, 3]。随着农业现代化的发展, 我国缺磷的耕地面积不断增加, 缺磷面积(0.70× 108 hm2)占耕地面积(1.07× 108 hm2)的65%左右[2, 4, 5]。增施磷肥能提高土壤中的磷含量, 但磷肥在土壤中容易被固定, 主要以磷酸盐[AlPO4、Ca3(PO4)2、FePO4等]的形式存在, 极大降低了植物对磷的吸收利用效率[6], 而且持续增施磷肥会导致生产成本高、水体富营养化等问题。因此, 研究植物在磷胁迫下的形态适应和生理响应机制, 确定植物的磷胁迫耐受程度, 对提高植物对磷的吸收利用效率, 促进农业可持续健康发展具有重要意义。
目前, 有关植物在磷胁迫下的形态适应和生理响应机制已有报道, 前人通过对烟草(Nicotiana tabacum)[7]、棉花(Gossypium hirsutum)[8]、紫花苜蓿(Medicago sativa)[9]等研究发现, 植物在磷胁迫环境下特别是低磷胁迫时会将较多的地上部分资源分配到根系, 使植物根表面积增加、侧根增长且数量增多、比根长增加、根重和根冠比增加、根毛长度增加且密度增大, 形成排根, 尽可能吸收土壤中的有效磷[2, 7, 8]。Richardson[10]和陈隆升等[11]研究表明, 植物受到磷胁迫时, 根系磷酸酶、柠檬酸、苹果酸、琥珀酸等多种有机酸的含量显著提高, 促进土壤中磷酸盐的溶解, 增加土壤中有效磷的含量。同时, 低磷胁迫使植物地上部分光合作用显著降低, 体内代谢受阻, 生长发育延缓, 出现株高变矮, 叶面积、分枝数或分蘖数减少等形态特征[8, 11]。龚丝雨等[7]对烟草的研究表明, 当植物处于低磷胁迫时, 植物体内的SOD、POD和CAT活性显著增强, 清除植物受胁迫时产生的超氧自由基, 维持细胞内外的氧化还原平衡, 确保植物的正常生长。在高磷胁迫条件下, 植物叶片中无机磷含量、光呼吸与光合比升高, 净光合速率、RuBP酶活性和电子传递速率下降, 光补偿点和表观量子产量下降, 暗呼吸速率提高, 光合午休现象加剧, 抑制了植物的生长和发育[12, 13]。
宽叶雀稗(Paspalum wellsteinii)属于禾本科雀稗属草本植物, 具有较强的耐盐碱、耐瘠薄、耐酸和抗旱的特性, 根系较发达, 生长速度快, 分蘖力和再生力强, 是生态植被恢复的先锋植物[14]。其次, 宽叶雀稗生长速度快, 适口性好, 营养丰富, 产草量高, C/N含量较高, 有利于有机质的积累, 腐殖化系数高, 对土壤有培肥的效果, 能够促进良好土壤结构的形成, 是一种优质的牧草兼绿肥, 在我国南方地区得以推广利用[14, 15]。当前对宽叶雀稗的研究主要集中在生态修复[15]、耐盐抗旱性[16]、种子萌发特性[14]、种子休眠机理及破除方法[17]等方面, 而关于磷胁迫下宽叶雀稗的表型适应和生理响应的研究鲜见报道, 对磷胁迫的适应策略尚不明确, 且南方地区土壤含磷量较低, 以10 mg· kg-1为丰缺界线, 缺磷土壤约占总耕地面积的70%。鉴于此, 本试验通过设置不同磷水平研究宽叶雀稗在磷胁迫下的形态适应和生理响应变化, 探讨其对磷胁迫的响应机制, 为宽叶雀稗对低磷环境的适应提供理论依据。
试验于2018年12月至2019年5月进行。选取健康饱满的宽叶雀稗种子, 用75%的乙醇进行消毒5 min, 然后用蒸馏水冲洗干净, 置于铺满2层滤纸的培养皿中, 放入恒温恒湿培养箱中25 ℃恒温培养, 待出苗7 d后, 选取整齐、发育一致的宽叶雀稗苗移栽至1/2全营养液的石英砂塑料盆中(长26 cm、宽12 cm、高15 cm), 每盆22株, 培养15 d后移栽至全营养液培养10 d, 待其长至三叶一心时进行胁迫处理。全营养液中的磷(KH2PO4)水平分别设置极度低磷2 μ mol· L-1(P0)、低磷20 μ mol· L-1(P1)、适磷200 μ mol· L-1(P2)、高磷600 μ mol· L-1(P3)、极高磷1000 μ mol· L-1(P4)5个处理对宽叶雀稗进行胁迫, 每个处理重复3次。为了使K+浓度维持在1700 μ mol·
供试营养液为改良的Hoagland与阿农微量元素混合液[19], 营养液配方为:KH2PO4 0.2 mmol· L-1、K2SO4 0.75 mmol· L-1、MgSO4· 7H2O 0.65 mmol· L-1、Ca(NO3)2· 4H2O 2 mmol· L-1、EDTA-Fe 0.1 mmol· L-1、H3BO4 1.0× 10-3 mmol· L-1、MnSO4· H2O 1× 10-3 mmol· L-1、ZnSO4· 7H2O 1.0× 10-3 mmol· L-1、CuSO4· 5H2O 0.5× 10-3 mmol· L-1、(NH4)6Mo7O24· 4H2O 0.05× 10-4 mmol· L-1, 营养液pH值为6.20。
1.2.1 形态指标的测定 将磷水平胁迫10、20、30 d的宽叶雀稗植株, 用直尺测量株高; 取相同部位的叶片, 利用叶面积扫描仪测定各处理时间的叶长、叶宽和叶面积; 将胁迫30 d后的植株连同根系一同取出, 从根节部位将植株地上部分与地下部分分开, 利用ScanMaker 9800XL plus扫描根系, 将扫描后的图片用Win RHIZO软件进行分析, 计算总根长、根系直径、根表面积等参数, 并将根和茎叶置于65 ℃下烘干, 计算地上生物量和地下生物量。3个生物学重复, 每个重复取6株。
1.2.2 生理指标的测定 采用对硝基苯磷酸二钠法(叶饼法)测定叶片酸性磷酸酶(acid phosphatase, ACP)活性和根部酸性磷酸酶活性[20]; 采用电导仪测定电导率[21]; 采用活性愈创木酚法测定过氧化物酶(peroxidase, POD)活性[22]; 采用紫外分光光度法测定过氧化氢酶(catalase, CAT)活性[22]; 采用氮蓝四唑光还原法测定超氧化物歧化酶(superoxide dismutase, SOD)活性[22]。
采用MS Excel 2007进行统计分析, 采用SPSS 20.0软件进行单因素方差分析(ANONA)和多重比较(Duncan), 采用SigmaPlot 14.0制图。主成分分析用于研究不同供磷水平对各形态变异和生理响应的总效应。采用用Origin 2018软件对不同供磷水平下的各指标参数, 即株高(X1)、根冠比(X2)、总根长(X3)、根系直径(X4)、根表面积(X5)、根体积(X6)、根尖数目(X7)、根毛数量(X8)、叶面积(X9)、叶周长(X10)、叶宽(X11)、叶长(X12)、叶长宽比(X13)、根部电导率(X14)、根部酸性磷酸酶活性(X15)、叶片酸性磷酸酶活性(X16)、CAT(X17)、SOD(X18)、POD(X19)、叶片电导率(X20)与总生物量(Y)进行最小二乘(PLS)回归分析, 并得到各指标参数的变量投影重要值(VIP)。
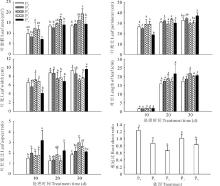
不同供磷水平条件下, 宽叶雀稗株高和生物量各不相同(图1)。在供磷处理10 d时, 极高磷(P4)处理的株高最大, 显著高于适磷处理(P2)和极低磷处理(P0)(P< 0.05); 在供磷处理20 d时, 极高磷处理时株高最大, 较适磷处理高出20.17%, 极低磷处理最小, 显著低于低磷处理和极高磷处理; 在供磷处理30 d时, 适磷处理株高最大, 较极低磷和低磷处理分别高出19.66%和23.05%(P< 0.05), 极高磷处理显著高于低磷处理(P< 0.05), 而与高磷处理(P3)间差异不显著(P> 0.05)。
随着供磷水平的增加, 宽叶雀稗的地上生物量呈先增加后降低的趋势(P< 0.05), 其中适磷处理最高, 显著高于两个低磷处理和极高磷处理(P< 0.05), 而与高磷处理间差异不显著(P> 0.05); 极低磷处理和高磷处理根系生物量相对较高, 单株分别达到0.88和0.90 g, 适磷处理最低, 仅为0.66 g, 表明低磷胁迫和高磷胁迫均能提高根系生物量。单株生物量以高磷处理最大, 显著高于两个低磷处理和极高磷处理(P< 0.05), 而与适磷处理间差异不显著(P> 0.05), 表明适当增加磷含量有利于提高宽叶雀稗的单株生物量。
在不同供磷水平下, 宽叶雀稗叶片形态表现各不一致(图2)。在供磷处理10 d时, 不同处理间的叶长差异均不显著(P> 0.05); 适磷处理的叶面积最大, 显著高于低磷和极高磷处理(P< 0.05); 极高磷处理的叶周长最小, 显著低于其余各处理(P< 0.05), 且其余各处理间差异不显著(P> 0.05); 适磷处理的叶片宽度最大, 显著高于极高磷处理(P< 0.05), 而与其余处理间差异不显著(P> 0.05); 极高磷处理的叶片长宽比较大, 长度是宽度的3.21倍, 显著高于其余各处理(P< 0.05), 且其余各处理间差异不显著(P> 0.05)。在供磷处理20 d时, 高磷处理叶面积最大, 显著高于极高磷处理和两个低磷处理(P< 0.05), 而与适磷处理差异不显著(P> 0.05); 两个低磷处理的叶宽显著高于适磷处理和极高磷处理(P< 0.05), 而二者间差异不显著(P> 0.05); 极高磷处理的叶长宽比最大, 显著高于高磷和极低磷处理(P< 0.05), 而与适磷和低磷处理间差异不显著(P> 0.05); 不同处理间的叶周长和叶片长度差异不显著(P> 0.05)。在供磷处理30 d时, 高磷处理的叶面积最大, 显著高于极高磷和两个低磷处理, 而与适磷处理间差异不显著(P> 0.05); 极高磷处理的叶周长最大, 较高磷、适磷和极低磷处理分别高出21.88%、25.01%和13.21%(P< 0.05), 与低磷处理间差异不显著(P> 0.05); 极高磷处理的叶宽显著高于高磷和适磷处理(P< 0.05), 而与两个低磷处理间差异不显著(P> 0.05), 适磷和高磷处理间差异不显著(P> 0.05); 适磷处理的叶长宽比最大, 长是宽的3.01倍, 显著高于极高磷和两个低磷处理(P< 0.05), 而与高磷处理间差异不显著(P> 0.05); 不同供磷处理间的叶长差异不显著(P> 0.05)。低磷和高磷处理均能显著提高宽叶雀稗的根冠比(P< 0.05), 表明宽叶雀稗在低磷处理和高磷处理胁迫条件下, 有利于促进其根系的生长发育。
在不同供磷水平条件下, 宽叶雀稗根系形态发生了改变(图3)。在低磷处理和高磷处理环境条件下, 总根长变大, 显著高于适磷处理(P< 0.05), 其中以极高磷处理最大, 较高磷、适磷、低磷和极低磷处理分别高出1.16、1.72、1.36和1.46倍; 极高磷处理的根系直径最小, 显著低于其余各个处理, 适磷处理显著高于高磷处理, 而与两个低磷处理间差异不显著(P> 0.05); 极高磷处理的根表面积和根体积最小, 显著低于其余各处理(P< 0.05), 且其余各处理间差异不显著(P> 0.05); 低磷和极高磷处理的根尖数目显著高于适磷和极低磷处理(P< 0.05), 而与高磷处理间差异不显著(P> 0.05); 低磷处理的根毛数量最多, 显著高于适磷和极高磷处理(P< 0.05), 而与极低磷和高磷处理间差异不显著(P> 0.05)。说明本试验中, 低磷处理环境条件下, 宽叶雀稗通过增加根尖数和根毛数量来吸收环境中的磷, 适当的高磷环境有利于促进根系的伸长和根表面积的增加, 但较高的磷环境反而抑制根系的生长。
与适磷处理相比, 高磷处理和低磷处理条件下, 宽叶雀稗细胞保护酶(CAT、POD、SOD)的活性均有所提高(图4), 且随着处理时间的延长呈增加的趋势。在供磷处理10、20、30 d时, 极低磷处理的CAT活性分别是正常供磷的1.76、1.12、1.13倍, 低磷处理的CAT活性较正常供磷分别高出46.53%、3.02%、25.10%, 在供磷处理10、20 d时, 两个高磷处理均显著高于适磷处理, 在供磷30 d时, 极高磷处理显著高于适磷处理(P< 0.05), 而高磷处理与适磷处理间差异不显著(P> 0.05)。在供磷处理10、20、30 d时, 极低磷处理的POD活性分别是适磷处理的1.48、1.26和1.25倍, 低磷处理分别是适磷处理的1.25、1.04和1.05倍, 高磷处理分别是适磷处理的0.97、1.07和1.02倍, 极高磷处理分别是适磷处理的1.15、1.18和1.29倍。在供磷处理10、20、30 d时, 低磷和高磷处理的SOD活性均显著高于适磷处理(P< 0.05)。在供磷处理10 d时, 各处理间的叶片酸性磷酸酶活性均差异不显著(P> 0.05), 在供磷20和30 d时, 低磷处理和高磷处理均显著增强, 且极低磷和极高磷处理增加幅度更为明显。说明本试验中, 在低磷和高磷胁迫环境条件下, 宽叶雀稗通过增强自身细胞保护酶的活性, 维持细胞的稳态来适应外界环境带来的压力, 同时通过增加植物体内的酸性磷酸酶活性来提高磷的利用效率。
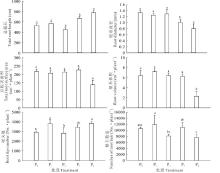
在低磷和高磷胁迫条件下, 宽叶雀稗根部酸性磷酸酶活性均有增加的趋势(图5), 极低磷和低磷处理较适磷处理分别高出23.53%和80.00%(P< 0.05), 且三者间差异显著(P< 0.05); 高磷和极高磷处理较适磷处理分别高出33.09%和17.89%(P< 0.05), 二者间差异不显著(P> 0.05)。根部和叶片电导率随着低磷和高磷胁迫程度的增加呈增加的趋势, 在极度低磷胁迫时, 分别是适磷处理的1.36和1.37倍; 在低磷胁迫时, 分别是适磷处理的1.31和1.18倍, 表明宽叶雀稗在极度低磷胁迫时受到的伤害比低磷胁迫严重。高磷和极高磷处理的根部电导率较适磷处理分别高出46.66%和56.27%, 叶片中较适磷处理分别高出10.04%和37.68%, 表明极高磷处理胁迫下宽叶雀稗的受害程度较大。
通过主成分分析(表1)可以得出, 提取的3个主成分的累积贡献率达91.27%, 对数据的变异具有较高的解释。其中主成分1(PC1)、主成分2(PC2)和主成分3(PC3)分别解释了50.09%、26.61%和14.58%的变异。第1主成分中, 叶宽、CAT活性、POD活性、叶片酸性磷酸酶活性和叶片电导率的权重系数均高于0.900(表1), 表明不同供磷水平对叶片形态和细胞保护酶活性有显著的影响; 第2主成分中, 根冠比、根系直径、根尖数量和根体积的载荷值较大(表1), 表明根系受磷胁迫水平的影响较为明显; 第3主成分中, 根毛数量、根尖数目、叶面积、总根长和单株生物量的载荷值相对较大, 是对磷元素供给较为敏感的指标。利用主成分分析法对不同供磷水平下宽叶雀稗的形态适应和生理响应的综合评价(表2)可以得出, 5个磷水平中高磷处理(P3)(600 μ mol· L-1)条件下, 得分最高, F值为0.570, 宽叶雀稗的综合表现较好; 其次是适磷处理(P2)(200 μ mol· L-1), F值为0.364; 再者分别是低磷(P1)、极度高磷(P4)、极度低磷(P0), 表明适当增加磷的含量有利于宽叶雀稗的生长和发育, 低磷和极度高磷均会影响宽叶雀稗的生长和发育。
| 表1 主成分载荷矩阵及贡献率 Table 1 Loading matrix and contribution rates of principal component |
| 表2 主成分综合得分 Table 2 Principal component comprehensive scores |
采用偏最小二乘(PLS)回归分析对宽叶雀稗不同供磷水平下各指标参数(X)与植株生物量(Y)的关系进行分析(表3), 并根据各指标参数与植株生物量的偏最小二乘回归结果进行相关预测得出回归方程为:Y=1.69-1.27× 10-3X1+8.70× 10-2X2+6.46× 10-5X3-3.57× 10-2X4+5.61× 10-4X5+3.34× 10-3X6-1.74× 10-5X7+6.11× 10-6X8+1.45× 10-2X9-7.46× 10-3X10-1.43× 10-2X11-5.03× 10-4X12+2.13× 10-2X13+1.38× 10-2X14-9.28× 10-3X15-1.52× 10-2X16-7.19× 10-3X17+2.02× 10-6X18+1.56× 10-5X19-4.70× 10-3X20, 各项指标参数对单株生物量的影响程度可根据其变量投影重要性(VIP)进行评价(表3), 结果可以看出, 根表面积、叶面积、叶周长、叶宽、叶片酸性磷酸酶活性、CAT活性、POD活性和叶片电导率的权重系数均大于1.0, 是植株生物量的重要影响因子。而叶长、根部电导率和根部酸性磷酸酶活性的VIP值均小于0.6, 表明该参数对植株生物量几乎没有影响。可见, 在不同供磷水平条件下, 叶片磷酸酶活性、CAT和POD活性的增强有利于根表面积和叶面积的增加, 促进植株的生长和发育, 从而增加其生物量。
| 表3 宽叶雀稗各项指标对单株生物量影响的重要性评价 Table 3 Variable importance of projection (VIP) of various parameters for biomass per plant in P. wellsteinii |
植物体内的磷库分为有机磷库和无机磷库两种, 无机磷库由代谢态磷库和存储态磷库组成。植物受到低磷胁迫时, 细胞存储态无机磷向代谢态无机磷转移, 维持代谢态无机磷的含量, 满足叶片的发育和光合产物的合成及运输时对酯磷的需求[23]。在低磷条件下, 地上部叶无机磷含量和分配比例大幅度降低, 而有机磷的降幅较小但分配比例增加, 叶片对无机磷的利用效率提高, 叶片的光合产物优先分配到根系, 促进根系的生长和发育, 增加根表面积和根系生物量, 并相对抑制地上部的生长, 使植株地上部生物量降低[2, 24]。同时, 低磷胁迫时植物细胞分裂受阻, 体内碳水化合物合成受到影响, 致使植株生长缓慢, 株高变矮[23]。在不同磷胁迫条件下, 植物的根形态也发生了改变, 当植物受到低磷胁迫时, 其总根长、根表面积、根体积、侧根数及根尖数显著提高, 提高了植株的根冠比, 扩大吸收面积, 提高对养分吸收[8, 25, 26, 27, 28]。本研究中, 在低磷水平胁迫处理30 d时, 其株高、地上生物量、叶长、叶面积较适磷处理均有降低的趋势, 而根表面积、总根长、根尖数量和根毛数量、根冠比均有增加的趋势。这可能是由于在低磷胁迫条件下, 植物叶绿素合成受阻, 光合速率下降, 叶肉细胞变小, 叶片生长受阻, 从而导致植株高度变矮、叶面积减少、地上生物量减少[25, 26]。低磷环境下植物优先将光合产物分配到地下部分, 抑制地上部分的生长, 从而促进根系生长, 增加根冠比[24]。宽叶雀稗这种降低地上生物量、增加根系生物量和改变根系形态的形式可能是对低磷胁迫的一种适应机制。同时, 在本研究中, 磷过量反而降低了单株生物量。这可能是由于高磷导致植株体内铁、锌、铜等元素的缺乏, 同时磷过量使植株叶片光呼吸/光合(Pr/Pn)升高, 光合午休现象加剧, 净光合速率下降[12, 13], 影响植株的正常的生长发育, 最终导致生物量降低。
在逆境胁迫条件下, 植物体内会产生大量的超氧自由基, 使活性氧代谢失衡, 从而对植物造成一定的氧化伤害。超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)是重要的植物细胞保护酶系统, SOD能够清除植物细胞内的
电导率是衡量植物在逆境胁迫时的受害程度之一。在低磷或高磷胁迫环境下, 植物细胞膜受到不同程度的破坏, 细胞膜的透性增加, 选择透性丧失, 细胞内部分电解质外渗, 使相对电导率升高[31]。本研究中, 在低磷和高磷胁迫条件下, 宽叶雀稗叶片相对电导率、根部相对电导率均显著高于适磷处理。这表明低磷和高磷胁迫会破坏宽叶雀稗细胞膜的选择透性, 植物受害程度较大, 造成代谢紊乱, 影响植株的生长发育。而在低磷胁迫时, 宽叶雀稗根膜透性较适磷供给时略有降低的趋势, 这可能是由于植物受到低磷胁迫时, 根部酸性磷酸酶活性显著增强, 细胞保护酶活性的提高缓解了低磷胁迫对植物的伤害。
土壤有机磷只有经过磷酸酯酶矿化分解为有效态磷才能被植物吸收利用。有机磷的矿化速率取决于土壤磷酸酯酶的活性。酸性磷酸酶是植物根系分泌的一种能够将土壤中的有机磷转化为较易吸收的无机磷的分泌物[32]。在低磷胁迫条件下, 植物根系酸性磷酸酶活性显著增强, 增加植物根系环境中磷酸酯的含量, 加快有机磷的矿化分解, 提高根系生态系统中有机磷的生物有效性, 提高植物对磷的吸收利用效率, 这是植物对低磷胁迫的一种适应机制[33, 34]。本试验研究表明, 宽叶雀稗在低磷环境条件下, 根系酸性磷酸酶(ACP)的活性显著增强, 且随着胁迫时间的延长, 叶片酸性磷酸酶的活性也逐渐增强, 表明ACP活性增强是宽叶雀稗对低磷胁迫的适应性反应。高磷胁迫能增强宽叶雀稗根部酸性磷酸酶活性和叶片酸性磷酸酶活性, 具体的原因需进一步研究。
生物量是衡量牧草对畜牧业生产提供原料的重要指标之一, 牧草的外表形态和生理状态直接或间接地影响牧草的产量。植物根系是吸收营养的主要器官之一, 当植物处于低磷胁迫环境时, 根系表面积会呈增加的趋势, 根冠比增加, 同时根系分泌的有机酸能改善根际生态环境, 促进环境中有效磷的活化, 提高对磷的吸收利用率, 从而满足自身的生长需要[35]。当植物处于高磷胁迫条件下, 植物的生理代谢发生紊乱, 碳水化合物的合成和利用受阻, 可溶性糖通过韧皮部转运到茎和根组织的量大大增加, 促进了光合产物向根运转增加, 导致植株变矮, 生物量减少[36]。本研究中, 通过偏最小二乘法回归分析结果表明, 在不同供磷条件下, 根系表面积、根部酸性磷酸酶活性和叶周长是影响宽叶雀稗单株生物量的重要特征。这是因为根表面积反应植物根系与环境中营养元素的接触面积, 在一定程度上反映对营养成分的吸收能力, 细根是感知磷含量变化最为敏感的根系部分, 在磷胁迫条件下, 植物根系酸性磷酸酶活性增强, 有利于刺激细根的生长, 增加根表面积, 提高根系吸收能力和呼吸代谢速率[37, 38, 39]。植物根系的生长发育能有效摄取环境中的水分和无机盐, 为地上部分叶片进行光合作用提供原料, 促进叶片的生长发育, 使叶片周长变大, 提高植物的生物量。
本试验通过对宽叶雀稗在不同磷水平处理10、20、30 d时, 形态变化和生理响应的研究结果得出, 供磷水平为600 μ mol· L-1时, 宽叶雀稗综合表现较好。在低磷或较高磷胁迫环境下, 宽叶雀稗通过降低植株高度、地上生物量、叶面积和叶周长, 增加根系生物量、总根长、根表面积、根体积、根尖数目、根冠比, 同时提高机体内超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)活性, 增强酸性磷酸酶(ACP)活性来适应磷胁迫。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|