作者简介:牛欢欢(1994-),女,汉,河南郑州人,硕士。E-mail: 1035613644@qq.com
以光叶紫花苕子为供体植物,采用生物测定法,研究供体材料地上部及地下部不同浓度浸提液(2.5、5.0、10.0、20.0、40.0 g·L-1)对燕麦、黑麦草、紫花苜蓿和白三叶4种牧草种子萌发过程的影响,以期为牧草间的轮作提供理论依据。结果表明:在供试浓度范围内,光叶紫花苕子地上部浸提液明显抑制紫花苜蓿和白三叶的种子萌发,且白三叶种子发芽率随着浓度的增加而降低,40 g·L-1处理下的白三叶种子发芽率与对照相比减少62.5%;光叶紫花苕子地下部浸提液抑制黑麦草、紫花苜蓿和白三叶幼苗根长,其中,40 g·L-1处理下紫花苜蓿根长与对照相比抑制作用最为显著,抑制率达64.94%;在地下部浸提液对4种牧草幼苗苗高的影响中,紫花苜蓿幼苗苗高在40 g·L-1处理下与对照相比差异显著。同时发现,不同浓度的浸提液处理均降低黑麦草、紫花苜蓿和白三叶幼苗叶绿素含量,而增加燕麦幼苗叶绿素含量,在20 g·L-1地下部浸提液处理下,燕麦叶绿素含量与对照相比增加144.23%;地下部浸提液均显著增加紫花苜蓿与白三叶幼苗过氧化物酶(POD)活性,与对照相比差异显著;浸提液处理可增加白三叶幼苗的过氧化氢酶(CAT)活性,但其降低紫花苜蓿幼苗的CAT活性。
This research used a bioassay method to evaluate the effects of a range of concentrations (2.5, 5.0, 10.0, 20.0, 40.0 g·L-1) of extracts of aboveground and underground parts of Vicia villosa on seed germination of four important forage species: Avena sativa, Lolium multiflorum, Medicago sativa and Trifolium repens. The results showed that in the concentration range tested, the V. villosa extracts of aboveground parts significantly inhibited the seed germination of M. sativa and T. repens. The inhibitory effect of T. repens increased with increasing concentration and the germination rate of T. repens seeds reduced by 62.5% compared with the control under the 40 g·L-1 treatment. The extract of underground parts of V. villosa inhibited the root length of L. multiflorum, M. sativa and T. repens. Among the tested species, the M. sativa root length under 40 g·L-1 treatment displayed the largest inhibitory effect (64.94%) compared with the control. With respect to the effects of the underground extract on seedling heights, the height of M. sativa seedlings under the 40 g·L-1 treatment was significantly reduced, compared to the control. In some cases, the extracts reduced the chlorophyll content of L. multiflorum, M. sativa and T. repens. However, for A. sativa, treated with underground extracts at 20 g·L-1, the chlorophyll content was increased by 144.23% compared to the control. Treatment with the underground extract significantly increased the peroxidase activity of M. sativa and T. repens. Treatment with the aboveground and underground extract of V. villosa enhanced the catalase (CAT) activity of T. repens and decreased the CAT activity of M. sativa.
化感作用是指植物(包括微生物)通过一定的途径向周围环境释放特定的化学物质(即化感物质), 从而对同种或异种植物(包括微生物)的萌发和生长产生直接或间接影响的效应[1, 2]。植物体的各个器官几乎都存在化感物质, 其中茎、叶器官所含化感物质最多[3]。植物释放化学物质的途径通常被认为是通过淋溶、挥发、根系分泌、植株的分解及种子萌发和花粉传播而产生[4, 5]。植物的化感作用广泛存在, 通过研究植物化感作用, 确定化感物质, 并应用到农业生产中, 可为农作物的轮作、连作制度提供依据[6]。化感作用在作物增产、植物保护等方面有着广阔的应用前景[7]。
研究表明一些具有饲用价值的牧草体内含有化感物质, 其化感物质释放在自身生长的周围环境中, 对自身及周围植物的生长产生影响。常见的优良牧草如紫花苜蓿(Medicago sativa)、白三叶(Trifolium repens)、红三叶(Trifolium pratense)、黄花草木樨(Melilotus officinalis)和狗牙根(Cynodon dactylon)通过研究均被证实具有化感作用[1], 而关于光叶紫花苕子(Vicia villosa)化感作用的研究一直较为缺乏。光叶紫花苕子属双子叶植物纲豆科巢菜属变种, 一年生草本植物, 具有高产、优质的特点, 是一种优质冬春补饲青草[8], 也是新建人工草地较理想的保护伴种植物[9]。光叶紫花苕子在冬闲的种植面积逐年增长, 因此研究其化感作用在农田合理轮作中的应用具有重要的现实意义。本试验通过室内生物测定法研究光叶紫花苕子不同部位浸提液对燕麦(Avena sativa)、黑麦草(Lolium multiflorum)、紫花苜蓿和白三叶4种常见牧草种子及幼苗生长的影响, 旨在了解光叶紫花苕子的化感作用, 并对其化感作用潜力进行评价, 为光叶紫花苕子与其他牧草的轮作及实现饲草的优质高产提供理论依据。
光叶紫花苕子于2018年10月14日在湖南农业大学耘园实验基地(113° 7' E, 28° 18' N)种植, 并在当年12月15日进行采集, 燕麦品种青海444(A. sativa cv.Qinghai444)、黑麦草品种特高(L. multiflorum cv.Tetragold)、紫花苜蓿品种吉利(M. sativa cv.Ghillie)和白三叶品种海发(T. repens cv.Haifa)4种牧草种子均由湖南农业大学农学院草业科学研究所提供。
1.2.1 浸提液的制备 将采集的光叶紫花苕子地上部和地下部分开剪成小段, 于室内通风处自然晾干, 用粉碎机粉碎, 分别称取其地上部和地下部各40 g, 加蒸馏水1000 mL, 浸提48 h, 期间用玻璃棒搅拌数次, 然后用滤纸过滤收集浸提液, 获得质量浓度为40 g· L-1的地上部、地下部母液, 用蒸馏水稀释获得质量浓度为2.5、5.0、10.0、20.0 g· L-1 的浸提液, 4 ℃保存备用[10]。
1.2.2 种子萌发及幼苗生长试验 选取种皮完整、粒圆饱满的牧草种子, 用次氯酸钠消毒10 min, 自来水冲洗数次, 然后用蒸馏水冲洗5次, 用滤纸吸干种子表面水分。选用直径12 cm× 12 cm的发芽盒, 内铺两层滤纸[11], 每盒均匀地放入4种牧草种子, 每盒中放入 50 粒种子, 分别加入10 mL不同浓度的光叶紫花苕子浸提液, 对照组加入10 mL蒸馏水, 每处理重复4次, 置20 ℃ 光照培养箱进行光/暗(12 h/12 h)交替培养, 及时补充蒸馏水, 使滤纸始终保持湿润, 每24 h记录种子发芽情况, 参照国家标准结束种子萌发试验[12]。
1.2.3 测定指标与方法 生长指标的测定:10 d后测种子的发芽率(%)、幼苗根长(cm)和苗高(cm)。发芽率=已发芽种子数/供试种子数× 100%, 从每个发芽盒中随机挑取10株测量根长和苗高, 结果取其平均值[13]。
生理指标的测定:15 d后测定生理指标, 采用乙醇提取法测定叶绿素含量[14], 采用紫外吸收法测定过氧化氢酶(catalase, CAT)活性, 采用愈创木酚分光光度法测定过氧化物酶(peroxidase, POD)活性[15]。
采用Microsoft Excel 2016软件制图, 采用SPSS 22.0数据统计软件对数据进行单因素方差分析(One-way ANOVA), P< 0.05为差异显著性判断标准。
在供试浓度范围内, 光叶紫花苕子地上部和地下部5种浓度梯度浸提液对紫花苜蓿种子的发芽率均具有明显的抑制作用; 在地上部浸提液浓度为40 g· L-1时, 白三叶种子的发芽率与对照相比显著减少62.5%; 而与对照相比, 不同部位的光叶紫花苕子浸提液对黑麦草、燕麦种子发芽无显著性抑制(图1和图2)。
 | 图1 光叶紫花苕子地上部浸提液对4种牧草种子发芽率的影响Fig.1 Influence of V. villosa aboveground part extract on seed germination of four grass species |
2.2.1 不同浓度光叶紫花苕子浸提液对牧草幼苗根长的影响 光叶紫花苕子地上部和地下部浸提液均对黑麦草幼苗根长有明显的抑制作用, 且浓度越高抑制效果越明显; 地上部浸提液为2.5~20 g· L-1时, 紫花苜蓿幼苗根长与对照相比无显著性差异, 而当浓度为40 g· L-1时, 导致其无法生长, 地下部浸提液为10~40 g· L-1时, 紫花苜蓿幼苗根长与对照相比差异显著; 在地上部浸提液为2.5和10 g· L-1时和地下部浸提液为5和20 g· L-1时, 白三叶幼苗根长与对照相比有显著性差异, 而在地上部浸提液浓度为20和40 g· L-1和地下部浸提液浓度为40 g· L-1时无法正常生长; 与对照相比, 不同部位的光叶紫花苕子浸提液对燕麦幼苗根长无显著性影响(图3和图4)。
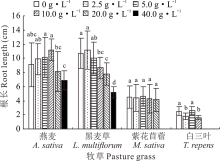 | 图3 光叶紫花苕子地上部浸提液对4种牧草幼苗根长的影响Fig.3 Influence of V. villosa aboveground part extract on root length of four grass species |
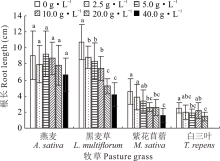 | 图4 光叶紫花苕子地下部浸提液对4种牧草幼苗根长的影响Fig.4 Influence of V. villosa underground part extract on root length of four grass species |
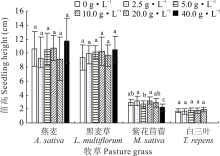
2.2.2 不同浓度光叶紫花苕子浸提液对牧草幼苗苗高的影响 地上部浸提液在2.5~20 g· L-1时, 紫花苜蓿幼苗苗高与对照相比无显著性差异, 当地下部浸提液浓度为40 g· L-1时, 其幼苗苗高与对照相比显著减少25.04%; 白三叶在地上部浸提液浓度为20和40 g· L-1和地下部浸提液浓度为40 g· L-1时无法正常生长, 其他不同浓度的处理与对照相比苗高无显著性差异; 不同部位的光叶紫花苕子浸提液对燕麦、黑麦草幼苗苗高无显著性影响(图5和图6)。
 | 图5 光叶紫花苕子地上部浸提液对4种牧草幼苗苗高的影响Fig.5 Influence of V. villosa aboveground part extract on seedling height of four grass species |
2.3.1 不同浓度光叶紫花苕子浸提液对牧草幼苗叶绿素含量的影响 在供试浓度范围内, 地上部与地下部浸提液显著提高燕麦幼苗的叶绿素含量, 地下部浸提液为20 g· L-1时, 燕麦幼苗的叶绿素与对照相比提高144.23%; 在地上部各浓度浸提液处理下, 随着浸提液浓度的增加, 黑麦草幼苗的叶绿素含量先升高后降低, 地下部浸提液为40 g· L-1时, 其与对照相比无显著性差异; 紫花苜蓿与白三叶幼苗的叶绿素含量均随着浸提液浓度的增加而降低(表1)。
| 表1 光叶紫花苕子水浸提液对受体植物叶绿素含量的影响 Table 1 Effects of water extract from V. villosa on chlorophyll content in recipient plants (mg· g-1 FW) |
2.3.2 不同浓度光叶紫花苕子浸提液对牧草幼苗 POD活性的影响 在供试浓度范围内, 地上部浸提液显著降低燕麦与黑麦草幼苗的POD活性, 而地下部浸提液处理下, 紫花苜蓿与白三叶幼苗的POD活性均与对照相比显著增强(表2)。供试地上部浸提液浓度为5 g· L-1时, 燕麦幼苗的POD活性与对照相比降低48.87%; 在浓度为10 g· L-1时, 黑麦草幼苗的POD活性与对照相比降低39.30%。供试地下部浸提液浓度为2.5 g· L-1时, 紫花苜蓿幼苗的POD活性与对照相比增加52.74%, 在浓度为5 g· L-1时, 白三叶幼苗的POD活性与对照相比增加34.68%。
| 表2 光叶紫花苕子水浸提液对受体植物POD活性的影响 Table 2 Effects of water extract from V. villosa on POD activity of receptor plants (U· g-1· min-1 FW) |
2.3.3 不同浓度光叶紫花苕子浸提液对牧草幼苗CAT活性的影响 在供试浓度范围内, 光叶紫花苕子浸提液对4种牧草幼苗CAT活性均有显著影响(表3)。在地上部浸提液浓度为2.5~10 g· L-1时, 显著降低燕麦幼苗CAT活性; 在地上部浸提液浓度为20 g· L-1时, 黑麦草幼苗的CAT活性相比对照提高33.90%。地下部浸提液对紫花苜蓿幼苗CAT活性的影响大于地上部浸提液, 在地下部浸提液浓度为40 g· L-1时, 其相比对照降低34.02%。不同部位浸提液显著增加白三叶幼苗CAT活性, 在地下部浸提液浓度为5 g· L-1时, 其相比对照提高98.38%。
| 表3 光叶紫花苕子水浸提液对受体植物CAT活性的影响 Table 3 Effects of water extract from V. villosa on CAT activity of receptor plants (U· g-1· min-1 FW) |
植物的化感作用主要表现在对受试植物种子萌发及幼苗生长的影响[10], 不同植物的化感作用敏感程度不同, 化感物质具有选择性和专一性, 且化感作用与水浸提液的浓度有关[16]。紫花苜蓿地上部浸提液对少花蒺藜草(Cenchrus pauciflorus)种子萌发的抑制作用强于地下部浸提液[17]。苯甲酸和水杨酸等化感物质降低了大豆(Glycine max)的生长[18]。花椒(Zanthoxylum bungeanum)浸提液对苜蓿、白三叶的萌发有显著抑制作用, 且化感作用随花椒浸提液浓度的升高而增强, 但对草地早熟禾(Poa pratensis)、高丹草(Sorghum bicolor× S. sudanense cv.)的抑制作用不显著[19]。本研究显示, 光叶紫花苕子不同部位浸提液对受试4种牧草种子萌发有不同程度的化感作用, 地上部浸提液对紫花苜蓿、白三叶种子的萌发有显著的抑制作用, 且随浓度的升高对白三叶种子萌发的抑制作用增强。当供试浸提液浓度升高时, 紫花苜蓿和白三叶根部发生霉烂, 甚至坏死, 说明根直接接触水浸提液中起作用的化感物质, 更容易受到伤害, 而地上部靠吸收营养物质满足需要, 只有当根系受害达到一定程度时, 地上部才表现出受害症状, 这与前人研究结果相一致[20, 21]。
光合作用是植物代谢的基础, 叶绿素是光能吸收与转换的主要物质, 其含量直接影响植株对光能的利用。化感物质会对植物细胞造成一定的损害, 植物的叶绿素合成因化感物质的参与而受到影响, 打破植物的正常光合作用。在黄花草木樨浸提液对黑麦草与苏丹草(Sorghum sudanense)的叶绿素含量影响的研究中, 浸提液处理均低于对照叶绿素含量[22], 本试验与其结果类似, 紫花苜蓿与白三叶处理组的叶绿素含量均低于对照组。在植物正常生长时, 体内活性氧的产生与消除处于稳定的动态平衡中, 当植物受到胁迫时, 植物体内的活性氧会逐渐积累, 植物细胞内的稳定环境被打破, 抗氧化酶系统被认为是重要的防御体系[23]。抗氧化酶系统防御效果与各个保护酶之间的综合协调有关, CAT与POD将植物体内的H2O2分解成H2O与O2, 可以清除活性氧的积累, 减少其对植物细胞的损害。青蒿素对黑麦草、白三叶和光叶紫花苕子幼苗的抗氧化酶活性影响各异, POD和CAT对青蒿素响应不同, 说明它们对青蒿素敏感程度不一样[24]。本试验中, 在供试浓度范围内, 光叶紫花苕子浸提液对4种牧草的POD和CAT活性均有显著影响, 紫花苜蓿与白三叶POD、CAT活性与对照相比差异显著。由此可见, 光叶紫花苕子浸提液能引起植物体内活性氧的浓度变化, 激发抗氧化酶系统抵御伤害。光叶紫花苕子浸提液对紫花苜蓿与白三叶的POD、CAT活性影响有所不同, 可能是牧草种子不同, 对浸提液的敏感程度不一样。
本试验研究了紫花苕子地上部与地下部浸提液的化感作用, 结果表明光叶紫花苕子浸提液对受体植物的种子萌发和幼苗生长表现出不同程度的化感作用, 浸提液对紫花苜蓿与白三叶的化感作用强于燕麦与黑麦草。地上部浸提液显著抑制紫花苜蓿与白三叶种子的发芽率, 且白三叶种子的发芽率随浓度升高抑制作用增强, 在地上部浸提液浓度为40 g· L-1时, 造成紫花苜蓿和白三叶幼苗均无法生长。光叶紫花苕子浸提液可以抑制紫花苜蓿与白三叶的发芽率与根长, 降低叶绿素含量及改变酶活性等生理指标进而影响其生长, 这可能与光叶紫花苕子中的化感物质有关。本试验仅在室内进行, 避免了外界环境条件下多种因素的干扰, 因此研究光叶紫花苕子的化感作用需要室内与外界自然环境相结合, 对所得结果要进一步研究。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|